Clear Sky Science · fr
Un modèle computationnel fondé sur des règles de la régulation du système MAPK/ERK
Pourquoi de petits interrupteurs cellulaires sont importants
Chaque seconde, nos cellules doivent décider de croître, se diviser, se déplacer ou s'autodétruire. Un décideur central est une chaîne de protéines appelée voie MAPK/ERK. C’est aussi l’un des systèmes les plus fréquemment perturbés dans le cancer. Bien que les manuels présentent souvent cette voie comme une simple transmission en relay, il s’agit en réalité d’un réseau dense de composants en interaction. Cette étude construit un modèle informatique détaillé de ce réseau pour poser une question pratique : comment une même voie peut-elle produire à la fois des réponses graduées et des décisions franches du type tout-ou-rien, et comment des protéines étroitement apparentées coopèrent-elles ou s’opposent-elles pour contrôler le destin cellulaire ?
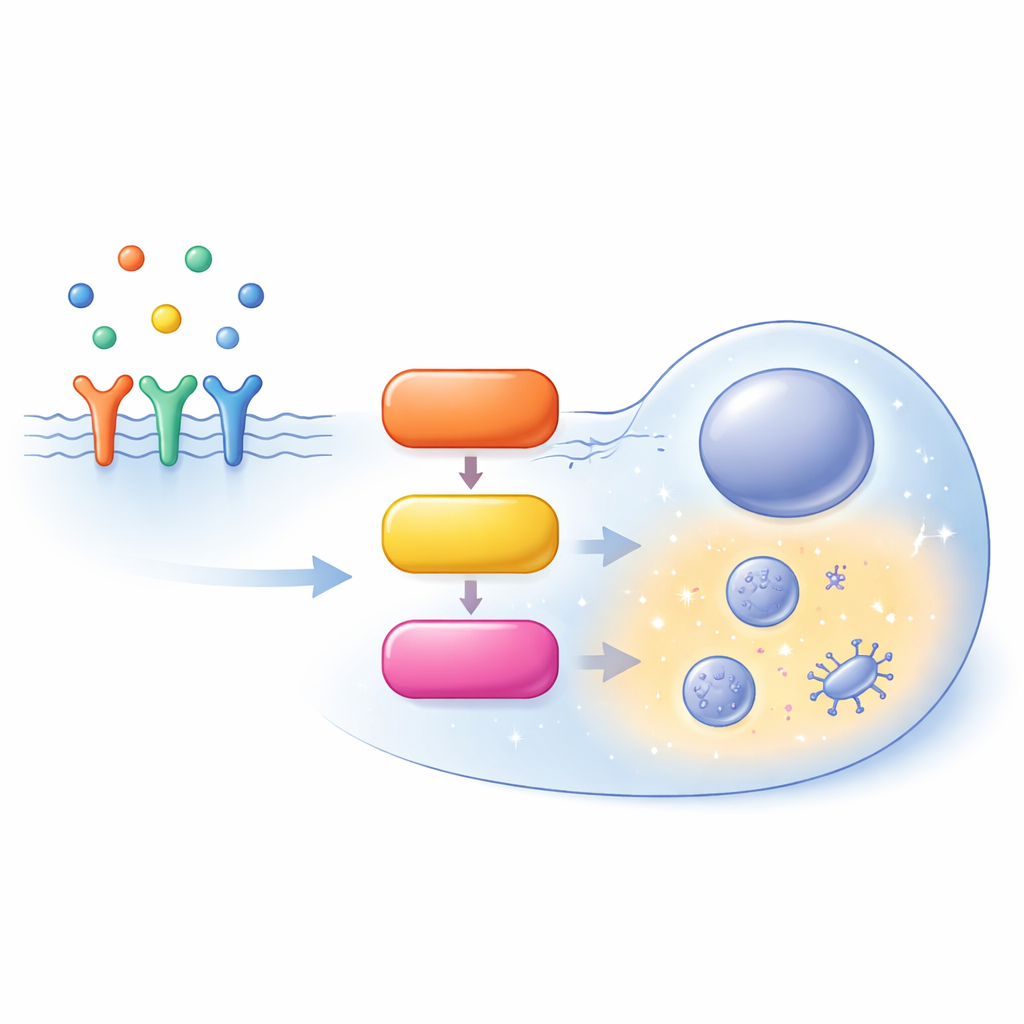
Une autoroute très fréquentée à l’intérieur de la cellule
La voie MAPK/ERK commence à la surface cellulaire, où des facteurs de croissance se lient à des récepteurs et recrutent une protéine d’aide appelée SOS. SOS active RAS, un petit interrupteur moléculaire ancré à la face interne de la membrane plasmique. RAS actif recrute ensuite une famille d’enzymes appelées RAF, qui activent MEK, lequel active à son tour ERK. ERK activé régule ensuite des centaines de cibles dans toute la cellule, influençant la prolifération, la différenciation, la migration ou la mort programmée. Plutôt que d’être une simple ligne droite, cette route est pleine de boucles de rétroaction, de embranchements et de variantes parallèles des mêmes protéines (isoformes), rendant son comportement très dépendant du contexte.
Du simple cascade au réseau fondé sur des règles
Pour capturer cette complexité, les auteurs utilisent la modélisation fondée sur des règles, une méthode qui encode des motifs d’interaction au lieu d’énumérer chaque état moléculaire possible un par un. Leur modèle inclut deux versions de MEK (MEK1 et MEK2) et trois versions de RAF (BRAF, CRAF et ARAF), ainsi que des partenaires régulateurs tels que les protéines 14-3-3. Il intègre aussi une rétroaction renforçante (où RAS actif stimule son propre activateur SOS) et trois rétroactions inhibitrices (où ERK actif atténue SOS, RAF et MEK). Parce que chaque protéine peut être modifiée et liée de nombreuses façons, un modèle traditionnel deviendrait explosif en taille ; l’approche par règles le maintient raisonnable tout en représentant plus de 600 espèces moléculaires distinctes et des milliers de réactions.
Expliquer des signaux gradués et en forme d’interrupteur
Les expériences ont montré un motif déroutant : au niveau de RAS et de RAF, l’activité augmente progressivement lorsque la dose de facteur de croissance s’élève, mais en bas de la cascade ERK s’allume souvent de façon quasiment tout-ou-rien. Le modèle l’explique en proposant que, à faibles doses, RAS ne s’active que par petits patchs sur la membrane cellulaire. Lorsqu’on augmente la dose, une plus grande fraction de la membrane passe à l’état actif. Localement, l’interrupteur RAS est bistable — il bascule brutalement de l’état éteint à l’état allumé — mais parce qu’une fraction seulement de la membrane est active, l’activité moyenne de RAS et de RAF sur l’ensemble de la cellule paraît lisse. En aval, l’activation en deux étapes de MEK et ERK agit comme un amplificateur puissant, de sorte que même une activité amont modeste produit une activation presque complète d’ERK, donnant une réponse nette de type interrupteur. La rétroaction négative d’ERK vers SOS transforme ensuite une stimulation continue en pulses rythmiques d’activité ERK, dont la période dépend de l’intensité du facteur de croissance et de la force de la rétroaction.
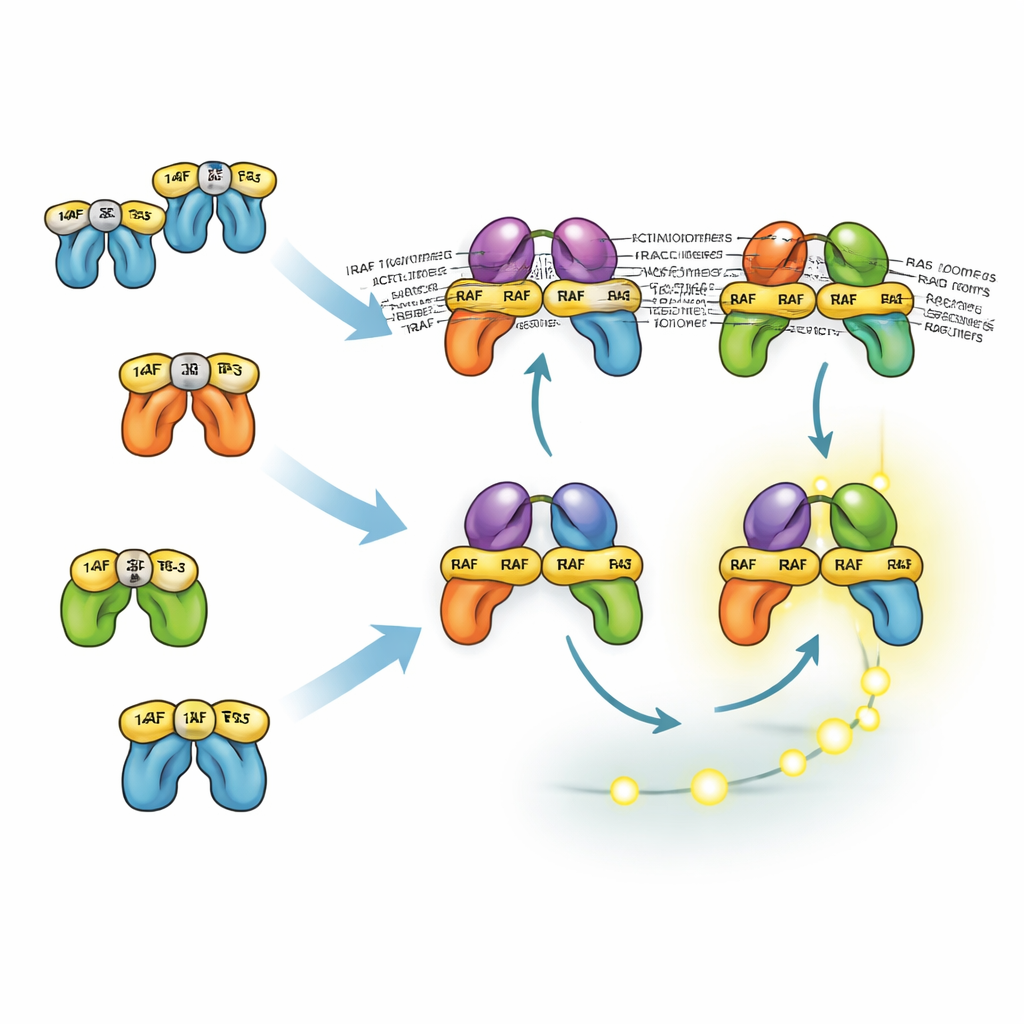
Comment des protéines semblables se partagent et se distribuent les tâches
Les trois isoformes RAF se comportent différemment en raison de leurs interactions avec les protéines 14-3-3, qui peuvent à la fois verrouiller les molécules RAF dans une conformation inactive et stabiliser des paires RAF actives. Le principal site d’accrochage de 14-3-3 sur BRAF se situe à son extrémité C-terminale, ce qui lui permet de rester associé à 14-3-3 tout en se liant à RAS et en formant des dimères avec CRAF ou ARAF. Ces dimères mixtes sont particulièrement stables et efficaces pour activer MEK. En revanche, CRAF et ARAF dépendent davantage d’un lien en tête avec 14-3-3, ce qui bloque leur recrutement par RAS. Par conséquent, les dimères dépourvus de BRAF sont moins stables et généralement moins abondants. Pourtant, le modèle montre que, même sans BRAF, les cellules peuvent encore générer de forts signaux ERK parce que la rétroaction positive en amont et l’amplification en aval compensent. Cela aide à expliquer pourquoi les médicaments ciblant uniquement BRAF suppriment souvent ERK de façon partielle et doivent être associés à des inhibiteurs de MEK ou d’ERK.
Équilibrer mouvement, survie et mort
Le modèle suit aussi des rôles de RAF qui dépassent l’activation d’ERK. Lorsque des dimères se dissocient sous l’effet de rétroactions négatives entraînées par ERK, des formes ouvertes de CRAF peuvent se lier à des partenaires contrôlant le mouvement cellulaire et la survie, tels que la kinase ROKα ou la protéine pro-apoptotique MST2. Au fur et à mesure que les niveaux de facteur de croissance et l’abondance de 14-3-3 varient, l’équilibre bascule entre des dimères riches en BRAF qui stimulent fortement ERK, des complexes à base de CRAF et ARAF qui modulent la motilité, et des pools qui libèrent MST2 pour promouvoir la mort cellulaire. Parce que ces équilibres répondent de façon continue à la force du stimulus tandis que la sortie d’ERK peut être presque binaire, une même voie peut à la fois ajuster des aspects subtils du comportement et prendre des décisions tranchées sur le destin.
Ce que cela implique pour la compréhension des cellules
En tissant interactions spécifiques aux isoformes, basculements locaux de la membrane et boucles de rétroaction emboîtées, le modèle montre comment une voie moléculaire peut agir à la fois comme un variateur et comme un interrupteur numérique. Les variations des quantités de BRAF, CRAF, ARAF, MEK1, MEK2 et 14-3-3, observées entre tissus et tumeurs, conduisent naturellement à des motifs dynamiques différents de signalisation ERK, des pulsations aux plateaux soutenus. Cela suggère que le câblage propre à chaque type cellulaire des mêmes composants de base peut réutiliser la voie MAPK/ERK pour des rôles physiologiques divers, et que des thérapies efficaces devront prendre en compte non seulement des cibles isolées mais l’ensemble du contexte régulateur dans lequel ces interrupteurs moléculaires opèrent.
Citation: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Mots-clés: signalisation MAPK ERK, isoformes RAF, régulation 14-3-3, modèle computationnel de voie, dynamique du destin cellulaire