Clear Sky Science · ar
نموذج حاسوبي قائم على القواعد لتنظيم نظام MAPK/ERK
لماذا تهم مفاتيح الخلايا الصغيرة
كل ثانية، يجب على خلايانا أن تقرر ما إذا كانت ستنمو أو تنقسم أو تتحرك أو تدمر نفسها. أحد صانعي القرار المركزيين هو سلسلة من البروتينات تُعرف بمسار MAPK/ERK. وهو أيضًا أحد أكثر الأنظمة تعرضًا للاضطراب في السرطان. وعلى رغم أن الكتب الدراسية تعرض هذا المسار غالبًا كمرحل بسيط، إلا أنه في الواقع شبكة كثيفة من الأجزاء المتفاعلة. تبني هذه الدراسة نموذجًا حاسوبيًا مفصّلًا لتلك الشبكة لطرح سؤال عملي: كيف يمكن لمسار واحد أن يولّد في الوقت نفسه استجابات ناعمة متدرجة وقرارات حاسمة من نوع كل شيء أو لا شيء، وكيف تتعاون البروتينات المتقاربة أو تتنافس للتحكم في مصير الخلية؟
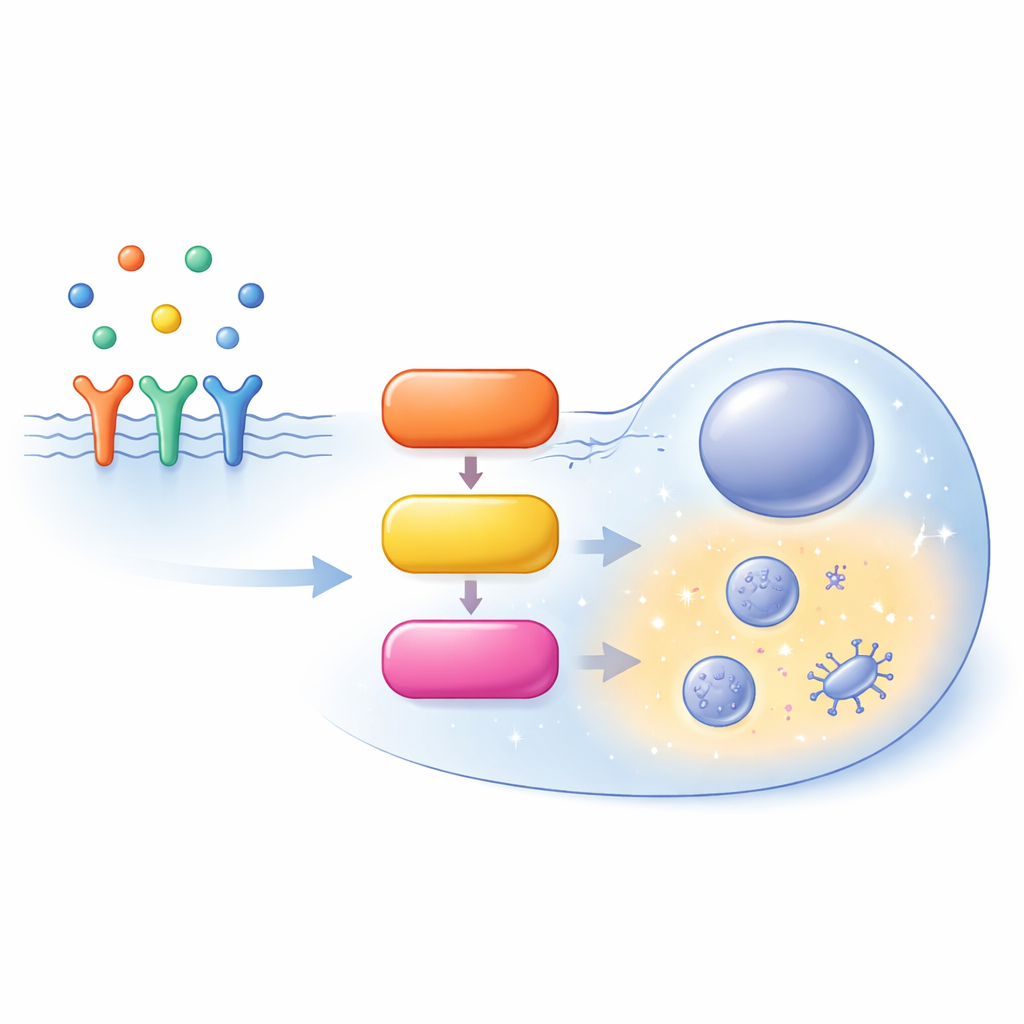
طريق سريع مزدحم داخل الخلية
يبدأ مسار MAPK/ERK على سطح الخلية، حيث ترتبط عوامل النمو بمستقبلات وتستقطب بروتينًا مساعدًا يُسمى SOS. يُفعّل SOS بروتين RAS، وهو مفتاح جزيئي صغير مربوط بالوجه الداخلي لغشاء الخلية. يقوم RAS النشط بعد ذلك بتجنيد عائلة من الإنزيمات المعروفة باسم RAF، التي تُفعّل MEK، والتي بدورها تُفعّل ERK. يقوم ERK المُفعّل بتنظيم مئات الأهداف في أنحاء الخلية، مهيئًا ما إذا كانت الخلية ستتكاثر أو تختلف أو تهاجر أو تدخل في موت مبرمج. بدلاً من أن يكون خطًا مستقيمًا بسيطًا، فإن هذا المسار مليء بحلقات التغذية الراجعة والتفرعات وأنواع متوازية من نفس البروتينات (أشكال متغايرة)، مما يجعل سلوكه معتمدًا بدرجة كبيرة على السياق.
من سلسلة بسيطة إلى شبكة قائمة على القواعد
لالتقاط هذه التعقيدات، يستخدم المؤلفون النمذجة القائمة على القواعد، وهي طريقة تُشفّر أنماط التفاعل بدلًا من سرد كل حالة جزيئية ممكنة وحدة بوحدة. يتضمن نموذجهم نسختين من MEK (MEK1 وMEK2) وثلاثة أشكال من RAF (BRAF وCRAF وARAF)، بالإضافة إلى شركاء تنظيميّين مثل بروتينات 14-3-3. كما يبني النموذج حلقة تعزيز واحدة (حيث يقوم RAS النشط بتعزيز منشطه SOS) وثلاث حلقات تثبيط (حيث يقوم ERK النشط بتقليل نشاط SOS وRAF وMEK). ونظرًا لأن كل بروتين يمكن تعديله والارتباط بطرق عديدة، فإن نموذجًا تقليديًا سيزيد بسرعة من التعقيد؛ تحافظ المقاربة القائمة على القواعد على قابلية الإدارة مع تمثيل أكثر من 600 نوع جزيئي مميز وآلاف التفاعلات.
تفسير الإشارات المتدرجة وشبيهة المفتاح
أظهرت التجارب نمطًا محيرًا: على مستوى RAS وRAF، تزداد النشاطية تدريجيًا مع ارتفاع جرعة عامل النمو، لكن في نهاية السلسلة غالبًا ما يُشغل ERK بطريقة شبه كل شيء أو لا شيء. يفسّر النموذج هذا بالقول إنه عند الجرعات المنخفضة، ينشط RAS فقط في قطع صغيرة من غشاء الخلية. مع ازدياد الجرعة، يتحول المزيد من الغشاء للحالة النشطة. محليًا، يكون مُفتاح RAS ثنائي الاستقرار—ينتقل فجأة من إيقاف إلى تشغيل—لكن لأن جزءًا فقط من الغشاء نشط، يبدو المتوسط عبر الخلية لنشاط RAS وRAF ناعمًا. في المراحل اللاحقة، يعمل التنشيط المكوّن من خطوتين لـMEK وERK كمكبر قوي، بحيث إن نشاطًا علويًا متواضعًا ينتج عنه تنشيط شبه كامل لـERK، مما يؤدي إلى استجابة حادة تشبه المفتاح. ثم تحوّل التغذية الراجعة السالبة من ERK إلى SOS التحفيز الثابت إلى نبضات إيقاعية لنشاط ERK، تعتمد فترة هذه النبضات على قوة عامل النمو وشدة التغذية الراجعة.
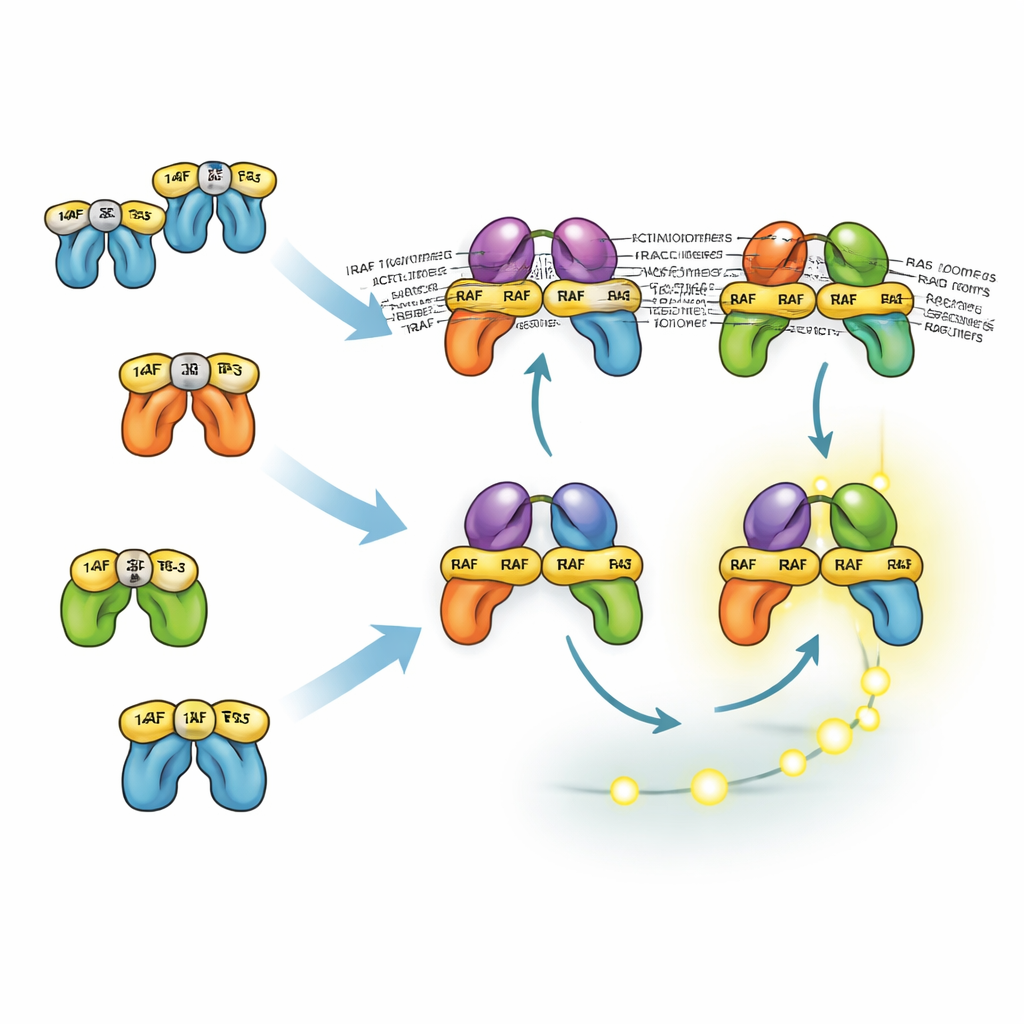
كيف تتقاسم البروتينات الشبيهة المهام
تتصرف الأشكال الثلاثة من RAF بشكل مختلف بسبب كيفية تفاعلها مع بروتينات 14-3-3، التي يمكن أن تقفل جزيئات RAF في شكل غير نشط وتثبّت الأزواج النشطة من RAF. يقع موقع الارتباط الرئيسي لـBRAF مع 14-3-3 في ذيله، ما يسمح له بالبقاء مرتبطًا بـ14-3-3 بينما يظل قادرًا على الارتباط بـRAS وتشكيل ثنائيات مع CRAF أو ARAF. هذه الثنائيات المختلطة مستقرة وفعّالة بشكل خاص في تفعيل MEK. في المقابل، يعتمد CRAF وARAF أكثر على الارتباط من نهاية الرأس بـ14-3-3، مما يمنع توظيفهما إلى RAS. ونتيجة لذلك، تكون الثنائيات التي تفتقر إلى BRAF أقل استقرارًا وعادةً أقل وفرة. ومع ذلك يُظهِر النموذج أنه حتى بدون BRAF، يمكن للخلايا أن تولّد إشارات ERK قوية لأن التعزيز العلوي والتضخيم السفلي يعوّضان عن ذلك. يساعد هذا على تفسير لماذا غالبًا ما تُثبط الأدوية التي تستهدف BRAF وحده ERK جزئيًا فقط وتُستعمل مع مثبطات MEK أو ERK.
موازنة الحركة والبقاء والموت
يتتبّع النموذج أيضًا أدوار RAF التي تتجاوز تشغيل ERK. عندما تنهار الثنائيات تحت تأثير التغذية الراجعة السالبة المحفّزة من ERK، يمكن لأشكال CRAF المفتوحة أن ترتبط بشركاء يتحكمون في حركة الخلية وبقائها، مثل الكيناز ROKα أو بروتين القتل البرنامجي MST2. مع تغيّر مستويات عامل النمو ووفرة 14-3-3، يتبدّل التوازن بين ثنائيات غنية بـBRAF التي تدفع ERK بقوة، ومجمعات قائمة على CRAF وARAF تعدّل الحركة، وحمامات تحرّر MST2 لتعزيز موت الخلية. وبما أن هذه التوازنات تستجيب بنعومة لقوة المنبه بينما يمكن أن يكون مخرج ERK شبه كل شيء أو لا شيء، فإن نفس المسار يمكنه ضبط جوانب دقيقة من السلوك وفي الوقت نفسه اتخاذ خيارات مصيرية حاسمة.
ما الذي يعنيه هذا لفهم الخلايا
بجمع التفاعلات الخاصة بالأشكال المتغايرة، والتحوّل المحلي لغشاء الخلية، وحلقات التغذية الراجعة المتداخلة، يظهر النموذج كيف يمكن لمجرى جزيئي واحد أن يعمل كمخفض مُضاء وكـمفتاح رقمي في آن واحد. تؤدي التباينات في كميات BRAF وCRAF وARAF وMEK1 وMEK2 و14-3-3، كما لوحظ عبر الأنسجة والأورام، بطبيعة الحال إلى أنماط ديناميكية مختلفة لإشارات ERK، من نبضات إلى هضبات مستمرة. يقترح هذا أن توصيل الخلايا المحدد للنوع لنفس المكونات الأساسية يمكن أن يعيد توظيف مسار MAPK/ERK لأدوار فسيولوجية متنوعة، وأن العلاجات الفعالة ستحتاج إلى مراعاة ليس الهدف المفرد فحسب بل السياق التنظيمي الكامل الذي تعمل فيه هذه المفاتيح الجزيئية.
الاستشهاد: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
الكلمات المفتاحية: إشارة MAPK ERK, أشكال RAF المتغايرة, تنظيم 14-3-3, نموذج مسار حاسوبي, ديناميكيات مصير الخلية