Clear Sky Science · pl
Obliczeniowy model regułowy regulacji układu MAPK/ERK
Dlaczego małe przełączniki komórkowe mają znaczenie
Co sekundę nasze komórki muszą zdecydować, czy rosnąć, dzielić się, przemieszczać czy się samobójczo zniszczyć. Kluczowym decydentem jest łańcuch białek zwany szlakiem MAPK/ERK. Jest to także jeden z najczęściej zaburzanych systemów w nowotworach. Chociaż w podręcznikach szlak ten bywa przedstawiany jako prosty przekaźnik, w rzeczywistości to gęsta sieć wzajemnych interakcji. W tej pracy zbudowano szczegółowy model komputerowy tej sieci, aby postawić praktyczne pytanie: jak jeden szlak może jednocześnie generować łagodne, stopniowe odpowiedzi i ostre, wszystko-albo-nic decyzje, oraz jak blisko spokrewnione białka współpracują lub konkurują, by kontrolować los komórki?
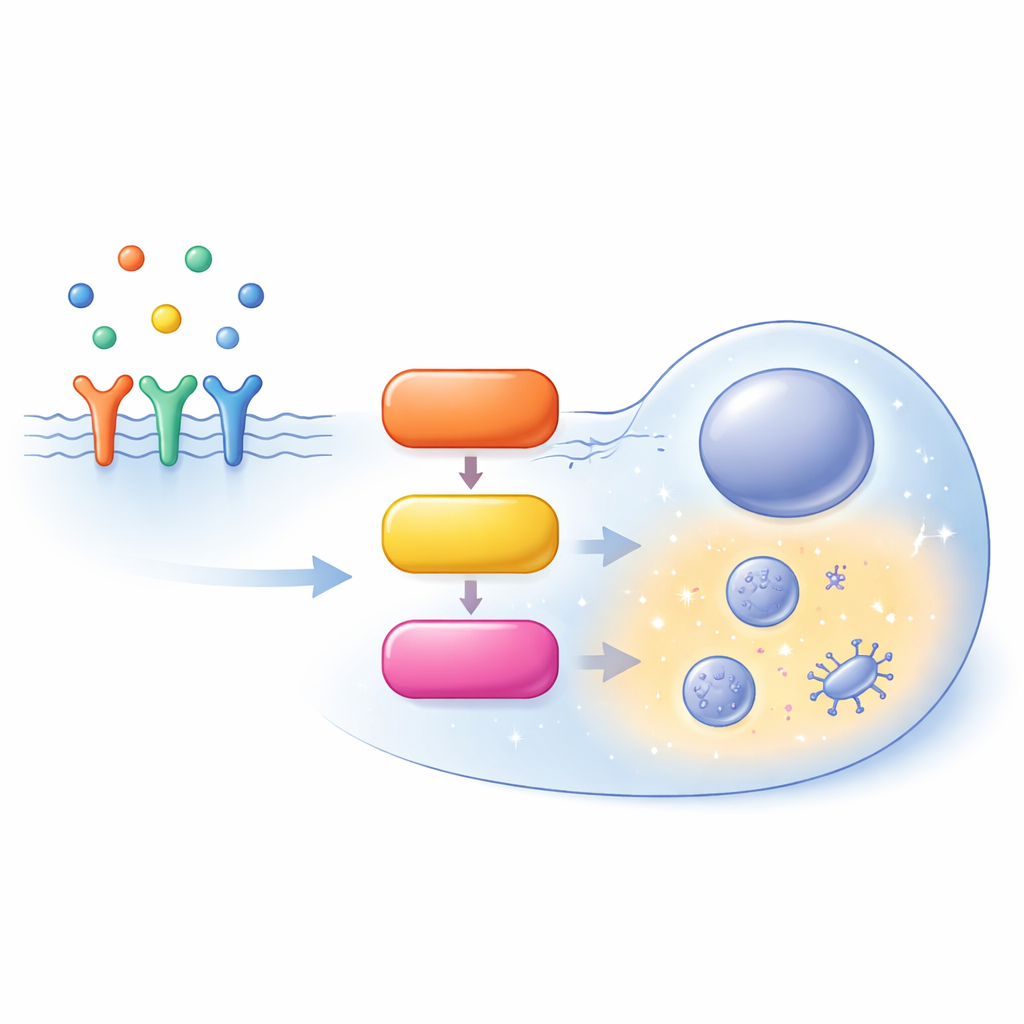
Zajęta autostrada wewnątrz komórki
Szlak MAPK/ERK zaczyna się na powierzchni komórki, gdzie czynniki wzrostu wiążą receptory i rekrutują białko pomocnicze zwane SOS. SOS aktywuje RAS, mały przełącznik molekularny przytwierdzony do wewnętrznej warstwy błony komórkowej. Aktywny RAS rekrutuje rodzinę enzymów znanych jako RAF, które aktywują MEK, a te z kolei aktywują ERK. Aktywowany ERK reguluje setki celów w całej komórce, kształtując, czy komórka się proliferuje, różnicuje, przemieszcza czy przechodzi programowaną śmierć. Zamiast prostego szlaku liniowego, trasa ta pełna jest pętli sprzężeń zwrotnych, rozgałęzień i równoległych wariantów tych samych białek (izoform), co sprawia, że jej zachowanie zależy silnie od kontekstu.
Od prostej kaskady do sieci regułowej
Aby uchwycić tę złożoność, autorzy wykorzystali modelowanie regułowe, metodę kodującą wzorce interakcji zamiast wypisywać każdy możliwy stan molekularny z osobna. Ich model obejmuje dwie wersje MEK (MEK1 i MEK2) oraz trzy wersje RAF (BRAF, CRAF i ARAF), jak również regulatorowe partnera, takie jak białka 14-3-3. Wbudowano też jedno wzmacniające sprzężenie zwrotne (gdzie aktywny RAS zwiększa aktywność swojego aktywatora SOS) i trzy hamujące sprzężenia zwrotne (gdzie aktywny ERK tłumi SOS, RAF i MEK). Ponieważ każde białko może być modyfikowane i związane na wiele sposobów, tradycyjny model eksplodowałby w rozmiarze; podejście regułowe utrzymuje model w ryzach, jednocześnie reprezentując ponad 600 odrębnych gatunków molekularnych i tysiące reakcji.
Tłumaczenie sygnałów stopniowych i przełącznikowych
Eksperymenty wykazały zagadkowy wzorzec: na poziomie RAS i RAF aktywność rośnie stopniowo wraz ze wzrostem dawki czynnika wzrostu, lecz na końcu kaskady ERK często włącza się w sposób niemal wszystko-albo-nic. Model wyjaśnia to proponując, że przy niskich dawkach RAS aktywuje się tylko w małych plamach błony komórkowej. W miarę wzrostu dawki więcej obszarów błony przechodzi w stan aktywny. Lokalnie przełącznik RAS jest bistabilny — przechodzi gwałtownie z wyłączonego na włączony — ale ponieważ aktywna jest tylko część błony, średnia aktywność RAS i RAF w całej komórce wydaje się gładka. Dalej, dwuetapowa aktywacja MEK i ERK działa jak potężny wzmacniacz, tak że nawet umiarkowana aktywność upstream prowadzi do niemal pełnej aktywacji ERK, dając ostry, przełącznikowy efekt. Ujemne sprzężenie zwrotne z ERK do SOS następnie przekształca stałą stymulację w rytmiczne pulsacje aktywności ERK, których okres zależy od siły czynnika wzrostu i intensywności sprzężenia.
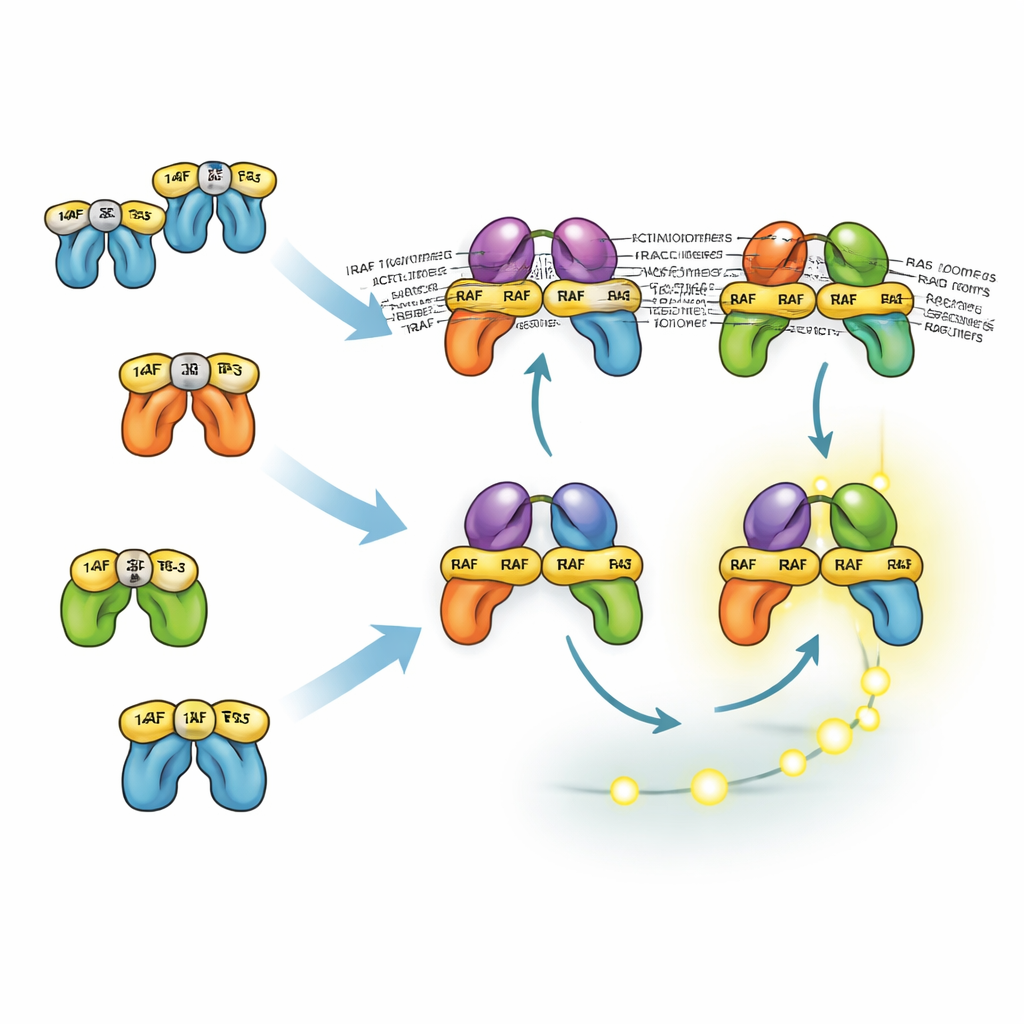
Jak podobne białka dzielą się zadaniami
Trzy izoformy RAF zachowują się odmiennie z powodu różnic w interakcjach z białkami 14-3-3, które mogą zarówno blokować RAF w nieaktywnej konformacji, jak i stabilizować aktywne pary RAF. Główne miejsce dokujące BRAF dla 14-3-3 znajduje się na jego ogonie, co pozwala mu pozostawać związanym z 14-3-3, jednocześnie wiążąc RAS i tworząc dimery z CRAF lub ARAF. Te mieszane dymery są szczególnie stabilne i efektywne w aktywacji MEK. Natomiast CRAF i ARAF bardziej polegają na wiązaniu od strony głowy z 14-3-3, co blokuje ich rekrutację do RAS. W rezultacie dimery pozbawione BRAF są mniej stabilne i zwykle rzadsze. Jednak model pokazuje, że nawet bez BRAF komórki potrafią wygenerować silne sygnały ERK, ponieważ upstreamowe dodatnie sprzężenie zwrotne i downstreamowe wzmocnienie to kompensują. To pomaga wyjaśnić, dlaczego leki celujące jedynie BRAF często tylko częściowo tłumią ERK i muszą być łączone z inhibitorami MEK lub ERK.
Równoważenie ruchu, przeżycia i śmierci
Model śledzi także role RAF wykraczające poza włączanie ERK. Kiedy dimery rozpadają się pod wpływem ujemnego sprzężenia związanego z ERK, otwarte formy CRAF mogą wiązać partnerów kontrolujących ruch i przeżycie komórki, takich jak kinaza ROKα lub pro-śmiercionośne białko MST2. W miarę jak poziomy czynnika wzrostu i ilość 14-3-3 zmieniają się, równowaga przesuwa się między dimerami bogatymi w BRAF, które silnie napędzają ERK, kompleksami opartymi na CRAF i ARAF modulującymi motorykę, a pulami uwalniającymi MST2 do promowania śmierci komórki. Ponieważ te równowagi reagują płynnie na siłę bodźca, podczas gdy output ERK może być niemal wszystko-albo-nic, ten sam szlak potrafi dostroić subtelne aspekty zachowania i jednocześnie podejmować zdecydowane wyboru losu.
Co to oznacza dla zrozumienia komórek
Poprzez splecenie interakcji specyficznych dla izoform, lokalnego przełączania błonowego i zagnieżdżonych pętli sprzężeń zwrotnych, model pokazuje, jak jeden szlak molekularny może działać zarówno jako ściemniacz, jak i cyfrowy przełącznik. Zmiany ilości BRAF, CRAF, ARAF, MEK1, MEK2 i 14-3-3, obserwowane w różnych tkankach i nowotworach, naturalnie prowadzą do różnych dynamicznych wzorców sygnalizacji ERK, od pulsów do trwałych plateau. Sugeruje to, że specyficzne dla typu komórki okablowanie tych samych podstawowych komponentów może przekształcić szlak MAPK/ERK do odmiennych ról fizjologicznych, a skuteczne terapie będą musiały brać pod uwagę nie pojedyncze cele, lecz pełny kontekst regulacyjny, w którym te molekularne przełączniki działają.
Cytowanie: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Słowa kluczowe: sygnalizacja MAPK ERK, izoformy RAF, regulacja 14-3-3, obliczeniowy model szlaku, dynamika losu komórki