Clear Sky Science · nl
Een computationeel regelgebaseerd model van de regulatie van het MAPK/ERK-systeem
Waarom kleine cellulaire schakelaars ertoe doen
Elke seconde moeten onze cellen beslissen of ze groeien, delen, bewegen of zichzelf vernietigen. Een centraal beslissingsmechanisme is een keten van eiwitten die het MAPK/ERK-pad wordt genoemd. Dit systeem is ook een van de meest verstoorde systemen bij kanker. Hoewel leerboeken dit pad vaak als een eenvoudige doorgeefketen presenteren, is het in werkelijkheid een dicht web van onderling reagerende onderdelen. Deze studie bouwt een gedetailleerd computermodel van dat web om een praktische vraag te beantwoorden: hoe kan één pad tegelijk geleidelijke, afgestelde reacties en scherpe, alles-of-niets-beslissingen produceren, en hoe werken nauw verwante eiwitten samen of concurreren ze om de celbestemming te sturen?
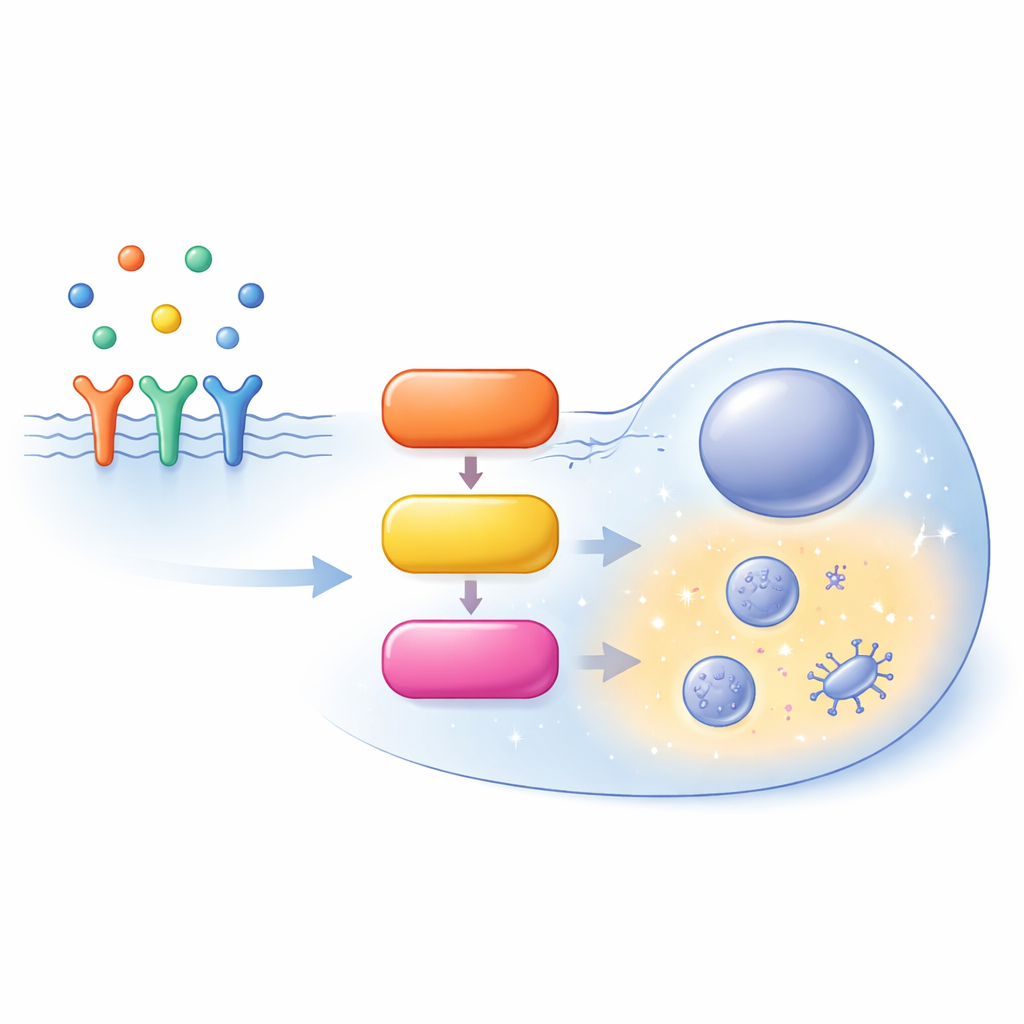
Een drukke snelweg binnenin de cel
Het MAPK/ERK-pad begint aan het celoppervlak, waar groeifactoren binden aan receptoren en een hulpstof genaamd SOS aantrekken. SOS schakelt RAS aan, een kleine moleculaire schakelaar die vastzit aan de binnenzijde van het celmembraan. Actief RAS rekruteert vervolgens een familie enzymen die bekendstaat als RAF, die MEK activeren, dat op zijn beurt ERK activeert. Geactiveerd ERK reguleert honderden doelen door de cel heen en bepaalt of de cel prolifereert, differentieert, migreert of geprogrammeerde celdood ondergaat. In plaats van een eenvoudige rechte lijn is deze route vol terugkoppelingen, vertakkingen en parallelle varianten van dezelfde eiwitten (isoformen), waardoor het gedrag sterk contextafhankelijk is.
Van eenvoudige cascade naar regelgebaseerd netwerk
Om deze complexiteit vast te leggen gebruiken de auteurs regelgebaseerde modellering, een methode die interactiepatronen codeert in plaats van elke mogelijke moleculaire toestand afzonderlijk op te sommen. Hun model bevat twee versies van MEK (MEK1 en MEK2) en drie versies van RAF (BRAF, CRAF en ARAF), evenals regulerende partners zoals 14-3-3-eiwitten. Het bouwt ook één versterkende feedback in (waarbij actief RAS zijn eigen activator SOS versterkt) en drie remmende feedbacks (waarbij actief ERK SOS, RAF en MEK dempt). Omdat elk eiwit op veel verschillende manieren kan worden gewijzigd en gebonden, zou een traditioneel model in omvang exploderen; de regelgebaseerde aanpak houdt het beheersbaar terwijl het nog steeds meer dan 600 onderscheidende moleculaire soorten en duizenden reacties weergeeft.
Graded en schakelachtige signalen verklaren
Experimenten tonen een raadselachtig patroon: op het niveau van RAS en RAF neemt de activiteit geleidelijk toe met de groeifactorconcentratie, maar onderin de cascade schakelt ERK vaak bijna alles-of-niets aan. Het model verklaart dit door voor te stellen dat RAS bij lage doses alleen in kleine vlekken van het celmembraan wordt geactiveerd. Als de dosis stijgt, schakelt een groter deel van het membraan over naar de actieve staat. Lokaal is de RAS-schakelaar bistabiel—hij springt scherp van uit naar aan—maar omdat slechts een fractie van het membraan actief is, lijkt de gemiddelde RAS- en RAF-activiteit over de hele cel glad te verlopen. Stroomsgewijs fungeert de tweestapsactivatie van MEK en ERK als een krachtige versterker, zodat zelfs bescheiden upstream-activiteit bijna volledige ERK-activatie oplevert en een scherpe, schakelachtige respons veroorzaakt. Negatieve feedback van ERK naar SOS zet dan voortdurende stimulatie om in ritmische pulsen van ERK-activiteit, waarvan de periode afhangt van de sterkte van de groeifactor en de feedbackintensiteit.
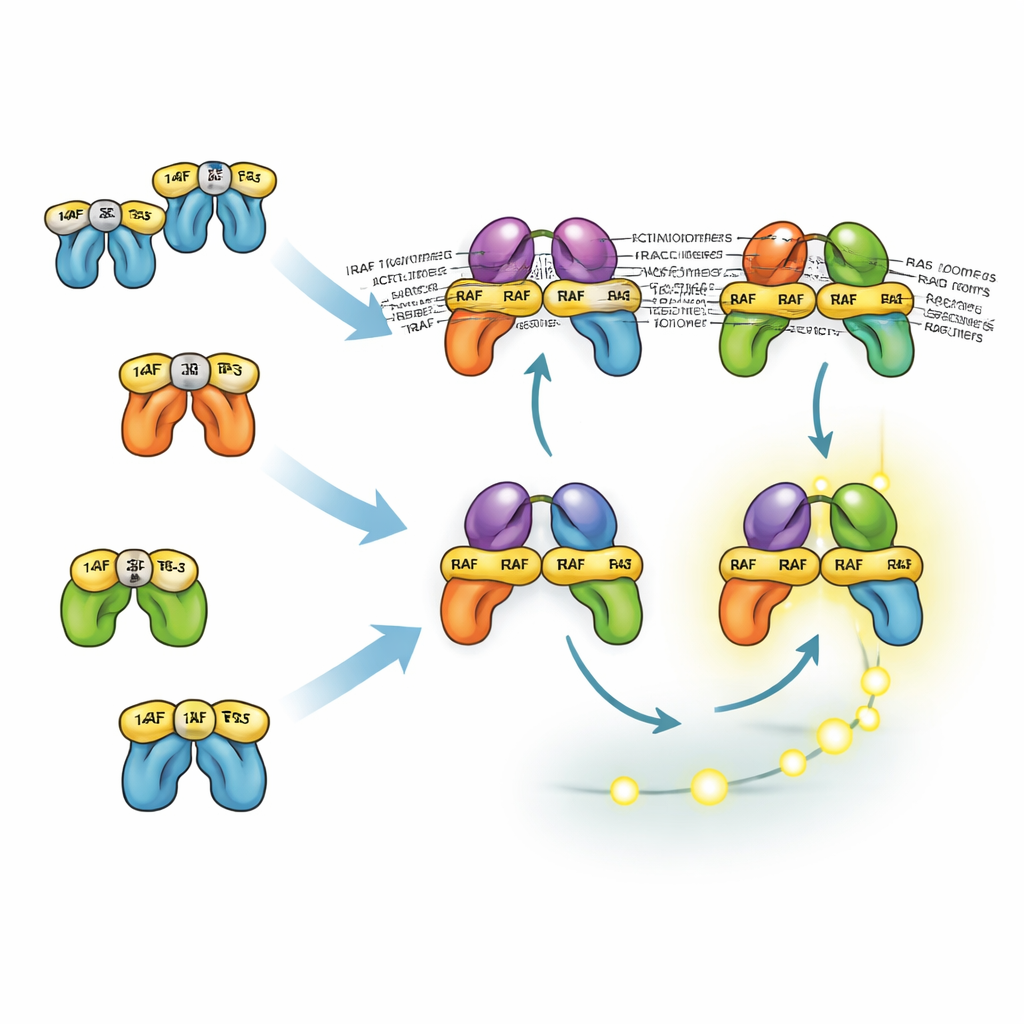
Hoe op elkaar lijkende eiwitten taken delen en verdelen
De drie RAF-isoformen gedragen zich verschillend vanwege hun interacties met 14-3-3-eiwitten, die zowel RAF-moleculen in een inactieve vorm kunnen vergrendelen als actieve RAF-paren kunnen stabiliseren. De belangrijkste aanhechtingsplaats voor 14-3-3 op BRAF ligt in de staart, waardoor het geassocieerd kan blijven met 14-3-3 terwijl het toch aan RAS bindt en dimers vormt met CRAF of ARAF. Deze gemengde dimers zijn bijzonder stabiel en efficiënt in het activeren van MEK. Daarentegen vertrouwen CRAF en ARAF meer op kop-einde binding aan 14-3-3, wat hun rekrutering naar RAS blokkeert. Als gevolg daarvan zijn dimers zonder BRAF minder stabiel en gewoonlijk minder talrijk. Het model toont echter dat zelfs zonder BRAF cellen nog steeds sterke ERK-signalen kunnen genereren omdat upstream positieve feedback en downstreamversterking compenseren. Dit helpt verklaren waarom medicijnen die alleen BRAF remmen vaak slechts gedeeltelijk ERK onderdrukken en gecombineerd moeten worden met MEK- of ERK-remmers.
Balanceren van beweging, overleving en dood
Het model volgt ook rollen van RAF die verder gaan dan alleen het inschakelen van ERK. Wanneer dimers uit elkaar vallen onder door ERK aangedreven negatieve feedback, kunnen open vormen van CRAF partners binden die beweging en overleving van de cel controleren, zoals de kinase ROKα of het pro-dood-eiwit MST2. Naarmate groeifactorniveaus en de hoeveelheid 14-3-3 veranderen, verschuift de balans tussen BRAF-rijke dimers die sterk ERK aandrijven, CRAF- en ARAF-gebaseerde complexen die motiliteit moduleren, en pools die MST2 vrijmaken om celdood te bevorderen. Omdat deze balansen soepel reageren op de sterkte van de stimulus terwijl ERK-uitvoer bijna alles-of-niets kan zijn, kan hetzelfde pad subtiele gedragsaspecten afstemmen en toch beslissende bestemmingskeuzes maken.
Wat dit betekent voor het begrijpen van cellen
Door isoformspecifieke interacties, lokale membraanschakeling en geneste feedbacklussen samen te brengen, laat het model zien hoe één moleculair pad zowel als dimmer als digitale schakelaar kan fungeren. Variaties in de hoeveelheden BRAF, CRAF, ARAF, MEK1, MEK2 en 14-3-3, zoals waargenomen in verschillende weefsels en tumoren, leiden van nature tot verschillende dynamische patronen van ERK-signalisatie, van pulsen tot aanhoudende plateaus. Dit suggereert dat celtypespecifieke bedrading van dezelfde kerncomponenten het MAPK/ERK-pad kan herbestemmen voor diverse fysiologische rollen, en dat effectieve therapieën niet alleen individuele doelen moeten beschouwen maar de volledige regelgevende context waarin deze moleculaire schakelaars functioneren.
Bronvermelding: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Trefwoorden: MAPK ERK signalering, RAF isoformen, 14-3-3 regulatie, computationeel padmodel, celbestemmingsdynamica