Clear Sky Science · de
Ein regelbasiertes Rechenmodell zur Regulation des MAPK/ERK‑Systems
Warum winzige Zellschalter wichtig sind
Sekunde für Sekunde müssen Zellen entscheiden, ob sie wachsen, sich teilen, sich bewegen oder sich selbst zerstören. Ein zentraler Entscheider ist eine Proteinkette, die als MAPK/ERK‑Signalweg bekannt ist. Dieser Weg gehört zu den am häufigsten gestörten Systemen bei Krebs. Obwohl Lehrbücher ihn oft als einfache Weiterleitung darstellen, ist er in Wirklichkeit ein dichtes Netz miteinander interagierender Bausteine. In dieser Studie wird ein detailliertes Computer‑Modell dieses Netzes aufgebaut, um eine praktische Frage zu beantworten: Wie kann ein einziger Signalweg gleichzeitig sanfte, graduelle Reaktionen und scharfe, alles‑oder‑nichts‑Entscheidungen erzeugen, und wie arbeiten eng verwandte Proteine zusammen oder konkurrieren miteinander, um das Zellschicksal zu steuern?
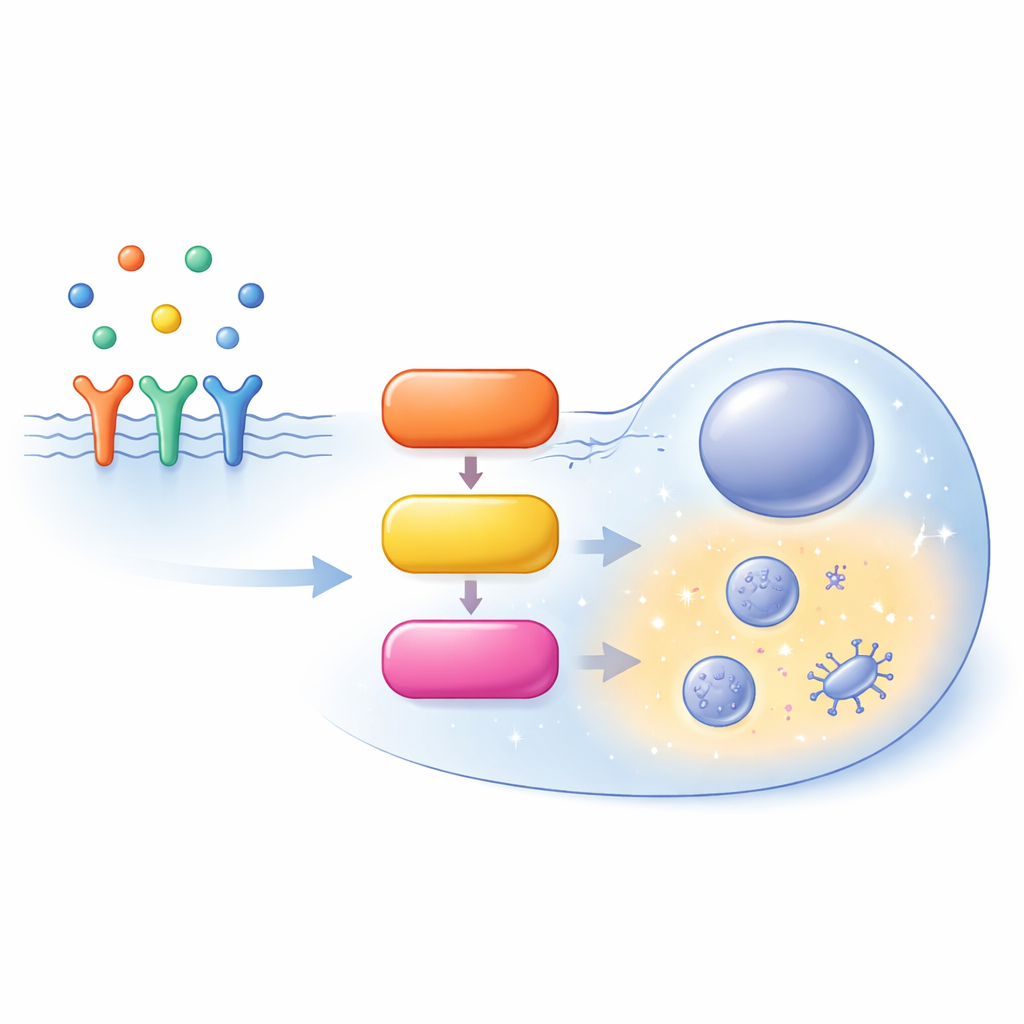
A busy highway inside the cell
Der MAPK/ERK‑Signalweg beginnt an der Zelloberfläche, wo Wachstumsfaktoren an Rezeptoren binden und das Hilfsprotein SOS rekrutieren. SOS schaltet RAS ein, einen kleinen molekularen Schalter, der an der Innenseite der Zellmembran verankert ist. Aktives RAS rekrutiert dann eine Enzymfamilie, die als RAF bezeichnet wird; diese aktivieren MEK, das wiederum ERK aktiviert. Aktiviertes ERK reguliert Hunderte von Zielmolekülen in der Zelle und bestimmt, ob eine Zelle proliferiert, differenziert, migriert oder programmierten Zelltod vollzieht. Statt einer einfachen Geraden ist diese Strecke voller Rückkopplungen, Verzweigungen und paralleler Varianten derselben Proteine (Isoformen), was ihr Verhalten stark vom Kontext abhängig macht.
Vom einfachen Kaskadenmodell zum regelbasierten Netzwerk
Um diese Komplexität zu erfassen, verwenden die Autoren regelbasiertes Modellieren, eine Methode, die Interaktionsmuster kodiert, anstatt jeden möglichen molekularen Zustand einzeln aufzulisten. Ihr Modell enthält zwei Varianten von MEK (MEK1 und MEK2) und drei Varianten von RAF (BRAF, CRAF und ARAF) sowie regulatorische Partner wie 14‑3‑3‑Proteine. Eingebaut sind außerdem eine verstärkende Rückkopplung (bei der aktives RAS seinen eigenen Aktivator SOS stärkt) und drei dämpfende Rückkopplungen (bei denen aktives ERK SOS, RAF und MEK abschwächt). Da jedes Protein auf viele Arten modifiziert und gebunden werden kann, würde ein traditionelles Modell in der Größe explodieren; der regelbasierte Ansatz hält das Modell handhabbar und repräsentiert dennoch mehr als 600 verschiedene molekulare Spezies und Tausende von Reaktionen.
Erklärung gradueller und schalterartiger Signale
Experimente zeigen ein rätselhaftes Muster: Auf der Ebene von RAS und RAF steigt die Aktivität mit zunehmender Wachstumsfaktordosis allmählich an, während ERK am Ende der Kaskade oft nahezu alles‑oder‑nichts‑artig eingeschaltet wird. Das Modell erklärt dies damit, dass RAS bei niedrigen Dosen nur in kleinen Membranarealen aktiv wird. Mit steigender Dosis schaltet ein größerer Anteil der Membran in den aktiven Zustand. Lokal ist der RAS‑Schalter bistabil — er springt scharf von aus zu an — aber weil nur ein Bruchteil der Membran aktiv ist, erscheint die mittlere RAS‑ und RAF‑Aktivität über die ganze Zelle hinweg glatt. Weiter stromabwärts wirkt die zweistufige Aktivierung von MEK und ERK wie ein starker Verstärker, sodass schon mäßige Aktivität stromauf nahezu vollständige ERK‑Aktivierung hervorruft und so eine scharfe, schalterartige Antwort erzeugt. Negative Rückkopplung von ERK auf SOS verwandelt anhaltende Stimulation in rhythmische ERK‑Pulse, deren Perioden von der Stärke des Wachstumsfaktors und der Rückkopplungsintensität abhängen.
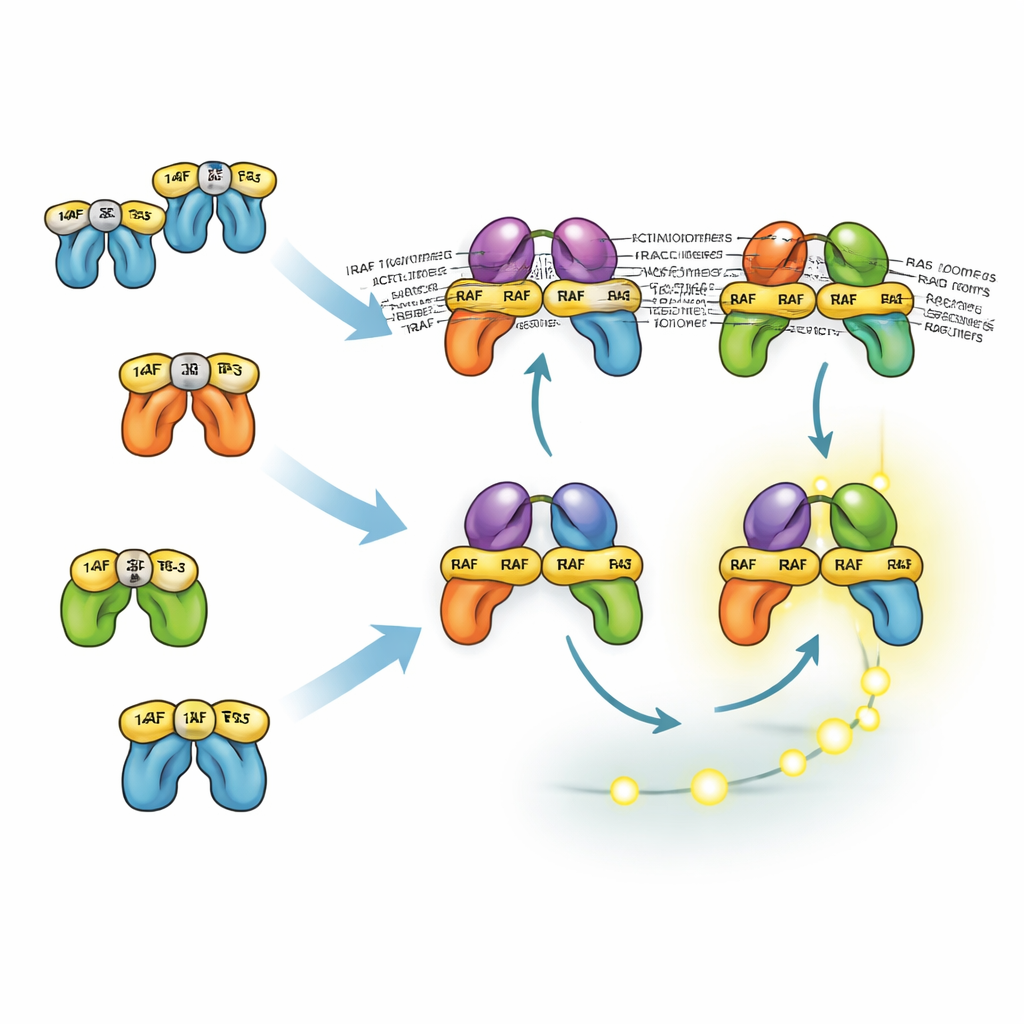
Wie sich ähnlich aussehende Proteine Aufgaben teilen
Die drei RAF‑Isoformen verhalten sich unterschiedlich, weil sie unterschiedlich mit 14‑3‑3‑Proteinen interagieren. Diese können RAF‑Moleküle sowohl in eine inaktive Konformation sperren als auch aktive RAF‑Paare stabilisieren. BRAF verfügt über seine wichtigste 14‑3‑3‑Andockstelle am Schwanzende, sodass es mit 14‑3‑3 assoziiert bleiben kann und gleichzeitig RAS binden und Dimere mit CRAF oder ARAF bilden kann. Diese gemischten Dimere sind besonders stabil und effizient bei der Aktivierung von MEK. Im Gegensatz dazu stützen sich CRAF und ARAF stärker auf Kopf‑seitiges Binden an 14‑3‑3, was ihre Rekrutierung zu RAS blockiert. Folglich sind Dimere ohne BRAF weniger stabil und in der Regel weniger zahlreich. Das Modell zeigt jedoch, dass Zellen auch ohne BRAF starke ERK‑Signale erzeugen können, weil upstream positive Rückkopplung und downstream Verstärkung dies kompensieren. Das erklärt mit, warum Medikamente, die nur BRAF angreifen, oft nur eine partielle Unterdrückung von ERK bewirken und deshalb mit MEK‑ oder ERK‑Inhibitoren kombiniert werden müssen.
Balance zwischen Bewegung, Überleben und Tod
Das Modell verfolgt auch RAF‑Funktionen, die über das einfache Einschalten von ERK hinausgehen. Wenn Dimere unter ERK‑getriebener negativer Rückkopplung auseinanderfallen, können offene Formen von CRAF Partner binden, die Zelltätigkeit und Überleben steuern, wie die Kinase ROKα oder das pro‑Tod‑Protein MST2. Mit wechselnden Wachstumsfaktorspiegeln und 14‑3‑3‑Mengen verschiebt sich das Gleichgewicht zwischen BRAF‑reichen Dimeren, die stark ERK antreiben, CRAF‑ und ARAF‑basierten Komplexen, die die Beweglichkeit modulieren, und Pools, die MST2 freisetzen und Zelltod fördern. Weil diese Verschiebungen glatt auf Stimulusstärke reagieren, während ERK‑Ausgang nahezu alles‑oder‑nichts sein kann, kann derselbe Signalweg subtile Verhaltensaspekte feinjustieren und gleichzeitig entschiedene Schicksalsentscheidungen treffen.
Was das für das Verständnis von Zellen bedeutet
Indem isoformspezifische Interaktionen, lokales Membranschalten und verschachtelte Rückkopplungsschleifen zusammengeführt werden, zeigt das Modell, wie ein molekularer Signalweg sowohl als Dimmer als auch als digitaler Schalter fungieren kann. Unterschiede in den Mengen von BRAF, CRAF, ARAF, MEK1, MEK2 und 14‑3‑3, wie sie in verschiedenen Geweben und Tumoren beobachtet werden, führen naturgemäß zu unterschiedlichen dynamischen Mustern der ERK‑Signalübertragung, von Pulsen bis zu andauernden Plateaus. Das legt nahe, dass die zelltypspezifische Verdrahtung gleicher Kernkomponenten den MAPK/ERK‑Weg für vielfältige physiologische Rollen umnutzen kann und dass wirksame Therapien nicht nur einzelne Ziele, sondern den gesamten regulatorischen Kontext, in dem diese molekularen Schalter arbeiten, berücksichtigen müssen.
Zitation: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Schlüsselwörter: MAPK ERK Signalübertragung, RAF‑Isoformen, 14‑3‑3 Regulation, computationaler Signalweg‑Modell, Zellschicksalsdynamik