Clear Sky Science · ja
MAPK/ERK 系の制御に関する計算的ルールベースモデル
なぜ小さな細胞スイッチが重要なのか
私たちの細胞は常に、成長するか、分裂するか、移動するか、自己破壊するかを瞬時に決めなければなりません。その中心的な判断装置のひとつが MAPK/ERK 経路と呼ばれるタンパク質の連鎖です。がんで最も頻繁に攪乱されるシステムの一つでもあります。教科書ではこの経路を単純なリレーのように描くことが多いですが、実際には多くの相互作用が張り巡らされた密なネットワークです。本研究はそのネットワークの詳細なコンピュータモデルを構築し、実用的な問いに答えようとします:どうすれば同じ経路が緩やかな段階的応答と鋭いオン/オフの決定を同時に生み出せるのか、そして密接に関連したタンパク質群はどのように協調または競合して細胞運命を制御するのか?
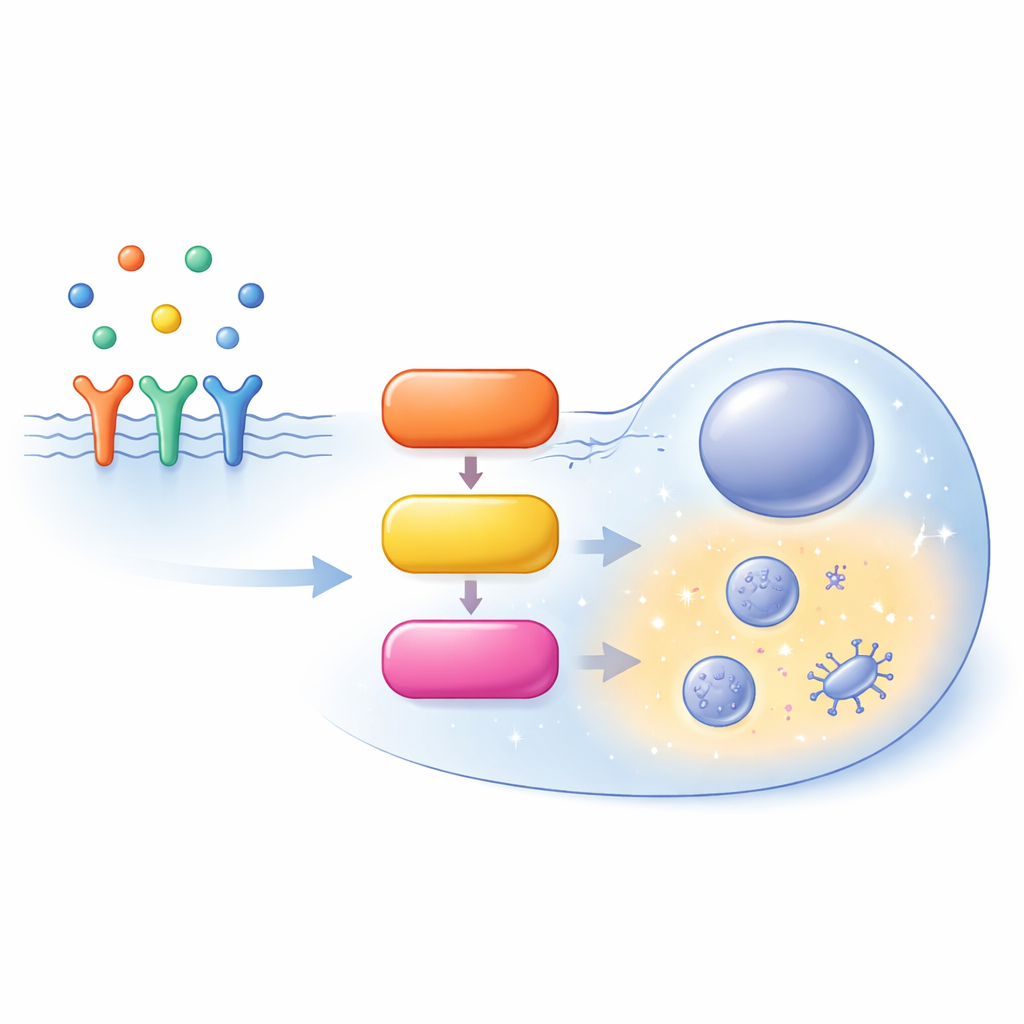
細胞内の忙しいハイウェイ
MAPK/ERK 経路は細胞表面で始まります。成長因子が受容体に結合すると SOS と呼ばれる補助タンパク質が動員され、SOS は小さな膜結合スイッチである RAS を活性化します。活性化された RAS は RAF として知られる酵素群を呼び寄せ、これが MEK を活性化し、さらに ERK を活性化します。活性化された ERK は細胞内の数百の標的を制御し、細胞の増殖、分化、移動、あるいはプログラム死の選択を形作ります。この経路は単純な一直線ではなく、フィードバックループ、枝分かれ、同じタンパク質の並行バリアント(アイソフォーム)に満ちており、その挙動は文脈依存になります。
単純なカスケードからルールベースのネットワークへ
この複雑さを捉えるために、著者らはルールベースモデリングという手法を用いています。これは可能な分子状態を一つずつ列挙するのではなく、相互作用のパターンを符号化する方法です。モデルには MEK の二つのバージョン(MEK1 と MEK2)と RAF の三つのバージョン(BRAF、CRAF、ARAF)、さらに 14-3-3 タンパク質のような調節パートナーが含まれます。また、強化型フィードバック(活性化された RAS が自らの活性化因子 SOS を強める)と三つの抑制フィードバック(活性化 ERK が SOS、RAF、MEK を抑える)を組み込んでいます。各タンパク質が多数の修飾や結合状態を取り得るため、従来型のモデルでは爆発的に状態数が増えますが、ルールベースのアプローチは数百の異なる分子種と数千の反応を表現しつつ、扱いやすさを保ちます。
段階的な信号とスイッチ様の信号を説明する
実験では興味深いパターンが観察されています:RAS と RAF のレベルでは成長因子の量に応じて活動が段階的に上がる一方で、カスケードの下流では ERK がほぼオンかオフかのように急激に立ち上がることが多いのです。モデルはこれを、低用量では RAS が細胞膜の小さなパッチだけでオンになると提案して説明します。用量が増すにつれて、活性化する膜領域が増えます。局所的には RAS のスイッチは二安定性を示し、オフからオンへ急激に移りますが、膜全体のうち活性領域が一部しかないため、細胞全体の平均的な RAS や RAF 活性は滑らかに見えます。下流では MEK と ERK の二段階の活性化が強力な増幅器として働き、上流のわずかな活動でもほぼ完全な ERK 活性化を生み出して鋭くスイッチのような応答を作ります。さらに ERK から SOS への負のフィードバックは、定常的な刺激を ERK 活性のリズミカルなパルスに変換し、その周期は成長因子の強さやフィードバックの強度に依存します。
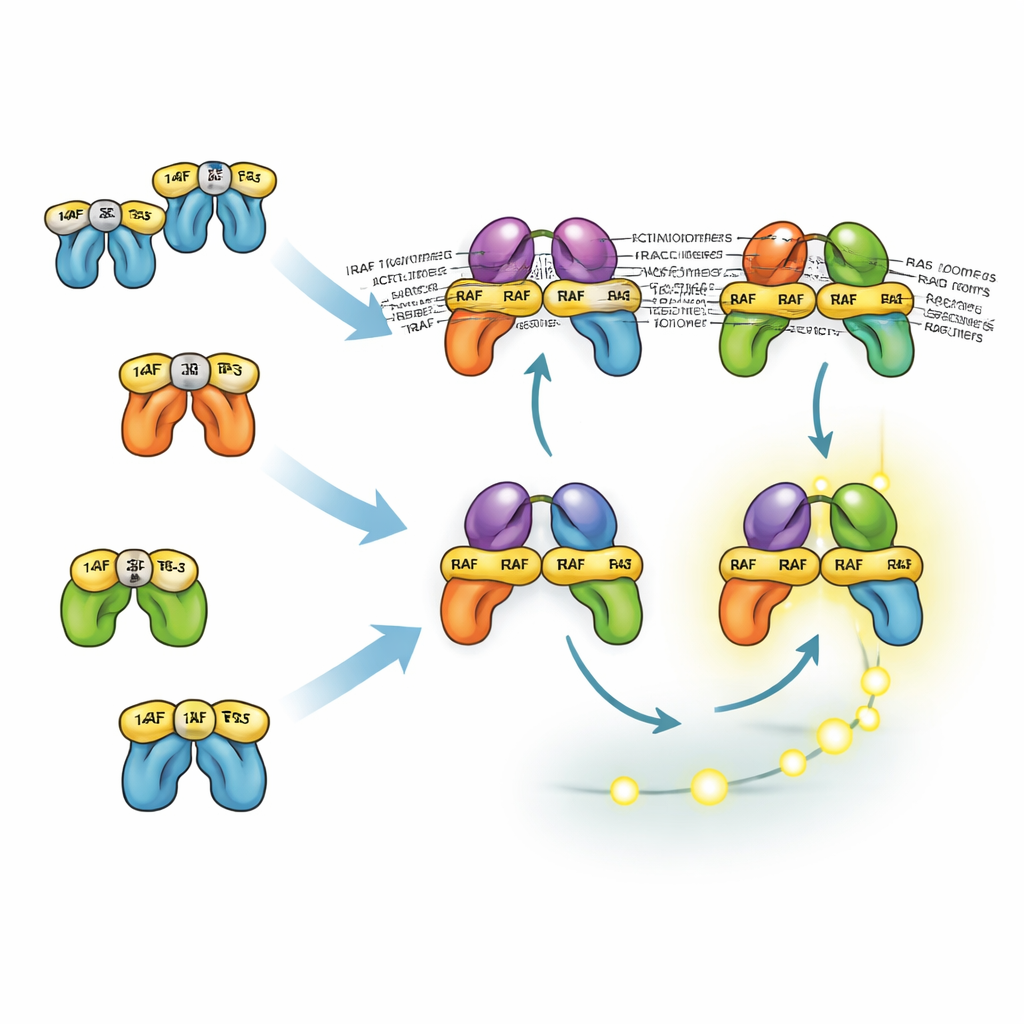
似たタンパク質が役割を共有し分担する仕組み
三つの RAF アイソフォームが異なる振る舞いを示すのは、14-3-3 タンパク質との相互作用の仕方が異なるためです。14-3-3 は RAF 分子を不活性形状でロックすることも、活性化した RAF の対を安定化することもできます。BRAF の主な 14-3-3 結合部位は尾部にあり、BRAF は 14-3-3 と結合したままでも RAS に結合し、CRAF や ARAF と二量体を形成できます。これらの混合二量体は特に安定かつ MEK を効率的に活性化します。対照的に CRAF と ARAF は頭部側での 14-3-3 結合に依存する傾向があり、これが RAS への動員を阻害します。その結果、BRAF を含まない二量体は安定性が低く、通常は数が少ないのです。それでもモデルは、BRAF がなくても上流の正のフィードバックと下流の増幅が補償するため、細胞は強い ERK 信号を生成できることを示します。これが単独の BRAF を標的にした薬剤が ERK を部分的にしか抑えられず、MEK や ERK 阻害剤との併用が必要になる理由の一端を説明します。
運動、生存、死のバランス
モデルは ERK をオンにする以外の RAF の役割も追跡します。ERK 駆動の負のフィードバックで二量体が解離すると、開いた形の CRAF は ROKα のような運動や生存を制御するパートナーや、細胞死を促す MST2 のようなタンパク質と結合できます。成長因子の量や 14-3-3 の存在量が変わると、ERK を強く駆動する BRAF に富む二量体、運動性を調節する CRAF/ARAF を基盤とする複合体、そして MST2 を解放して細胞死を促すプールとの間でバランスが変化します。これらのバランスは刺激強度に滑らかに応答する一方で、ERK の出力はほぼ全か無かになり得るため、同じ経路で微妙な行動の調整と決定的な運命の選択を同時に行うことができます。
細胞理解への示唆
アイソフォーム特異的な相互作用、局所的な膜スイッチング、入れ子状のフィードバックループを織り合わせることで、本モデルは一つの分子経路がディマー(明るさを調整する)としてもデジタルスイッチとしても働ける仕組みを示します。組織や腫瘍で観察される BRAF、CRAF、ARAF、MEK1、MEK2、14-3-3 の量の変動は、パルスから持続的なプラトーまで多様な ERK シグナルの動的パターンを自然に生み出します。これは同じコア成分の細胞種特異的な配線が MAPK/ERK 経路を多様な生理学的役割に再利用できること、そして有効な治療法は単一標的だけでなくこれらの分子スイッチが作用する全体の制御文脈を考慮する必要があることを示唆しています。
引用: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
キーワード: MAPK ERK シグナル伝達, RAF アイソフォーム, 14-3-3 による調節, 計算経路モデル, 細胞運命のダイナミクス