Clear Sky Science · tr
MAPK/ERK sistem düzenlemesinin hesaplamalı kural tabanlı modeli
Neden küçük hücresel anahtarlar önemlidir
Her saniye hücrelerimiz büyüyüp çoğalmak, hareket etmek ya da kendini yok etmek arasında karar vermek zorundadır. Merkezi bir karar verici, MAPK/ERK yolu adı verilen bir protein zinciridir. Bu yol kanserde en sık bozulan sistemlerden biridir. Ders kitapları genellikle bu yolu basit bir iletim hattı gibi gösterse de gerçekte birbirleriyle yoğun şekilde etkileşen parçaların sıkı bir ağıdır. Bu çalışma, bu ağı ayrıntılı bir bilgisayar modeliyle kurarak pratik bir soru soruyor: tek bir yol aynı anda nasıl hem kademeli, ılımlı yanıtlar hem de keskin, ya hep ya hiç kararlar üretebilir; çok benzer proteinler hücre kaderini kontrol etmek için nasıl iş birliği yapar veya rekabet eder?
Hücresel içindeki yoğun bir otoyol
MAPK/ERK yolu hücre yüzeyinde başlar; büyüme faktörleri reseptörlere bağlanır ve SOS adlı bir yardımcı proteini çağırır. SOS, hücre zarının iç yüzüne bağlı küçük bir moleküler anahtar olan RAS’ı etkinleştirir. Aktif RAS ardından RAF ailesinden enzimleri devreye çağırır; bunlar MEK’i, MEK de ERK’i aktive eder. Aktif ERK, hücre boyunca yüzlerce hedefi düzenleyerek hücrenin çoğalmasını, farklılaşmasını, göç etmesini veya programlı ölümü seçmesini şekillendirir. Bu rota basit bir düz çizgi olmaktan ziyade geri besleme döngüleri, dallanma ve aynı proteinlerin paralel varyantları (izoformlar) ile doludur; bu yüzden davranışı bağlama çok bağlıdır.
Basit kaskaddan kural tabanlı ağa
Bu karmaşıklığı yakalamak için yazarlar kural tabanlı modellemeyi kullanır; bu yöntem her olası moleküler durumu tek tek listelemek yerine etkileşim kalıplarını kodlar. Modellerinde iki MEK versiyonu (MEK1 ve MEK2) ve üç RAF versiyonu (BRAF, CRAF ve ARAF) ile 14-3-3 gibi düzenleyici ortakları içerir. Ayrıca bir güçlendirici geri besleme (aktif RAS’ın kendi aktivatörü SOS’u artırması) ve üç frenleyici geri besleme (aktif ERK’in SOS, RAF ve MEK’i bastırması) kurar. Her protein birçok şekilde modifiye edilebildiği ve bağlanabildiği için geleneksel bir model hızla devasa hale gelir; kural tabanlı yaklaşım ise hâlâ 600’den fazla ayırt edilebilir moleküler tür ve binlerce reaksiyonu temsil ederken modeli yönetilebilir tutar.
Kademeli ve anahtar benzeri sinyalleri açıklamak
Deneyler şaşırtıcı bir desen göstermiştir: RAS ve RAF düzeyinde aktivite büyüme faktörü dozu arttıkça kademeli biçimde yükselir, ancak kaskadın sonunda ERK genellikle neredeyse hep ya hiç şeklinde açılır. Model bunu şu şekilde açıklar: düşük dozlarda RAS yalnızca hücre zarının küçük yamalarında etkinleşir. Doz arttıkça zarın daha büyük bir kısmı aktif duruma geçer. Yerel olarak RAS anahtarı çift kararlı olabilir—kapalıdan açık duruma keskin atlar—ama yalnızca zarfın bir bölümü aktif olduğundan hücre genelindeki ortalama RAS ve RAF aktivitesi düzgün görünür. Aşağı akımda, MEK ve ERK’in çift adımlı aktivasyonu güçlü bir yükseltici gibi davranır; böylece ılımlı yukarı akım aktivitesi bile neredeyse tam ERK aktivasyonu üreterek keskin, anahtar benzeri bir yanıt verir. ERK’den SOS’a giden negatif geri besleme ise sürekli uyarımı ERK aktivitesinin ritmik darbelerine çevirir; bu darbelerin periyodu büyüme faktörü gücüne ve geri besleme yoğunluğuna bağlıdır.
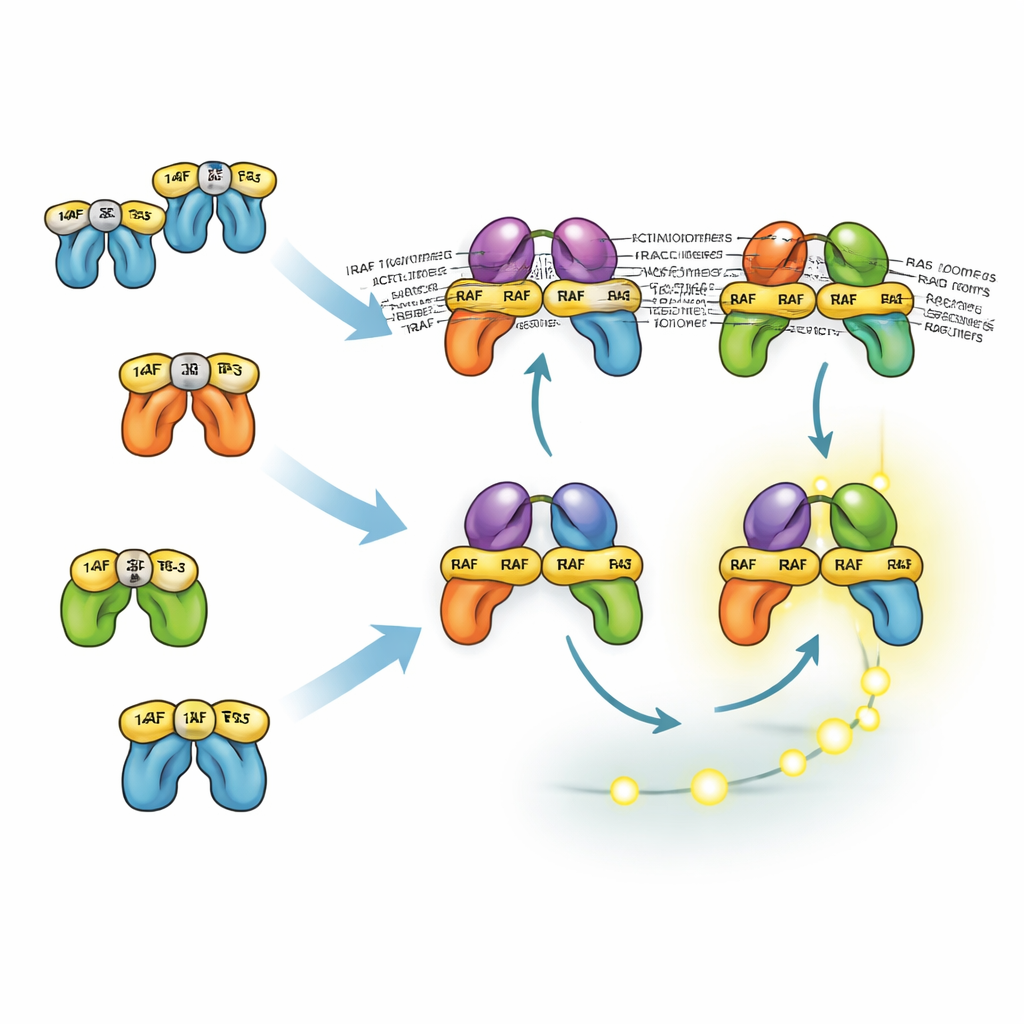
Benzer görünen proteinler görevleri nasıl paylaşır ve böler
Üç RAF izoformu, 14-3-3 proteinleriyle nasıl etkileştiklerine bağlı olarak farklı davranır; 14-3-3 hem RAF moleküllerini inaktif bir biçimde kilitleyebilir hem de aktif RAF çiftlerini stabilize edebilir. BRAF’ın 14-3-3 için ana bağlanma noktası kuyruğundadır; bu, BRAF’ın 14-3-3’e bağlı kalırken RAS’a bağlanmasını ve CRAF ya da ARAF ile dimer oluşturmasını sağlar. Bu karışık dimerler özellikle stabil ve MEK’i aktive etmede etkilidir. Buna karşılık CRAF ve ARAF daha çok baş uç bağlanmasına dayanır; bu, onların RAS’a çekilmesini engeller. Sonuç olarak BRAF içermeyen dimerler daha az stabil ve genellikle daha az bol olur. Yine de model, BRAF olmasa bile hücrelerin güçlü ERK sinyalleri üretebildiğini gösterir; çünkü yukarı akım pozitif geri besleme ve aşağı akım yükseltimi bunu telafi eder. Bu, yalnızca BRAF’ı hedefleyen ilaçların sıklıkla ERK’i kısmen baskıladığını ve MEK veya ERK inhibitörleriyle birlikte kullanılmaları gerektiğini açıklamaya yardımcı olur.
Hareket, hayatta kalma ve ölümü dengelemek
Model ayrıca RAF’ın ERK’i açmanın ötesindeki rollerini izler. Dimerler ERK kaynaklı negatif geri besleme ile ayrıldığında, açık biçimdeki CRAF hareket ve hayatta kalmayı kontrol eden ortaklara bağlanabilir; örneğin kinaz ROKα veya pro-ölüm proteini MST2 gibi. Büyüme faktörü seviyeleri ve 14-3-3 bolluğu değiştikçe denge, ERK’i güçlü şekilde tetikleyen BRAF ağırlıklı dimerler, hareketi düzenleyen CRAF- ve ARAF-tabanlı kompleksler ile MST2’yi serbest bırakarak hücre ölümünü teşvik eden havuzlar arasında kayar. Bu dengeler uyarı gücüne düzgün yanıt verirken ERK’in çıktısı neredeyse hep ya hiç olabildiğinden aynı yol davranışın ince ayarlarını düzenleyebilir ve yine de kararlı kader seçimleri yapabilir.
Hücreleri anlamak için ne anlama geliyor
İzoform-spesifik etkileşimleri, yerel zar anahtarlamayı ve iç içe geçmiş geri besleme döngülerini birleştirerek model, tek bir moleküler yolun hem bir dimmer hem de dijital bir anahtar gibi davranabildiğini gösterir. Dokular ve tümörler arasında gözlemlenen BRAF, CRAF, ARAF, MEK1, MEK2 ve 14-3-3 miktarlarındaki farklılıklar, ERK sinyal iletiminin darbelerden sürekli plato davranışına kadar çeşitli dinamik desenlere doğal olarak yol açar. Bu, aynı çekirdek bileşenlerin hücre tipi–spesifik kablolamasıyla MAPK/ERK yolunun farklı fizyolojik rollere yeniden kullanılabileceğini ve etkili terapilerin yalnızca tek hedefleri değil, bu moleküler anahtarların işlediği tam düzenleyici bağlamı dikkate alması gerektiğini öne sürer.
Atıf: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Anahtar kelimeler: MAPK ERK sinyal iletimi, RAF izoformları, 14-3-3 düzenlemesi, hesaplamalı yol modeli, hücre kaderi dinamikleri