Clear Sky Science · pt
Um modelo computacional baseado em regras da regulação do sistema MAPK/ERK
Por que interruptores celulares minúsculos importam
Cada segundo, nossas células precisam decidir se crescem, se dividem, se movem ou se autodestruem. Um tomador de decisão central é uma cadeia de proteínas chamada via MAPK/ERK. É também um dos sistemas mais frequentemente perturbados no câncer. Embora livros didáticos frequentemente mostrem essa via como um retransmissor simples, na prática ela é uma teia densa de componentes interagentes. Este estudo constrói um modelo de computador detalhado dessa teia para perguntar uma questão prática: como uma única via pode produzir simultaneamente respostas suaves e graduais e decisões bruscas de tudo-ou-nada, e como proteínas intimamente relacionadas cooperam ou competem para controlar o destino celular?
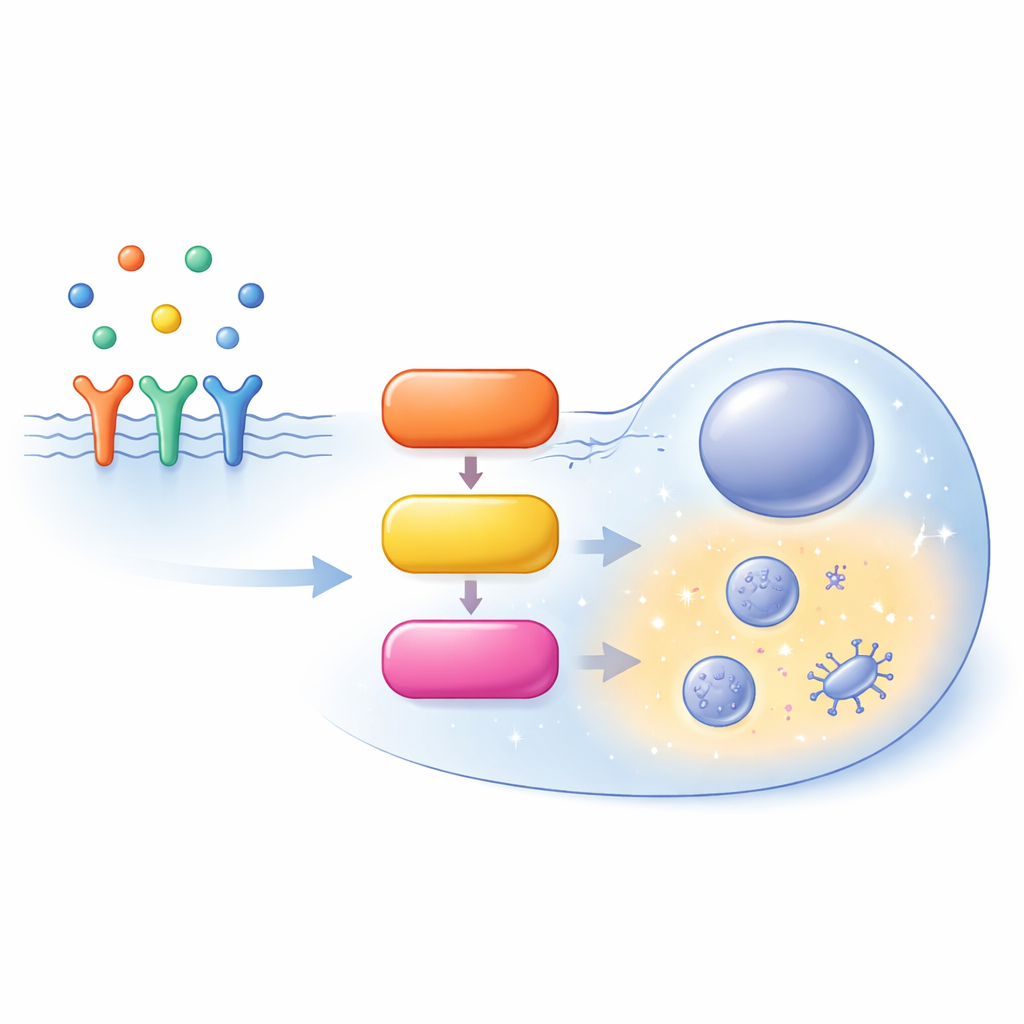
Uma rodovia movimentada dentro da célula
A via MAPK/ERK começa na superfície celular, onde fatores de crescimento se ligam a receptores e recrutam uma proteína auxiliar chamada SOS. SOS ativa RAS, um pequeno interruptor molecular preso à face interna da membrana celular. RAS ativo então recruta uma família de enzimas conhecidas como RAF, que ativam MEK, que por sua vez ativa ERK. ERK ativado regula centenas de alvos por toda a célula, moldando se a célula prolifera, se diferencia, migra ou entra em morte programada. Em vez de ser uma linha reta simples, esse percurso é repleto de laços de feedback, ramificações e variantes paralelas das mesmas proteínas (isoformas), tornando seu comportamento altamente dependente do contexto.
De cascata simples a rede baseada em regras
Para capturar essa complexidade, os autores usam modelagem baseada em regras, um método que codifica padrões de interação em vez de listar cada possível estado molecular um por um. O modelo inclui duas versões de MEK (MEK1 e MEK2) e três versões de RAF (BRAF, CRAF e ARAF), bem como parceiros regulatórios como as proteínas 14-3-3. Também incorpora um feedback reforçador (onde RAS ativo aumenta seu próprio ativador SOS) e três feedbacks inibitórios (onde ERK ativo reduz a atividade de SOS, RAF e MEK). Como cada proteína pode ser modificada e ligada de muitas maneiras diferentes, um modelo tradicional cresceria exponencialmente; a abordagem baseada em regras mantém o modelo manejável enquanto ainda representa mais de 600 espécies moleculares distintas e milhares de reações.
Explicando sinais graduais e em forma de chave
Experimentos mostraram um padrão intrigante: no nível de RAS e RAF, a atividade aumenta gradualmente à medida que a dose do fator de crescimento cresce, mas no final da cascata ERK frequentemente liga-se de forma quase tudo-ou-nada. O modelo explica isso propondo que, em baixas doses, RAS ativa-se apenas em pequenos trechos da membrana celular. À medida que a dose aumenta, mais áreas da membrana passam ao estado ativo. Localmente, o interruptor RAS é bistável — ele salta de forma abrupta do desligado para o ligado — mas, como apenas uma fração da membrana está ativa, a atividade média de RAS e RAF em toda a célula parece suave. A jusante, a ativação em dois passos de MEK e ERK atua como um amplificador poderoso, de modo que mesmo uma atividade moderada a montante produz quase ativação completa de ERK, gerando uma resposta aguda semelhante a um interruptor. Feedback negativo de ERK para SOS então converte estimulação contínua em pulsos rítmicos de atividade de ERK, cujo período depende da intensidade do fator de crescimento e da força do feedback.
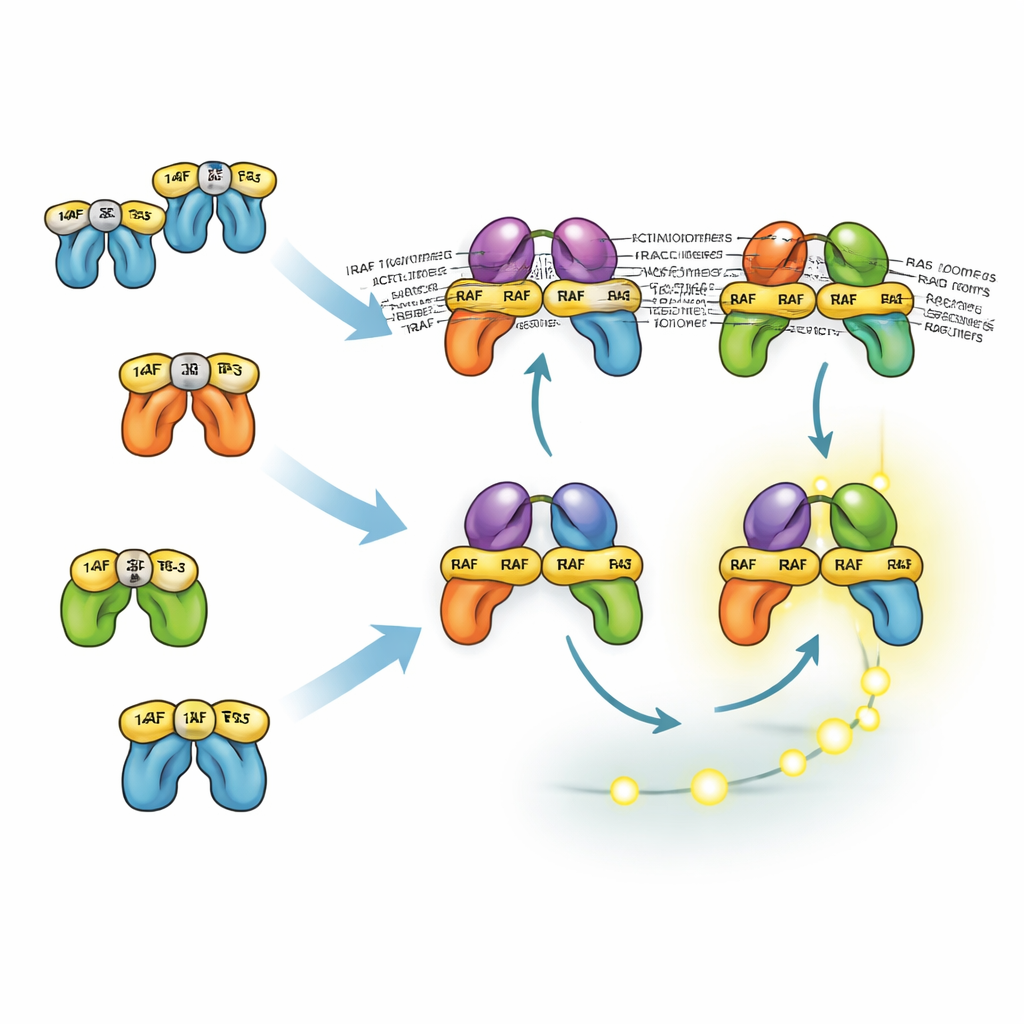
Como proteínas semelhantes compartilham e dividem tarefas
As três isoformas de RAF se comportam de maneiras diferentes por causa de como interagem com as proteínas 14-3-3, que podem tanto bloquear moléculas RAF em uma conformação inativa quanto estabilizar pares ativos de RAF. O principal sítio de ancoragem de BRAF para 14-3-3 fica em sua cauda, permitindo que permaneça associado à 14-3-3 enquanto ainda se liga a RAS e forma dímeros com CRAF ou ARAF. Esses dímeros mistos são especialmente estáveis e eficientes em ativar MEK. Em contraste, CRAF e ARAF dependem mais da ligação pela extremidade da cabeça à 14-3-3, o que bloqueia seu recrutamento por RAS. Como resultado, dímeros sem BRAF são menos estáveis e geralmente menos abundantes. Ainda assim, o modelo mostra que, mesmo sem BRAF, as células podem gerar sinais ERK fortes porque o feedback positivo a montante e a amplificação a jusante compensam. Isso ajuda a explicar por que fármacos que visam apenas BRAF muitas vezes suprimem ERK apenas parcialmente e precisam ser combinados com inibidores de MEK ou ERK.
Equilibrando movimento, sobrevivência e morte
O modelo também acompanha papéis de RAF que vão além de simplesmente ligar ERK. Quando dímeros se desfazem sob feedback negativo ativado por ERK, formas abertas de CRAF podem se ligar a parceiros que controlam movimento e sobrevivência celular, como a quinase ROKα ou a proteína pró-morte MST2. Conforme os níveis de fator de crescimento e a abundância de 14-3-3 mudam, o equilíbrio desloca-se entre dímeros ricos em BRAF que impulsionam fortemente ERK, complexos baseados em CRAF e ARAF que modulam a motilidade, e reservatórios que liberam MST2 para promover a morte celular. Porque esses equilíbrios respondem de forma suave à força do estímulo enquanto a saída de ERK pode ser quase tudo-ou-nada, a mesma via pode ajustar aspectos sutis do comportamento e ainda tomar decisões decisivas sobre o destino celular.
O que isso significa para entender as células
Ao entrelaçar interações específicas de isoformas, comutação local na membrana e laços de feedback aninhados, o modelo mostra como uma via molecular pode funcionar tanto como um dimmer quanto como um interruptor digital. Variações nas quantidades de BRAF, CRAF, ARAF, MEK1, MEK2 e 14-3-3, como observado em diferentes tecidos e tumores, levam naturalmente a padrões dinâmicos distintos de sinalização ERK, de pulsos a patamares sustentados. Isso sugere que a fiação específica por tipo celular dos mesmos componentes centrais pode reutilizar a via MAPK/ERK para papéis fisiológicos diversos, e que terapias eficazes precisarão considerar não apenas alvos isolados, mas todo o contexto regulatório no qual esses interruptores moleculares operam.
Citação: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Palavras-chave: sinalização MAPK ERK, isoformas RAF, regulação 14-3-3, modelo computacional de vias, dinâmica do destino celular