Clear Sky Science · zh
通过邻近标记进行膜编辑揭示脂质稳态的调节因子
细胞如何维持脂质外衣的平衡
你体内的每个细胞都被一层薄薄的脂质外衣包裹,称为膜。这些膜不仅仅是简单的屏障:它们的脂质组成精确地影响细胞如何生长、通信并应对压力。其中一种尤为重要的脂质,磷酸甘油酯(PA),像分子警报钟一样发挥作用。PA 的瞬时升高可以开启或关闭关键的信号通路,因此细胞必须以极快且精确的方式调节其水平。这项研究揭示了细胞如何感知突增的 PA 并招募特定蛋白将这一强效脂质重新拉回控制。
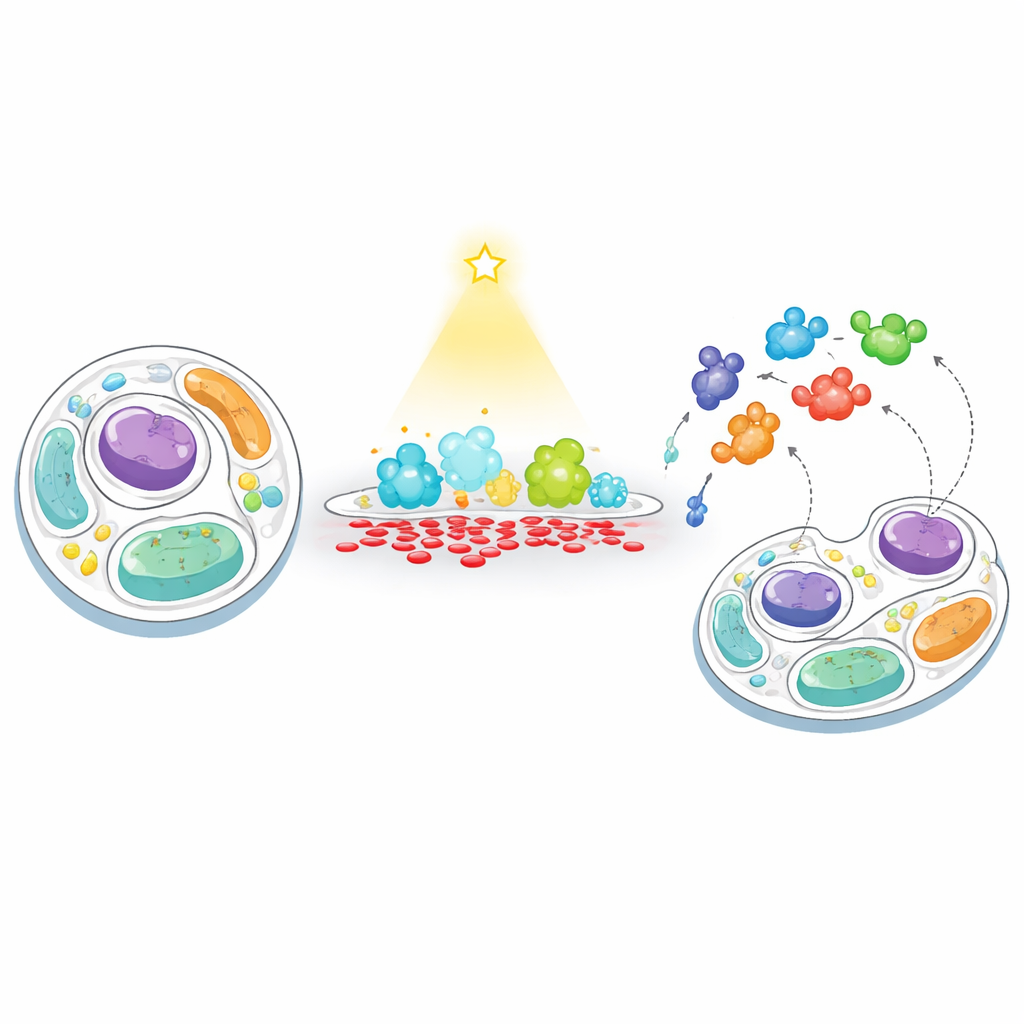
在细胞膜上“喂养”和“垂钓”的新方法
研究者们开发了一种两步策略,称为“喂养—垂钓”,用于追踪当膜的 PA 水平被人为扰动时细胞的反应。首先,他们利用一种受光控制的酶“喂养”目标膜,该酶是工程化的磷脂酶 D 版本,可通过蓝光随意开启。通过将这类酶定向到细胞的外表面或溶酶体(细胞的回收中心),他们可以触发短暂且局部的 PA 产生。接着,他们通过将一种生物素标记酶(TurboID)连接到同一膜上来“垂钓”附近的蛋白;任何靠近的蛋白都会被标记,随后通过高通量质谱捕获并鉴定,从而揭示哪些蛋白被 PA 富集区域吸引或排斥。
PA 激增时谁会出现?
将该方法应用于人类细胞后,团队鉴定出质膜和溶酶体附近的数千种蛋白,并找出在 PA 水平上升时丰度发生变化的那些。许多最强的响应者已知参与处理 PA 或相关脂质,这验证了该方法的有效性。被称为 lipin 的酶将 PA 分解为另一种信号脂质二酰基甘油(DAG),在加载 PA 的膜上富集;而产生 PA 的 DAG 合成酶则出现得较少,暗示存在内在的反馈机制。最著名的 PA 转运蛋白 Nir2 也被招募到富含 PA 的质膜和溶酶体,强调其在器官间搬运 PA 的核心角色。分析还显示与线粒体和胆固醇处理相关的蛋白发生变化,表明 PA 的突增会影响细胞代谢的多个方面。
搬运并移除 PA 的隐形快递员
为了测试哪些被招募的蛋白实际上有助于清除过量 PA,科学家们聚焦于若干脂质转运蛋白——在膜之间搬运脂质的分子快递员。通过过表达这些快递员并追踪荧光 PA 传感器,他们发现 Nir2 和名为 SCP2 的蛋白显著减少了质膜和溶酶体处的 PA 积累。SCP2 先前以搬运胆固醇和脂肪酸而闻名,在纯化的脂质体试验中也表现出携带 PA 的活性,扩展了其功能描述。其他转运蛋白,包括 PDZD8 和 TEX2,未能直接降低 PA 水平,但似乎加强了内质网与溶酶体之间的物理接触,可能有助于将脂质引导至后续处理路径。相反,一种氧甾醇结合蛋白 ORP1L 出人意料地导致 PA 进一步升高,这种效应依赖于其结合胆固醇的位点,提示 PA 与胆固醇流动之间存在更复杂的相互影响。
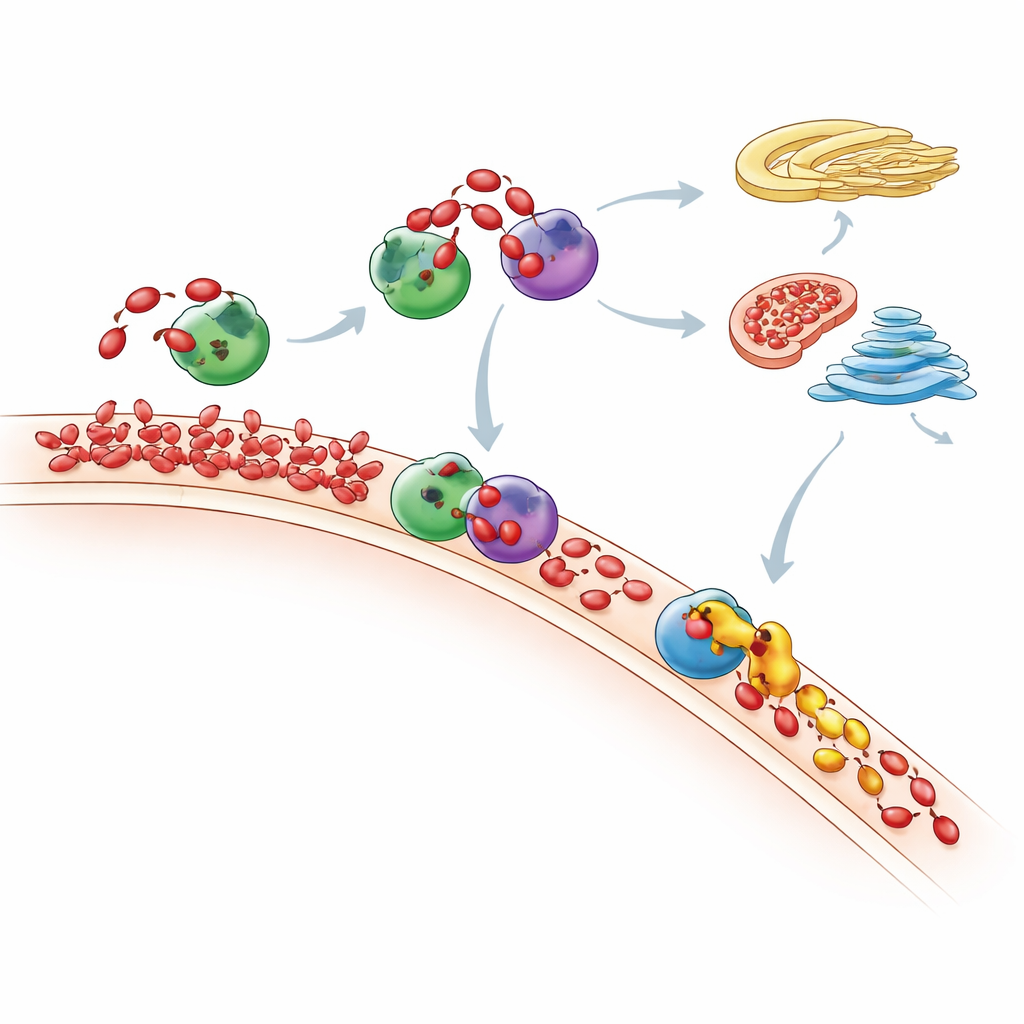
多余的 PA 最终去了哪里
通过灵敏的质谱测量全细胞脂质全景,研究人员追踪了在“喂养”后细胞整个磷脂组成如何变化。他们发现 PA 的激增是短暂的:随着时间推移,许多 PA 分子要么被转化为 DAG,随后通过 Kennedy 通路形成常见膜脂质,要么通过 CDP-DAG 路径转化为其他脂质。线粒体似乎发挥关键作用,利用名为 TAMM41 的酶将进入的 PA 转化为磷酸甘油(phosphatidylglycerol),这是线粒体膜的构件。当 Nir2 被耗竭时,新生成的 PA 不再留在产生地点,而是在高尔基区累积,表明破坏一个快递员会导致脂质交通在细胞内改道并改变如 mTOR 这样的重要信号通路。
这项工作对细胞健康为何重要
通过将精确的“膜编辑”与邻近标记结合,这项研究为发现细胞如何感知并纠正脂质组成失衡提供了强有力的蓝图。就 PA 而言,该工作绘制出一张酶和转运蛋白网络图,这些分子会迅速聚集到超载的膜上,将 PA 迁移到更安全的地点并将其转化为其他脂质,同时维持关键的信号回路。由于类似的脂质紊乱与癌症、代谢病和神经退行性疾病有关,喂养—垂钓方法可用于揭示在众多由膜脂质悄然塑造细胞行为的疾病中潜在的新药物靶点。
引用: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
关键词: 磷酸甘油酯, 脂质稳态, 膜蛋白质组学, 脂质转运蛋白, 光遗传膜编辑