Clear Sky Science · ja
近接標識による膜編集が脂質ホメオスタシスの調節因子を明らかにする
細胞はどのように脂肪の被膜を維持しているか
体のあらゆる細胞は膜と呼ばれる薄い脂質の被膜に包まれています。これらの膜は単なる障壁以上のもので、脂質の正確な組成が細胞の成長、情報伝達、ストレス応答を制御します。特に強力な脂質であるホスファチジン酸(PA)は分子レベルの警鐘のように働きます。PAの急増は主要なシグナル経路をオン・オフに切り替えるため、細胞はその量を非常に迅速かつ精密に上げ下げしなければなりません。本研究は、細胞が突然のPAの増加をどのように感知し、特定のタンパク質を動員してこの強力な脂質を制御下に戻すかを明らかにします。
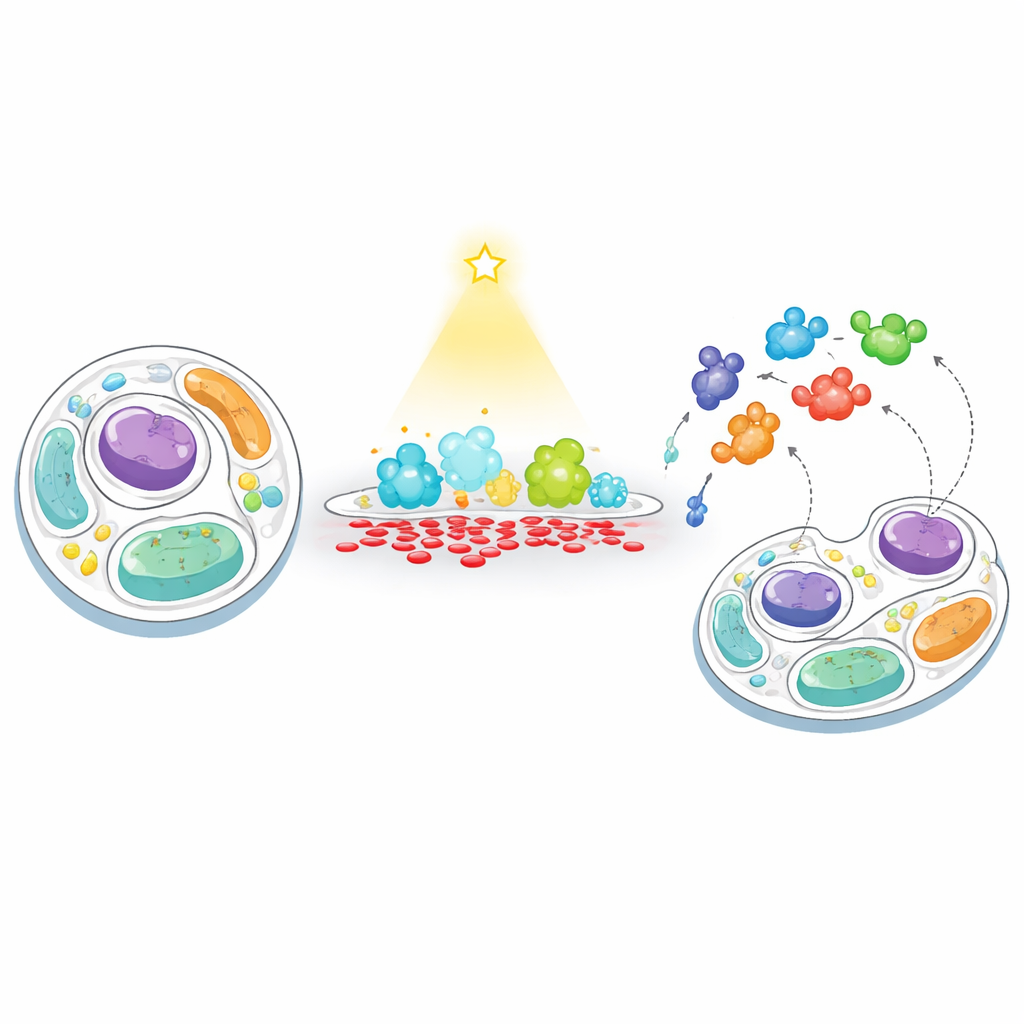
膜で「与え」「釣る」という新手法
研究者らは「feeding–fishing(与え–釣る)」と呼ぶ二段階の戦略を開発し、膜のPAレベルが人為的に乱された際の細胞応答を追跡しました。まず、青色光で駆動できる設計改変型ホスホリパーゼD(光でスイッチできる酵素)を用いて標的の膜にPAを「与え」ます。この酵素を細胞の外側膜(プラズマ膜)やリソソーム(細胞のリサイクルセンター)に誘導することで、局所的で短時間のPA生成を引き起こせます。次に、同じ膜にビオチン標識酵素(TurboID)を結びつけて近接するタンパク質を「釣り上げ」ます。近づいたタンパク質は標識され、高感度の質量分析で捕捉・同定されるため、PA豊富領域に惹き寄せられるタンパク質や反発するタンパク質が明らかになります。
PAが急増したとき誰が現れるか
この手法をヒト細胞に適用して、研究チームはプラズマ膜とリソソーム近傍で数千のタンパク質を同定し、PAレベル上昇時に量が変動するものを特定しました。強く反応するタンパク質の多くはPAや関連脂質を扱うことが既知であり、このアプローチの妥当性が示されました。PAを分解して別のシグナル脂質であるジアシルグリセロール(DAG)に変換するリンピン(lipin)という酵素はPA負荷膜に豊富に検出され、一方でPAを生成するDAG合成酵素は頻度が下がり、フィードバック機構が働いていることを示唆しました。最もよく知られたPA輸送タンパク質であるNir2もまた、PA豊富なプラズマ膜とリソソームの双方に移動し、オルガネラ間でPAを輸送する中心的役割を裏付けました。解析はさらにミトコンドリアやコレステロール処理に関連するタンパク質の変動も明らかにし、PAの急増が細胞代謝の多くの側面に波及することを示しています。
PAを移動・除去する隠れた運び屋たち
動員されたタンパク質のうち、実際に過剰なPAを除去する働きを持つものを検証するため、科学者たちはいくつかの脂質輸送タンパク質—膜間で脂質を運ぶ分子運び屋—に注目しました。これらを過剰発現させ、蛍光PAセンサーで追跡したところ、Nir2とSCP2というタンパク質がプラズマ膜およびリソソームでのPA蓄積を顕著に低下させました。SCP2はこれまでコレステロールや脂肪酸の輸送で知られていましたが、精製リポソームアッセイでもPA輸送活性を示し、その機能の幅が広がることが示されました。他の輸送タンパク質、PDZD8やTEX2などは直接PAを減らさなかったものの、小胞体とリソソームの物理的接触を強化して脂質を後続処理へ回す経路を整える役割を果たしているようでした。対照的に、オキシステロール結合タンパク質であるORP1Lは予期せずPAをさらに増加させ、その作用はコレステロール結合部位に依存していたため、PAとコレステロールの流れの間により複雑な相互作用があることを示唆しました。
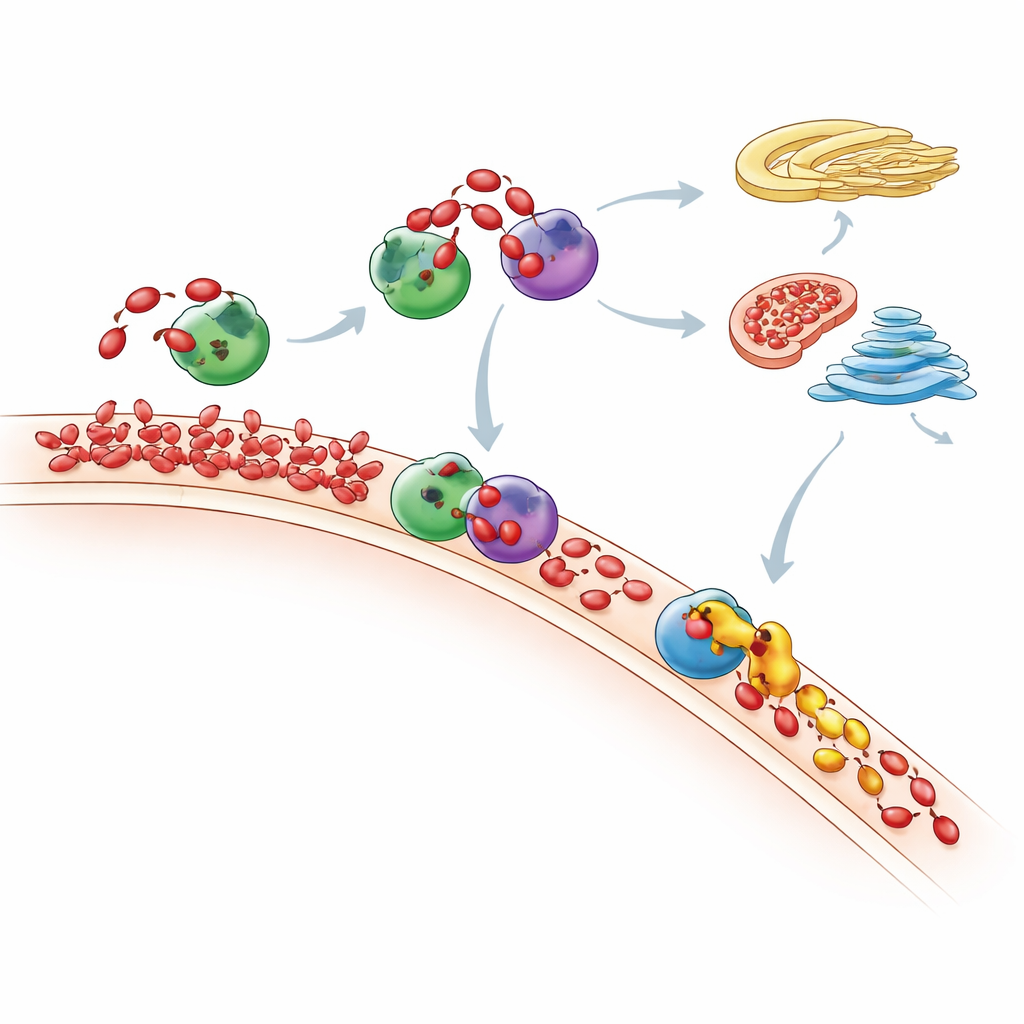
過剰なPAは最終的にどこへ行くか
感度の高い質量分析で全体の脂質プロファイルを測定し、研究者らはPA「与え」の後に細胞のリン脂質組成全体がどのように変化するかを追跡しました。PAの急増は短命であり、時間とともに多くのPA分子はDAGに変換され、その後ケネディ経路を経て一般的な膜脂質になったり、CDP-DAG経路を通じて他の脂質に変換されたりしました。ミトコンドリアは重要な役割を担っているようで、TAMM41という酵素を使って流入したPAをミトコンドリア膜の構成要素であるホスファチジルグリセロールへ変換するのに寄与していました。Nir2が枯渇すると、新たに生成されたPAは産生場所に留まらずゴルジ領域に蓄積し、単一の輸送係を失うと細胞内の脂質トラフィックが迂回してmTORのような主要な成長調節経路など重要なシグナル経路が変化することが示されました。
この研究が細胞の健康にとって重要な理由
精密な「膜編集」と近接標識を組み合わせることで、本研究は細胞が脂質組成の不均衡をどのように検出し是正するかを明らかにする強力な設計図を提供します。PAに関しては、過負荷になった膜に急行してPAを移動させ安全な場所へ運び変換する酵素と輸送タンパク質のネットワークが描き出され、主要なシグナル回路を維持する仕組みが示されました。類似の脂質異常はがん、代謝疾患、神経変性と関連するため、feeding–fishingアプローチは膜脂質が静かに細胞挙動を形作る多くの疾患領域で新たな薬物標的を明らかにするのに役立つ可能性があります。
引用: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
キーワード: ホスファチジン酸, 脂質ホメオスタシス, 膜プロテオミクス, 脂質輸送タンパク質, オプトジェネティック膜編集