Clear Sky Science · it
Modifica delle membrane con marcatura di prossimità rivela regolatori dell’omeostasi lipidica
Come le cellule mantengono in equilibrio il loro mantello grasso
Ogni cellula del tuo corpo è avvolta da un sottile mantello grasso chiamato membrana. Queste membrane sono più di semplici barriere: la loro precisa composizione lipidica contribuisce a regolamentare la crescita cellulare, la comunicazione e la risposta allo stress. Un lipide particolarmente influente, l’acido fosfatidico (PA), funziona come una sorta di campanello d’allarme molecolare. Raffiche di PA possono attivare o spegnere percorsi di segnalazione chiave, quindi le cellule devono aumentare e ridurre i suoi livelli in modo molto rapido e preciso. Questo studio mostra come le cellule percepiscono improvvisi aumenti di PA e reclutano proteine specifiche per riportare sotto controllo questo potente lipide.
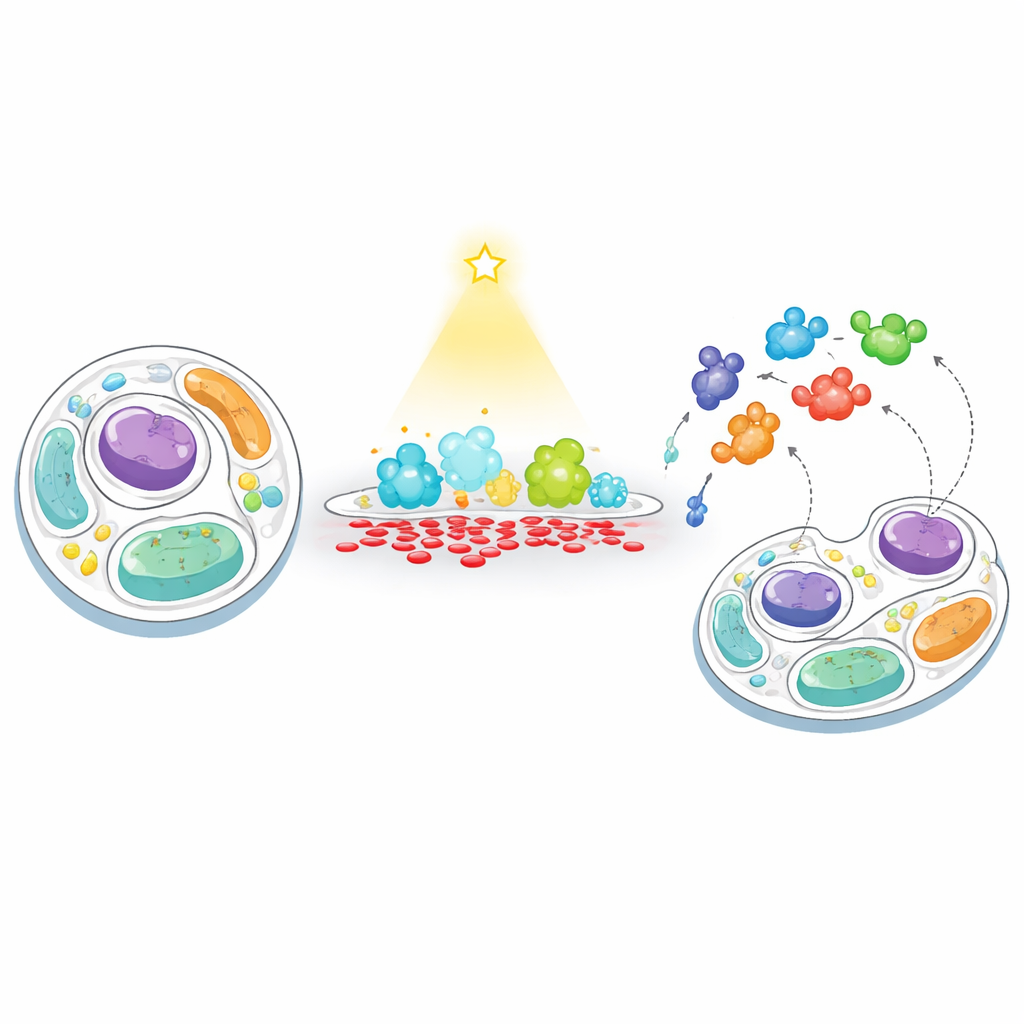
Un nuovo metodo per “nutrire” e “pescare” nelle membrane cellulari
I ricercatori hanno sviluppato una strategia in due fasi che chiamano “feeding–fishing” per tracciare come le cellule rispondono quando il livello di PA in una membrana viene artificialmente sbilanciato. Prima, “nutrono” una membrana scelta con PA usando un enzima controllato dalla luce, una versione ingegnerizzata della fosfolipasi D che può essere attivata a comando con luce blu. Mirando questo enzima alla superficie esterna della cellula o ai lisosomi (i centri di riciclo cellulare), possono produrre brevi raffiche localizzate di PA. Secondo, “pescano” le proteine vicine attaccando alla stessa membrana un enzima che aggiunge una biotina (TurboID). Qualsiasi proteina che si avvicina viene marcata e successivamente catturata e identificata con spettrometria di massa ad alta capacità, rivelando quali proteine vengono attirate verso le regioni ricche di PA o da esse respinte.
Chi arriva quando il PA aumenta improvvisamente?
Applicando questo metodo a cellule umane, il team ha identificato migliaia di proteine vicino alla membrana plasmatica e ai lisosomi, quindi ha evidenziato quelle la cui abbondanza cambiava quando i livelli di PA aumentavano. Molti dei rispondenti più forti erano già noti per elaborare PA o lipidi correlati, a convalida dell’approccio. Enzimi chiamati lipine, che degradano PA in un altro lipide di segnalazione, il diacilglicerolo (DAG), erano arricchiti sulle membrane cariche di PA, mentre un enzima che produce DAG mostrava una presenza ridotta, suggerendo un sistema di retroazione incorporato. La più nota proteina di trasferimento del PA, Nir2, si è spostata sia verso membrane plasmatiche ricche di PA sia verso i lisosomi, sottolineandone il ruolo centrale nello scambio di PA tra organelli. L’analisi ha inoltre rivelato cambiamenti in proteine legate ai mitocondri e alla gestione del colesterolo, suggerendo che le impennate di PA riverberano in molti aspetti del metabolismo cellulare.
Corrieri nascosti che spostano e rimuovono il PA
Per testare quali delle proteine reclutate aiutano effettivamente a eliminare l’eccesso di PA, gli scienziati si sono concentrati su diverse proteine di trasferimento lipidico — corrieri molecolari che spostano i grassi tra le membrane. Sovraprodurre questi corrieri e seguire un sensore fluorescente per il PA ha mostrato che Nir2 e una proteina chiamata SCP2 riducevano significativamente l’accumulo di PA nella membrana plasmatica e nei lisosomi. SCP2, già nota per trasferire colesterolo e acidi grassi, ha mostrato anche attività di trasporto del PA in un saggio con liposomi purificati, ampliandone la funzione. Altre proteine di trasferimento, tra cui PDZD8 e TEX2, non abbassavano direttamente i livelli di PA ma sembravano rafforzare i contatti fisici tra reticolo endoplasmatico e lisosomi, probabilmente facilitando il routing dei lipidi per un successivo processamento. Al contrario, una proteina legante ossisteroli, ORP1L, sorprendentemente ha causato un ulteriore aumento del PA, in maniera dipendente dal suo sito di legame del colesterolo, suggerendo un dialogo più complesso tra i flussi di PA e di colesterolo.
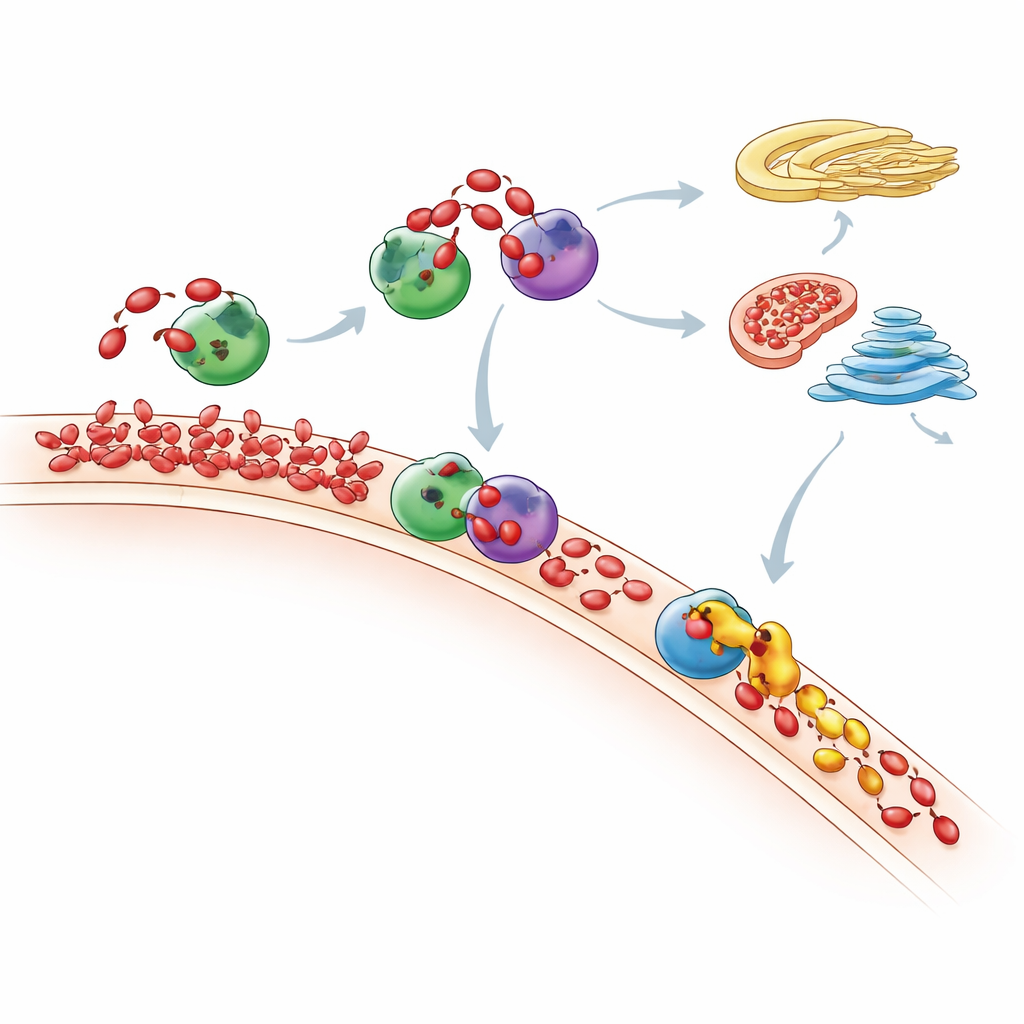
Dove finisce infine il PA in eccesso
Misurando l’intero panorama lipidico con spettrometria di massa sensibile, i ricercatori hanno tracciato come il mix di fosfolipidi della cellula cambiava dopo il “feeding” di PA. Hanno osservato che le impennate di PA sono di breve durata: col tempo molte molecole di PA vengono convertite in DAG e poi nei lipidi di membrana comuni attraverso la via di Kennedy, o in altri lipidi tramite la via CDP-DAG. I mitocondri sembrano svolgere un ruolo chiave, utilizzando un enzima chiamato TAMM41 per aiutare a convertire il PA in ingresso in fosfatidilglicerolo, un componente delle membrane mitocondriali. Quando Nir2 veniva depletata, il PA neoformato non rimaneva nel sito di produzione ma si accumulava nella regione del Golgi, dimostrando che la perturbazione di un singolo corriere può rimodellare il traffico lipidico nella cellula e alterare vie di segnalazione importanti come mTOR, un principale regolatore della crescita.
Perché questo lavoro è importante per la salute cellulare
Combinando una precisa “modifica delle membrane” con la marcatura di prossimità, questo studio fornisce un potente schema per scoprire come le cellule rilevano e correggono gli squilibri nella loro composizione lipidica. Per il PA, il lavoro mappa una rete di enzimi e proteine di trasporto che accorrono alle membrane sovraccariche, spostano il PA in luoghi più sicuri e lo trasformano in altri lipidi, mantenendo al contempo sotto controllo circuiti di segnalazione chiave. Poiché disturbi simili dei lipidi sono collegati a cancro, malattie metaboliche e neurodegenerazione, l’approccio feeding–fishing potrebbe essere utilizzato per scoprire nuovi bersagli farmacologici in molte condizioni in cui i lipidi di membrana modellano silenziosamente il comportamento cellulare.
Citazione: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Parole chiave: acido fosfatidico, omeostasi lipidica, proteomica delle membrane, proteine di trasferimento dei lipidi, modifica optogenetica delle membrane