Clear Sky Science · pl
Edytowanie błon z użyciem znakowania w bliskości ujawnia regulatorów homeostazy lipidów
Jak komórki utrzymują równowagę swojej tłustej powłoki
Każda komórka w twoim ciele jest otoczona cienką, tłustą powłoką zwaną błoną. Błony te to coś więcej niż proste bariery: ich dokładny skład lipidowy pomaga kontrolować wzrost komórek, komunikację i odpowiedzi na stres. Jednym z szczególnie silnych lipidów jest kwas fosfatydowy (PA), który działa niczym molekularny sygnał alarmowy. Nagłe wzrosty PA mogą włączać lub wyłączać kluczowe szlaki sygnalizacyjne, dlatego komórki muszą szybko i precyzyjnie regulować jego poziomy. To badanie ujawnia, jak komórki wykrywają nagłe skoki PA i rekrutują specyficzne białka, by przywrócić kontrolę nad tym potężnym lipidem.
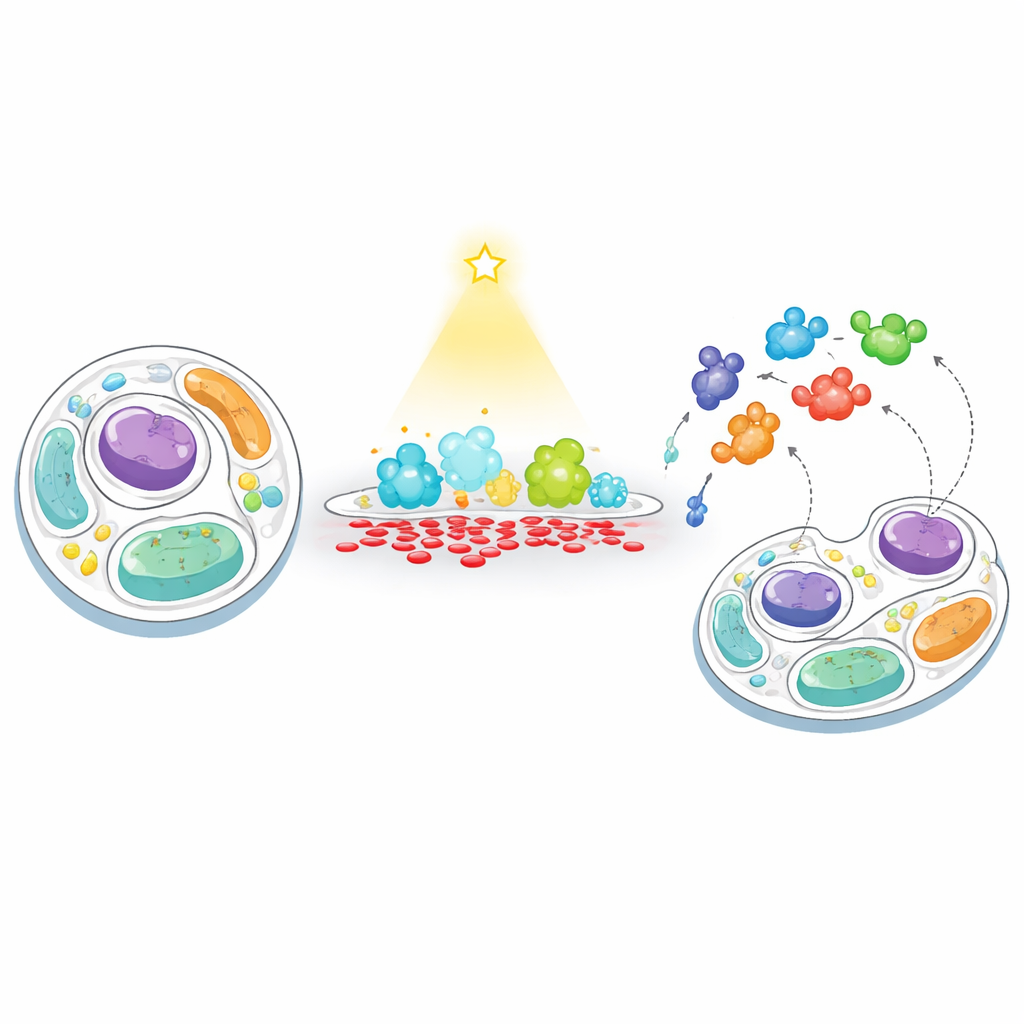
Nowy sposób „dokarmiania” i „łowienia” w błonach komórkowych
Naukowcy opracowali dwustopniową strategię, którą nazywają „dokarmianie–łowienie”, aby śledzić reakcje komórek, gdy poziom PA w błonie zostanie sztucznie zaburzony. Najpierw „dokarmiają” wybraną błonę PA przy użyciu enzymu kontrolowanego światłem — inżynierowanej wersji fosfolipazy D, którą można włączać za pomocą niebieskiego światła. Kierując ten enzym na powierzchnię komórki lub na lizosomy (komórkowe centra recyklingu), można wywołać krótkie, lokalne wybuchy produkcji PA. Następnie „łowią” pobliskie białka, przyczepiając do tej samej błony enzym znakujący biotyną (TurboID). Każde białko, które znajdzie się w pobliżu, zostaje oznaczone, a potem wychwycone i zidentyfikowane przy użyciu wysokoprzepustowej spektrometrii mas, co ujawnia, które białka są przyciągane do obszarów bogatych w PA lub z nich odsuwane.
Kto pojawia się przy skokach PA?
Stosując tę metodę w komórkach ludzkich, zespół zidentyfikował tysiące białek w pobliżu błony plazmatycznej i lizosomów, a następnie wyodrębnił te, których obfitość zmieniała się po wzroście poziomu PA. Wielu najsilniejszych responderów było już znanych z metabolizowania PA lub pokrewnych lipidów, co potwierdza słuszność podejścia. Enzymy zwane lipinami, które rozkładają PA do innego lipidu sygnalizacyjnego, diacyloglicerolu (DAG), były wzbogacone na błonach załadowanych PA, podczas gdy enzym produkujący DAG, który generuje PA, pojawiał się rzadziej — co sugeruje wbudowany układ sprzężenia zwrotnego. Najbardziej znane białko transportujące PA, Nir2, przemieściło się również zarówno do błon plazmatycznych bogatych w PA, jak i do lizosomów, podkreślając swoją centralną rolę w przemycie PA między organellami. Analiza ujawniła też zmiany w białkach powiązanych z mitochondriami i gospodarowaniem cholesterolem, sugerując, że skoki PA wpływają na wiele aspektów metabolizmu komórkowego.
Ukryci kurierzy, którzy przemieszczają i usuwają PA
Aby sprawdzić, które z rekrutowanych białek faktycznie pomagają oczyścić nadmiar PA, naukowcy skoncentrowali się na kilku białkach transferujących lipidy — molekularnych kurierach przemieszczających tłuszcze między błonami. Poprzez nadprodukcję tych kurierów i śledzenie fluorescencyjnego sensora PA odkryli, że Nir2 i białko zwane SCP2 znacząco zmniejszały nagromadzenie PA przy błonie plazmatycznej i w lizosomach. SCP2, wcześniej znane z transportu cholesterolu i kwasów tłuszczowych, wykazało także aktywność przenoszenia PA w oczyszczonym teście z liposomami, rozszerzając zakres jego funkcji. Inne białka transferujące, w tym PDZD8 i TEX2, nie obniżały bezpośrednio poziomów PA, lecz wydawały się zacieśniać fizyczne kontakty między retikulum endoplazmatycznym a lizosomami, prawdopodobnie ułatwiając kierowanie lipidów do późniejszego przetworzenia. W przeciwieństwie do tego, białko wiążące oksysterole, ORP1L, nieoczekiwanie powodowało dalszy wzrost PA w sposób zależny od jego miejsca wiążącego cholesterol, co sugeruje bardziej złożoną komunikację między przepływami PA i cholesterolu.
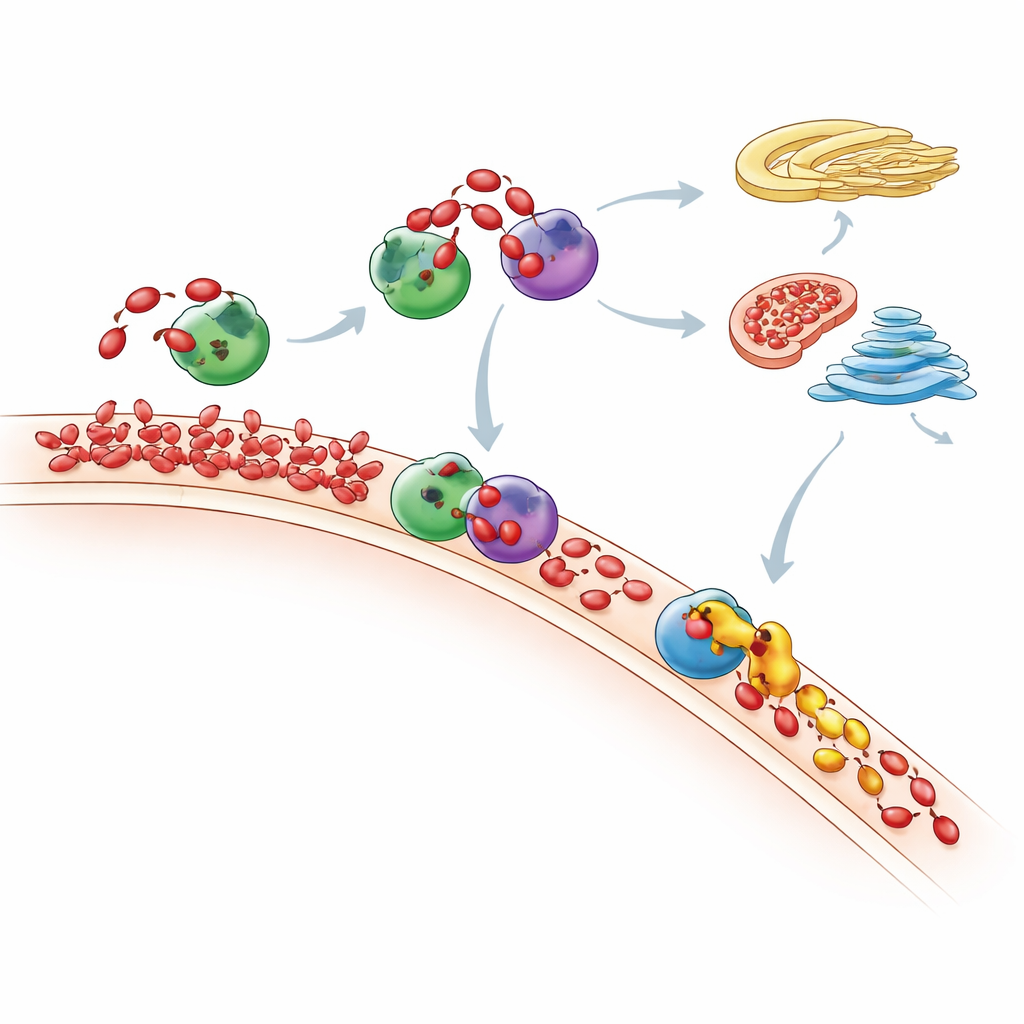
Dokąd ostatecznie trafia nadmiar PA
Mierząc pełny krajobraz lipidowy za pomocą czułej spektrometrii mas, badacze śledzili, jak cały skład fosfolipidów komórki zmienia się po „dokarmieniu” PA. Zauważyli, że skoki PA są krótkotrwałe: z upływem czasu wiele cząsteczek PA jest przekształcanych albo w DAG, a następnie w powszechne lipidy błonowe przez szlak Kennedy’ego, albo w inne lipidy przez szlak CDP-DAG. Mitochondria wydają się odgrywać kluczową rolę, wykorzystując enzym zwany TAMM41 do przekształcania napływającego PA w fosfatydyloglicerol, budulec błon mitochondrialnych. Gdy Nir2 został wyczerpany, nowo powstały PA nie pozostawał już tam, gdzie został wyprodukowany, lecz akumulował się w rejonie aparatu Golgiego, pokazując, że zakłócenie pracy jednego kuriera może przekierować ruch lipidów w komórce i zmieniać ważne szlaki sygnalizacyjne, takie jak mTOR, główny regulator wzrostu.
Dlaczego ta praca ma znaczenie dla zdrowia komórek
Łącząc precyzyjne „edytowanie błon” ze znakowaniem w bliskości, to badanie dostarcza potężnego planu działania do odkrywania, jak komórki wykrywają i korygują zaburzenia składu lipidowego. W przypadku PA praca mapuje sieć enzymów i białek transportujących, które pędzą do przeciążonych błon, przenoszą PA w bezpieczniejsze miejsca i przekształcają go w inne lipidy, równocześnie utrzymując w ryzach kluczowe obwody sygnalizacyjne. Ponieważ podobne zaburzenia lipidowe łączy się z rakiem, chorobami metabolicznymi i neurodegeneracją, podejście dokarmianie–łowienie może posłużyć do odkrywania nowych celów terapeutycznych w wielu schorzeniach, gdzie lipidy błon cicho kształtują zachowanie komórek.
Cytowanie: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Słowa kluczowe: kwas fosfatydowy, homeostaza lipidów, proteomika błon, białka przenoszące lipidy, opto-genetyczne edytowanie błon