Clear Sky Science · he
עריכת ממברנות בעזרת תיוג קרבה חושפת רגולטורים של הומאוסטזת שומנים
איך תאים שומרים על איזון שכבות השומן שלהם
כל תא בגופך עטוף במעטפה דקה ושומנית הנקראת ממברנה. ממברנות אלו יותר מסתם מחסומים: התערובת המדויקת של הליפידים בהן מסייעת לשלוט בצמיחה התאית, בתקשורת ובהתמודדות עם לחץ. ליפיד אחד במיוחד, חומצה פוספטידית (PA), מתפקד כפּעמון אזעקה מולקולרי. פרצי PA יכולים להדליק או לכבות מסלולי איתות מרכזיים, ולכן על התאים להעלות ולהוריד את רמותיו במהירות ובדיוק רב. המחקר הזה חושף כיצד תאים חשים התפרצויות פתאומיות של PA ומגייסים חלבונים ספציפיים כדי להחזיר את הליפיד החזק הזה תחת שליטה.
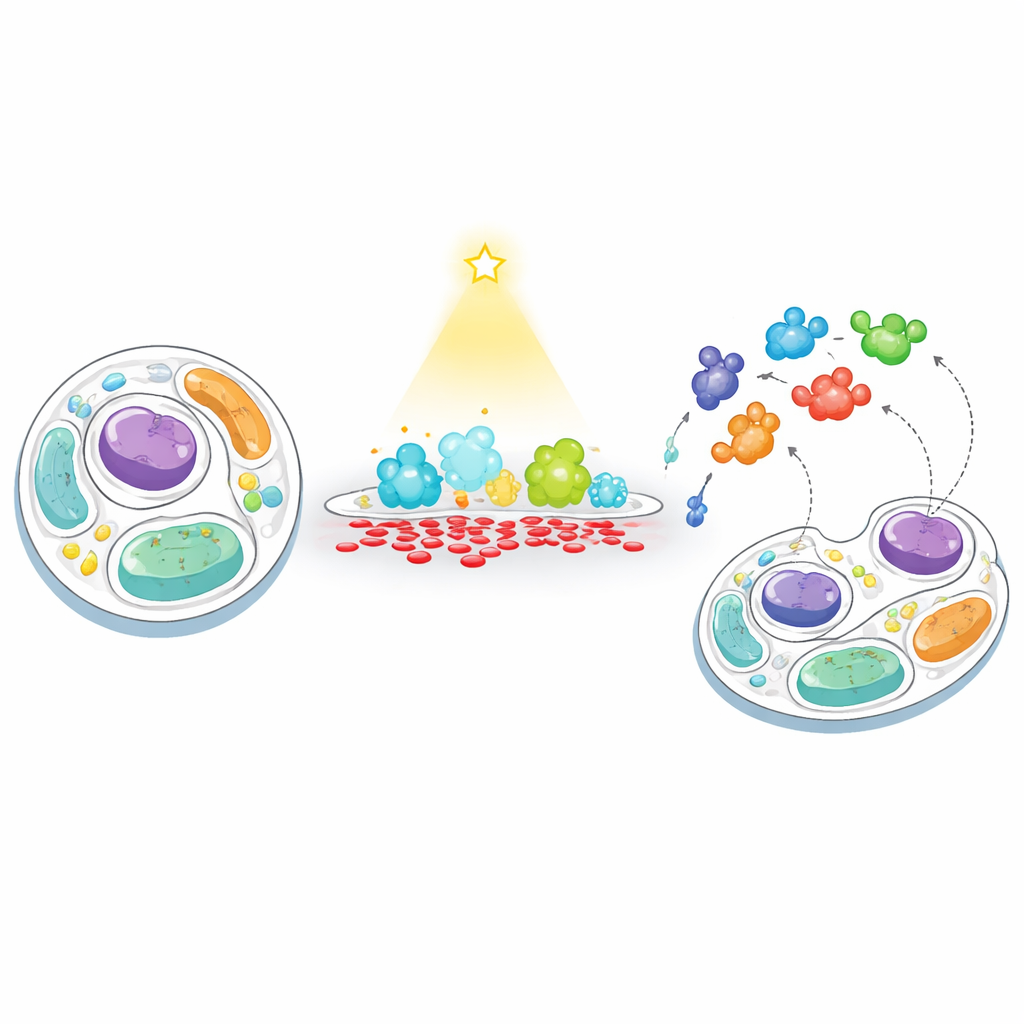
דרך חדשה "להאכיל" ו"לתפוס" בממברנות תאים
החוקרים פיתחו אסטרטגיה בשני שלבים שהם מכנים "האכלת–דיג" כדי לעקוב איך תאים מגיבים כאשר רמת ה‑PA בממברנה נדחפת באופן מלאכותי מחוץ לאיזון. ראשית, הם "מזינים" ממברנה נבחרת ב‑PA באמצעות אנזים הנשלט באור — גרסה מהונדסת של פוספוליפאז D שניתנת להדלקה בעזרת אור כחול לפי הצורך. על ידי מיקוד האנזים לפני השטח החיצוני של התא או בליזוזומים (מרכזי המיחזור של התא), הם יכלו לעורר פרצי ייצור PA קצרים ומקומיים. שנית, הם "דגים" לחלבונים קרובים על‑ידי חיבור אנזים תיוג עם ביוטין (TurboID) לאותה ממברנה. כל חלבון שמשוטט בקרבה מתוייג ולאחר מכן נתפס ומזוהה באמצעות ספקטרומטריית מסה ברצף גבוה, וחושף אילו חלבונים נמשכים לאזורי עשירי PA או נדחקים מהם.
מי מופיע כשה‑PA מזנקת?
ביישום השיטה על תאים אנושיים זיהתה הקבוצה אלפי חלבונים בסמוך לממברנת הפלזמה ולליזוזומים, ואז זיהתה את אלה שהשפע שלהם השתנה כאשר רמות PA עלו. רבים מהמשתתפים החזקים כבר היו ידועים כטפלים ב‑PA או בליפידים קרובים, מה שאישר את הגישה. אנזימים בשם ליפינים, המפרקים PA לליפיד איתות אחר, די־אצילגליצרול (DAG), נמצאו מועשרים על ממברנות טעונות ב‑PA, בעוד אנזים שמייצר DAG ומייצר PA הופיע פחות לעתים קרובות, מה שמרמז על מערכת משוב פנימית. חלבון ההעברה הידוע ביותר של PA, Nir2, גם הוא נודד לממברנות פלזמה ועשירות PA ולליזוזומים, מה שמדגיש את תפקידו המרכזי בהעברת PA בין האורגנלות. הניתוח חשף בנוסף שינויים בחלבונים קשורים למיטוכונדריה ולטיפול הכולסטרול, מה שמרמז כי פרצי PA מהדהדים عبر היבטים רבים של חילוף החומרים התאי.
שליחים חבויים שמעבירים ומסירים PA
כדי לבדוק אילו מהחלבונים המגויסים באמת מסייעים לנקות PA עודף, התמקדו המדענים בכמה חלבוני העברת ליפידים — שליחים מולקולריים שמעבירים שומנים בין ממברנות. על‑ידי ייצור-יתר של אותם שליחים ומעקב אחר חיישן פלואורסצנטי ל‑PA, הם מצאו כי Nir2 וחלבון בשם SCP2 הפחיתו באופן מובהק הצטברות PA בממברנת הפלזמה ובליזוזומים. SCP2, שהיה ידוע קודם לכן בהעברת כולסטרול וחומצות שומן, הראה גם פעילות נשיאת PA במבחן עם ליופוזומים טהורים, והרחיב בכך את תיאור התפקיד שלו. חלבוני העברה אחרים, כולל PDZD8 ו‑TEX2, לא הורידו ישירות את רמות ה‑PA אך נראו כמחברים פיזיים מהודקים בין הרטיקולום האנדופלזמתי וליזוזומים, דבר שעלול לסייע בניתוב ליפידים לעיבוד מאוחר יותר. בניגוד לכך, חלבון קושר אוקסיסטרול, ORP1L, הפתיע וגרם לעלייה נוספת ב‑PA, באופן שתלוי באתר הקושר כולסטרול שלו, מה שמרמז על תקשורת מסובכת יותר בין זרימות PA וכולסטרול.
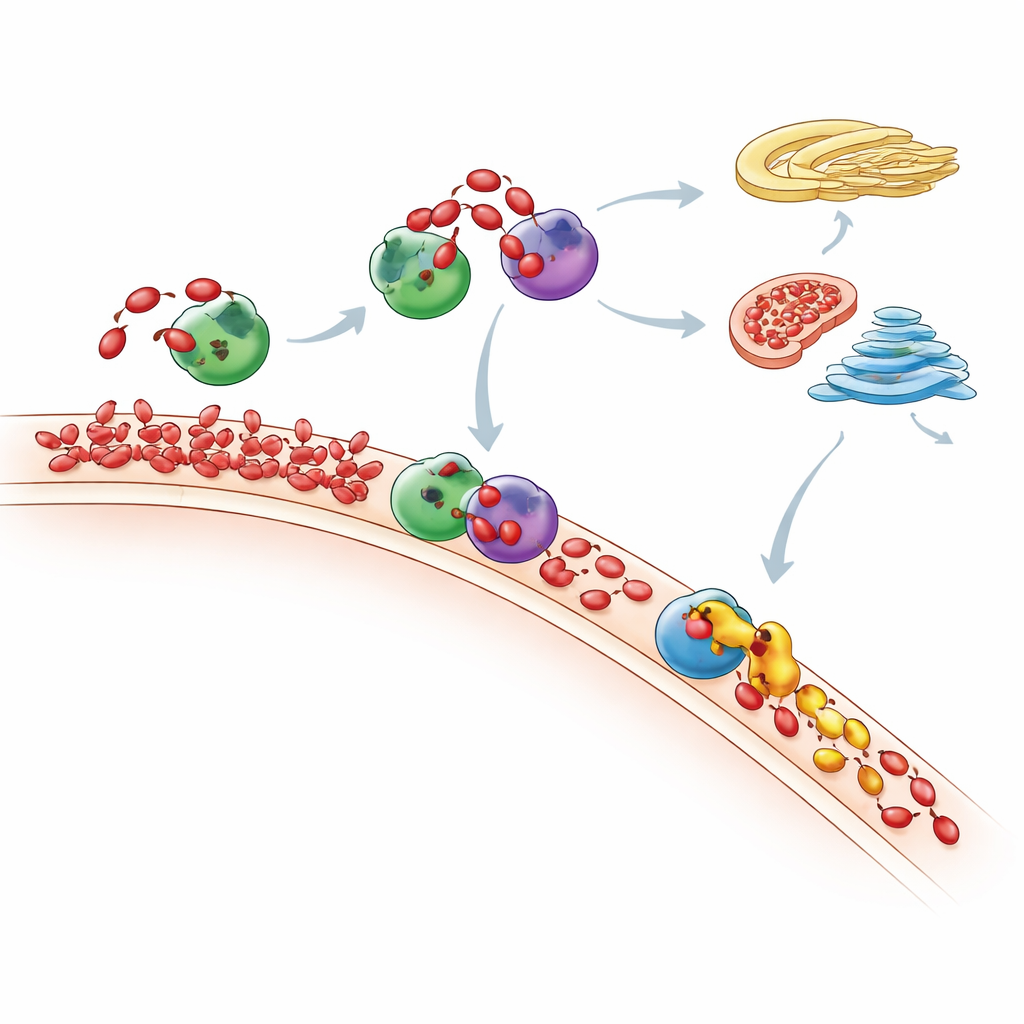
לאן ה‑PA העודף מגיע בסופו של דבר
על‑ידי מדידת הנוף הליפידי המלא בעזרת ספקטרומטריית מסה רגישת, עקבו החוקרים כיצד התערובת הכוללת של הפוספוליפידים בתא השתנתה לאחר "ההאכלה" ב‑PA. הם ראו כי פרצי PA הם קצרים־זמן: עם חלוף הזמן, מולקולות רבות של PA מומרות או ל‑DAG ולאחר מכן לליפידים ממברנליים נפוצים דרך מסלול קנדי, או לליפידים אחרים דרך מסלול CDP‑DAG. נראה כי המיטוכונדריה משחקות תפקיד מרכזי, באמצעות אנזים בשם TAMM41 המסייע להמיר PA נכנס לפוספטידילגליצרול, אבן בניין לממברנות מיטוכונדריאליות. כאשר Nir2 דוכא, ה‑PA שנוצר לא נשאר במקום בו הופק אלא הצטבר באזור הגולג'י, מה שמראה כי שיבוש שליח אחד יכול לשנות את תנועת הליפידים בתא ולהשפיע על מסלולי איתות חשובים כמו mTOR, רגולטור צמיחה מרכזי.
מדוע עבודה זו חשובה לבריאות התאים
על‑ידי שילוב "עריכת ממברנות" מדויקת עם תיוג קרבה, המחקר מספק שרטוט עוצמתי לגילוי כיצד תאים מזהים ומתוקנים חוסר איזון בהרכב הליפידים שלהם. עבור PA, העבודה ממפה רשת של אנזימים וחלבוני העברה שממהרים אל ממברנות עמוסות, מעבירים PA למקומות בטוחים יותר וממירים אותו לליפידים אחרים, תוך שמירה על מעגלי איתות מרכזיים. מאחר שהפרעות דומות בליפידים נקשרות לסרטן, מחלות מטבוליות והתנוונות נוירודית, גישת ההאכלה‑דיג עשויה לשמש לגילוי מטרות תרופתיות חדשות במגוון מצבים שבהם ליפידים ממברנליים מעצבים במתינות את התנהגות התא.
ציטוט: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
מילות מפתח: חומצה פוספטידית, הומאוסטזת ליפידים, פרוטאומיקס של ממברנות, חלבוני העברת ליפידים, עריכת ממברנות אופטוגנטית