Clear Sky Science · fr
Édition des membranes par marquage de proximité révèle des régulateurs de l’homéostasie lipidique
Comment les cellules maintiennent l’équilibre de leurs revêtements lipidiques
Chaque cellule de votre corps est enveloppée d’un mince manteau lipidique appelé membrane. Ces membranes ne sont pas de simples barrières : leur composition précise en lipides influe sur la croissance cellulaire, la communication et la réponse au stress. Un lipide particulièrement puissant, l’acide phosphatidique (PA), agit comme une alarme moléculaire. Des poussées de PA peuvent activer ou désactiver des voies de signalisation clés, si bien que la cellule doit pouvoir augmenter ou diminuer son niveau très rapidement et avec une grande précision. Cette étude révèle comment les cellules détectent des pics soudains de PA et recrutent des protéines spécifiques pour ramener ce lipide puissant sous contrôle.
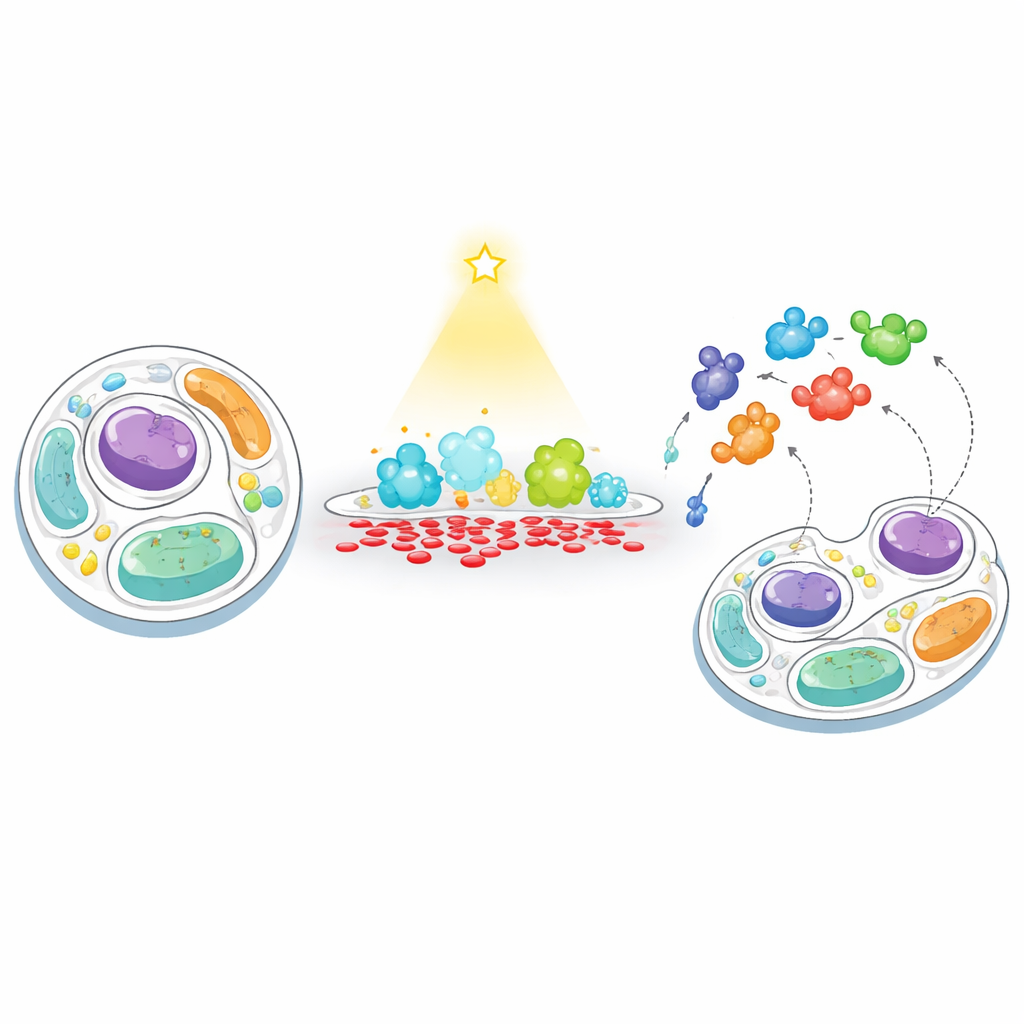
Une nouvelle façon de « nourrir » et de « pêcher » dans les membranes cellulaires
Les auteurs ont mis au point une stratégie en deux étapes qu’ils appellent « nourrir–pêcher » pour suivre la réponse cellulaire lorsque le niveau de PA d’une membrane est artificiellement perturbé. D’abord, ils « nourrissent » une membrane choisie en PA à l’aide d’une enzyme contrôlée par la lumière, une version modifiée de la phospholipase D activable à la demande par lumière bleue. En ciblant cette enzyme soit à la surface externe de la cellule, soit aux lysosomes (les centres de recyclage de la cellule), ils ont pu provoquer des bouffées courtes et localisées de production de PA. Ensuite, ils « pêchent » les protéines voisines en fixant une enzyme de marquage à la biotine (TurboID) à la même membrane. Toute protéine qui s’approche est marquée, puis capturée et identifiée par spectrométrie de masse à haut débit, ce qui révèle quelles protéines sont attirées par les régions riches en PA ou en sont repoussées.
Qui arrive quand le PA monte en flèche ?
En appliquant cette méthode à des cellules humaines, l’équipe a identifié des milliers de protéines proches de la membrane plasmique et des lysosomes, puis mis au jour celles dont l’abondance changeait lors de l’augmentation de PA. Beaucoup des répondants les plus marqués étaient déjà connus pour gérer le PA ou des lipides apparentés, validant ainsi l’approche. Des enzymes appelées lipines, qui dégradent le PA en un autre lipide de signalisation, le diacylglycérol (DAG), étaient enrichies sur les membranes chargées en PA, tandis qu’une enzyme produisant du DAG à partir du PA apparaissait moins, suggérant un mécanisme de rétroaction. La protéine de transfert de PA la mieux connue, Nir2, s’est aussi déplacée vers la membrane plasmique et les lysosomes riches en PA, soulignant son rôle central dans le transport du PA entre organites. L’analyse a également révélé des changements dans des protéines liées aux mitochondries et à la gestion du cholestérol, suggérant que les poussées de PA se répercutent sur de nombreux aspects du métabolisme cellulaire.
Des coursiers cachés qui déplacent et éliminent le PA
Pour tester quelles protéines recrutées contribuent réellement à éliminer l’excès de PA, les chercheurs se sont concentrés sur plusieurs protéines de transfert de lipides — des coursiers moléculaires qui déplacent des lipides entre membranes. En surexprimant ces coursiers et en suivant un capteur fluorescent de PA, ils ont découvert que Nir2 et une protéine nommée SCP2 réduisaient nettement l’accumulation de PA à la membrane plasmique et aux lysosomes. SCP2, connue auparavant pour transporter le cholestérol et les acides gras, a également montré une activité de transport de PA dans un essai purifié sur liposomes, élargissant ainsi son rôle. D’autres protéines de transfert, dont PDZD8 et TEX2, n’ont pas abaissé directement les niveaux de PA mais ont semblé resserrer les contacts physiques entre le réticulum endoplasmique et les lysosomes, aidant probablement à diriger les lipides vers un traitement ultérieur. En revanche, une protéine liant les oxystérols, ORP1L, a de manière inattendue causé une augmentation supplémentaire du PA, dépendante de son site de liaison au cholestérol, suggérant un dialogue plus complexe entre les flux de PA et de cholestérol.
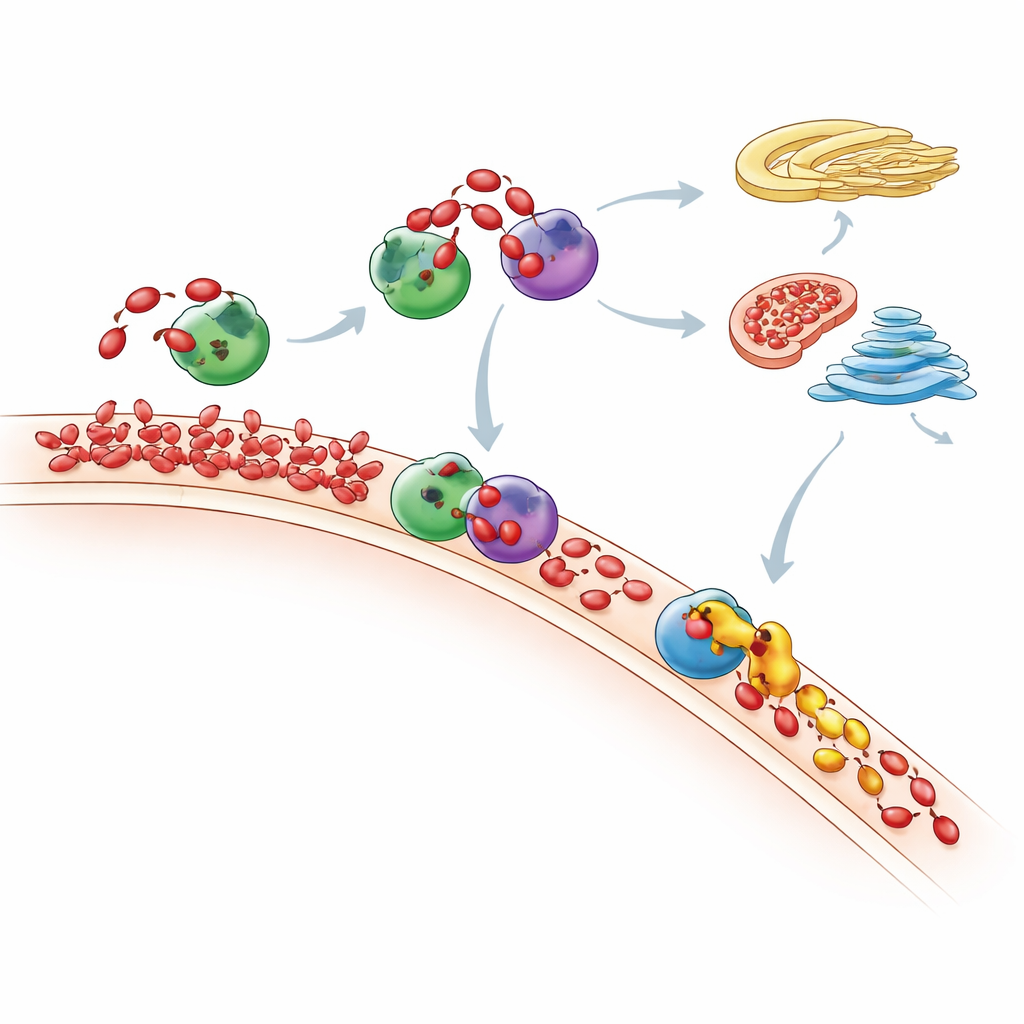
Où finit par aller l’excès de PA
En mesurant l’ensemble du paysage lipidique par spectrométrie de masse sensible, les chercheurs ont suivi comment le mélange phospholipidique de la cellule évoluait après le « nourrissage » en PA. Ils ont observé que les pics de PA sont de courte durée : au fil du temps, de nombreuses molécules de PA sont converties soit en DAG puis en lipides membranaires courants via la voie de Kennedy, soit en d’autres lipides via la voie CDP-DAG. Les mitochondries semblent jouer un rôle clé, en utilisant une enzyme nommée TAMM41 pour aider à convertir le PA entrant en phosphatidylglycérol, un élément constitutif des membranes mitochondriales. Lorsque Nir2 était épuisée, le PA nouvellement produit ne restait plus là où il avait été généré mais s’accumulait dans la région du Golgi, montrant que la perturbation d’un coursier peut rediriger le trafic lipidique dans la cellule et modifier des voies de signalisation importantes comme mTOR, un régulateur majeur de la croissance.
Pourquoi ce travail compte pour la santé cellulaire
En combinant une « édition membranaire » précise avec le marquage de proximité, cette étude fournit une feuille de route puissante pour découvrir comment les cellules détectent et corrigent les déséquilibres de leur composition lipidique. Pour le PA, le travail cartographie un réseau d’enzymes et de protéines de transport qui accourent vers les membranes surchargées, déplacent le PA vers des sites plus sûrs et le transforment en d’autres lipides, tout en maintenant l’équilibre des circuits de signalisation clés. Comme des perturbations similaires des lipides sont liées au cancer, aux maladies métaboliques et à la neurodégénérescence, l’approche nourrir–pêcher pourrait permettre de mettre au jour de nouvelles cibles thérapeutiques dans de nombreuses pathologies où les lipides membranaires influencent discrètement le comportement cellulaire.
Citation: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Mots-clés: acide phosphatidique, homéostasie lipidique, <keyword>protéines de transfert de lipides, édition membranaire optogénétique