Clear Sky Science · pt
Edição de membrana com marcação por proximidade revela reguladores da homeostase lipídica
Como as Células Mantêm Seu Revestimento Gordo em Equilíbrio
Cada célula do seu corpo é envolvida por uma fina camada gordurosa chamada membrana. Essas membranas são mais do que simples barreiras: sua composição exata de lipídios ajuda a controlar como as células crescem, se comunicam e respondem ao estresse. Um lipídio especialmente influente, o ácido fosfatídico (PA), age como um alarme molecular. Picos de PA podem ligar ou desligar vias de sinalização chave, então as células precisam aumentar e reduzir seus níveis de forma muito rápida e precisa. Este estudo revela como as células detectam surtos súbitos de PA e recrutam proteínas específicas para trazer esse lipídio potente novamente sob controle.
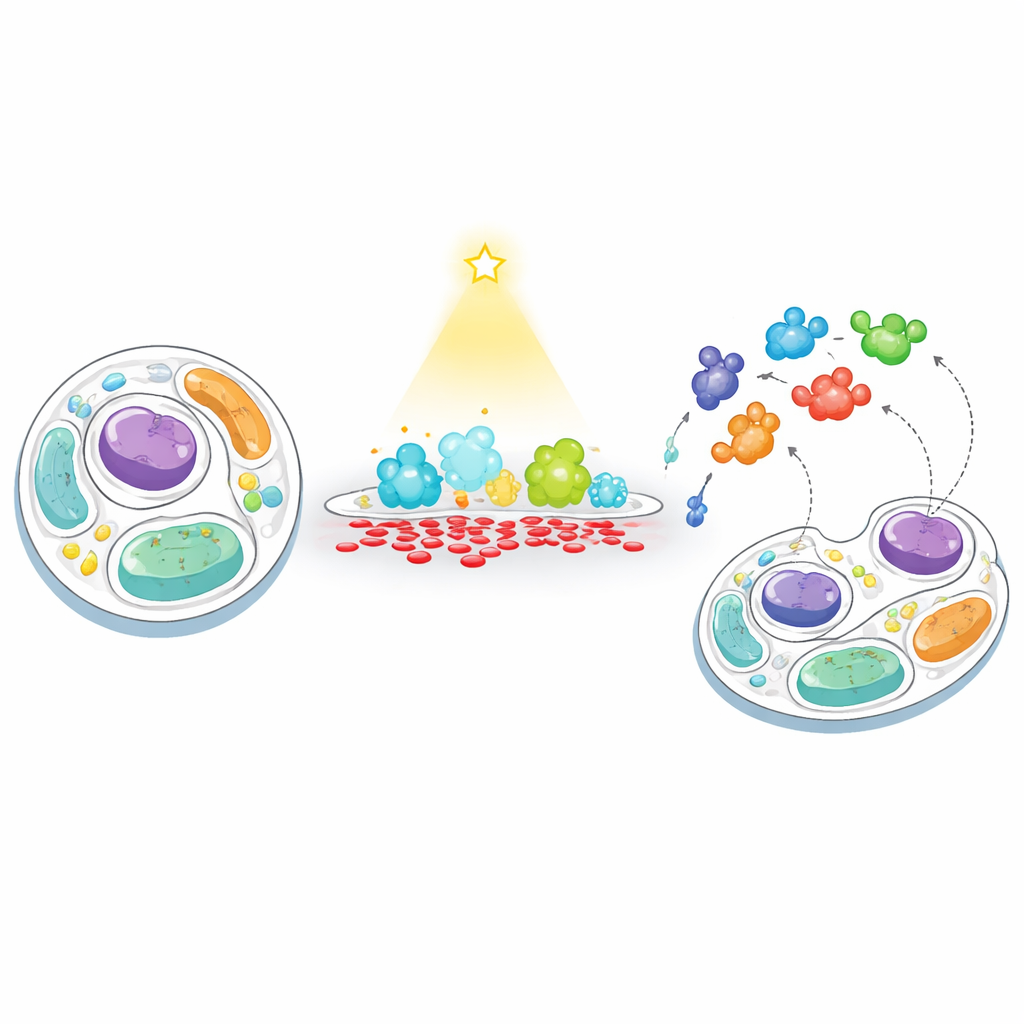
Uma Nova Maneira de “Alimentar” e “Pescar” nas Membranas Celulares
Os pesquisadores desenvolveram uma estratégia em dois passos que chamam de “alimentar–pescar” para rastrear como as células respondem quando o nível de PA de uma membrana é artificialmente desequilibrado. Primeiro, eles “alimentam” uma membrana escolhida com PA usando uma enzima controlada por luz, uma versão modificada da fosfolipase D que pode ser ativada à vontade com luz azul. Ao direcionar essa enzima para a superfície externa da célula ou para lisossomos (os centros de reciclagem celular), eles puderam desencadear explosões curtas e localizadas de produção de PA. Segundo, eles “pescam” proteínas próximas ao acoplar uma enzima de biotinilação (TurboID) à mesma membrana. Qualquer proteína que passe por ali é marcada e depois capturada e identificada por espectrometria de massa de alto rendimento, revelando quais proteínas são atraídas para regiões ricas em PA ou delas repelidas.
Quem Aparece Quando o PA Dispara?
Aplicando esse método em células humanas, a equipe identificou milhares de proteínas próximas à membrana plasmática e aos lisossomos, e então apontou aquelas cuja abundância mudou quando os níveis de PA aumentaram. Muitos dos respondedores mais fortes já eram conhecidos por lidar com PA ou lipídios relacionados, validando a abordagem. Enzimas chamadas lipinas, que degradam PA em outro lipídio de sinalização, diacilglicerol (DAG), estavam enriquecidas nas membranas carregadas de PA, enquanto uma enzima que produz DAG a partir de PA apareceu com menos frequência, sugerindo um sistema de feedback embutido. A proteína de transferência de PA mais conhecida, Nir2, também se deslocou tanto para membranas plasmáticas ricas em PA quanto para lisossomos, ressaltando seu papel central no transporte de PA entre organelas. A análise também revelou alterações em proteínas ligadas às mitocôndrias e ao manejo de colesterol, sugerindo que os surtos de PA repercutem em muitos aspectos do metabolismo celular.
Correios Ocultos que Movem e Removem PA
Para testar quais proteínas recrutadas realmente ajudam a eliminar o excesso de PA, os cientistas focaram em várias proteínas de transferência de lipídios — mensageiros moleculares que movem gorduras entre membranas. Ao superproduzir esses mensageiros e acompanhar um sensor fluorescente de PA, descobriram que Nir2 e uma proteína chamada SCP2 reduziram de forma marcante o acúmulo de PA na membrana plasmática e nos lisossomos. A SCP2, previamente conhecida por transportar colesterol e ácidos graxos, também mostrou atividade de transporte de PA em um ensaio purificado com lipossomos, ampliando sua descrição funcional. Outras proteínas de transferência, incluindo PDZD8 e TEX2, não reduziram diretamente os níveis de PA, mas pareceram estreitar contatos físicos entre o retículo endoplasmático e lisossomos, provavelmente ajudando a direcionar lipídios para processamento posterior. Em contraste, uma proteína de ligação a oxisteróis, ORP1L, causou inesperadamente um aumento adicional de PA, de maneira dependente de seu sítio de ligação ao colesterol, sugerindo uma comunicação mais complexa entre os fluxos de PA e colesterol.
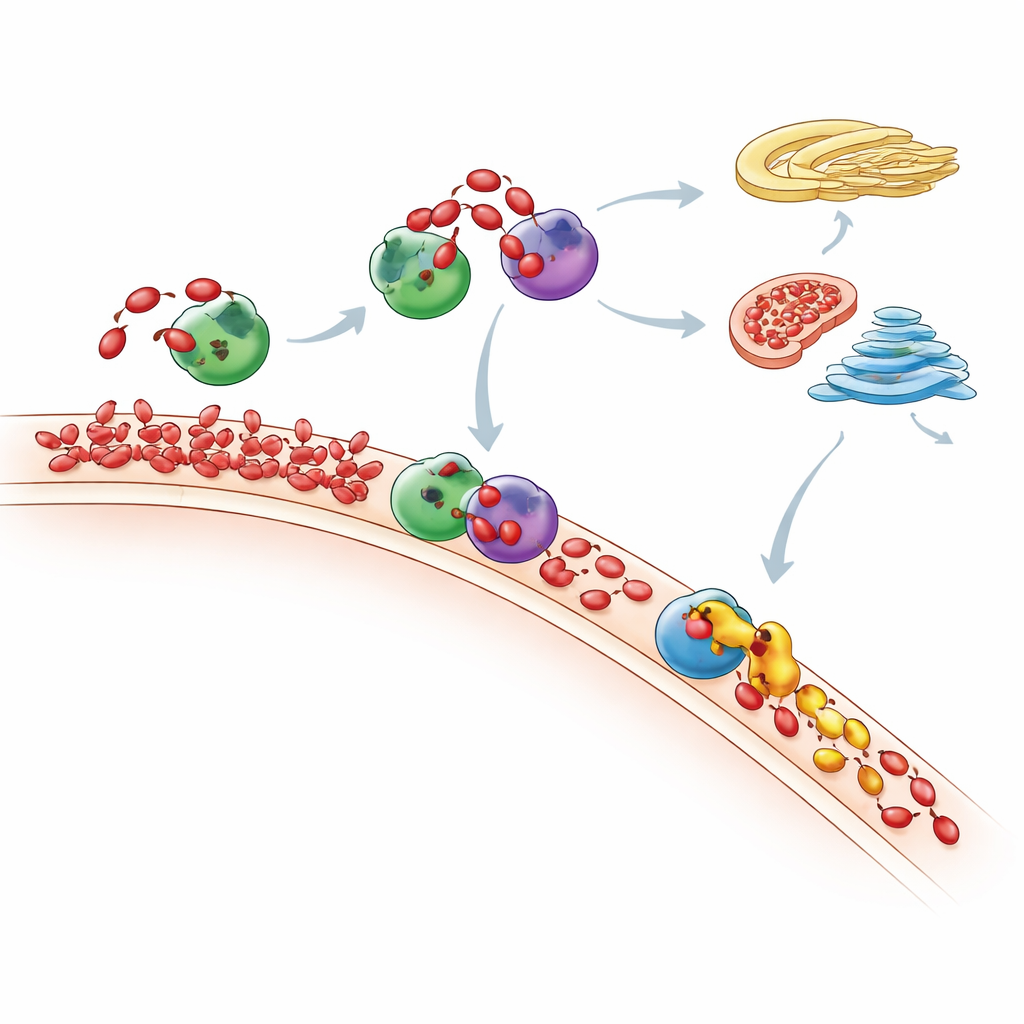
Onde o Excesso de PA Vai no Final das Contas
Medindo o panorama lipídico completo com espectrometria de massa sensível, os pesquisadores rastrearam como toda a mistura de fosfolipídios da célula mudou após a “alimentação” com PA. Eles observaram que os picos de PA são de curta duração: com o tempo, muitas moléculas de PA são convertidas em DAG e depois em lipídios de membrana comuns pela via de Kennedy, ou em outros lipídios pela rota CDP-DAG. As mitocôndrias parecem desempenhar um papel chave, usando uma enzima chamada TAMM41 para ajudar a converter o PA recebido em fosfatidilglicerol, um bloco de construção para membranas mitocondriais. Quando Nir2 foi depletada, o PA recém-produzido deixou de permanecer onde foi gerado e se acumulou na região do Golgi, mostrando que interromper um mensageiro pode redirecionar o tráfego de lipídios pela célula e alterar vias de sinalização importantes, como mTOR, um regulador de crescimento de grande relevância.
Por Que Este Trabalho Importa para a Saúde Celular
Ao combinar a precisa “edição de membrana” com marcação por proximidade, este estudo fornece um roteiro poderoso para descobrir como as células detectam e corrigem desequilíbrios em sua composição lipídica. Para o PA, o trabalho mapeia uma rede de enzimas e proteínas de transporte que correm para membranas sobrecarregadas, movem o PA para locais mais seguros e o transformam em outros lipídios, tudo enquanto mantêm circuitos de sinalização centrais sob controle. Como distúrbios lipídicos semelhantes estão associados ao câncer, doenças metabólicas e neurodegeneração, a abordagem alimentar–pescar pode ser usada para revelar novos alvos medicinais em muitas condições nas quais os lipídios de membrana moldam discretamente o comportamento celular.
Citação: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Palavras-chave: ácido fosfatídico, homeostase de lipídios, proteômica de membranas, proteínas de transferência de lipídios, edição de membrana optogenética