Clear Sky Science · sv
Membranredigering med närhetsmärkning avslöjar regulatorer av lipidbalans
Hur celler håller sina fettlager i balans
Varje cell i din kropp är omsluten av en tunn, fet hinna kallad membran. Dessa membraner är mer än enkla barriärer: deras precisa blandning av lipider hjälper till att styra hur celler växer, kommunicerar och reagerar på stress. En särskilt potent lipid, fosfatidsyra (PA), fungerar som en molekylär larmklocka. Kortvariga ökningar av PA kan slå av och på viktiga signalvägar, så cellerna måste snabbt och exakt kunna höja och sänka dess nivåer. Denna studie visar hur celler känner av plötsliga PA-ökningar och rekryterar särskilda proteiner för att återställa kontrollen över denna kraftfulla lipid.
En ny metod för att ”mata” och ”fiska” i cellmembran
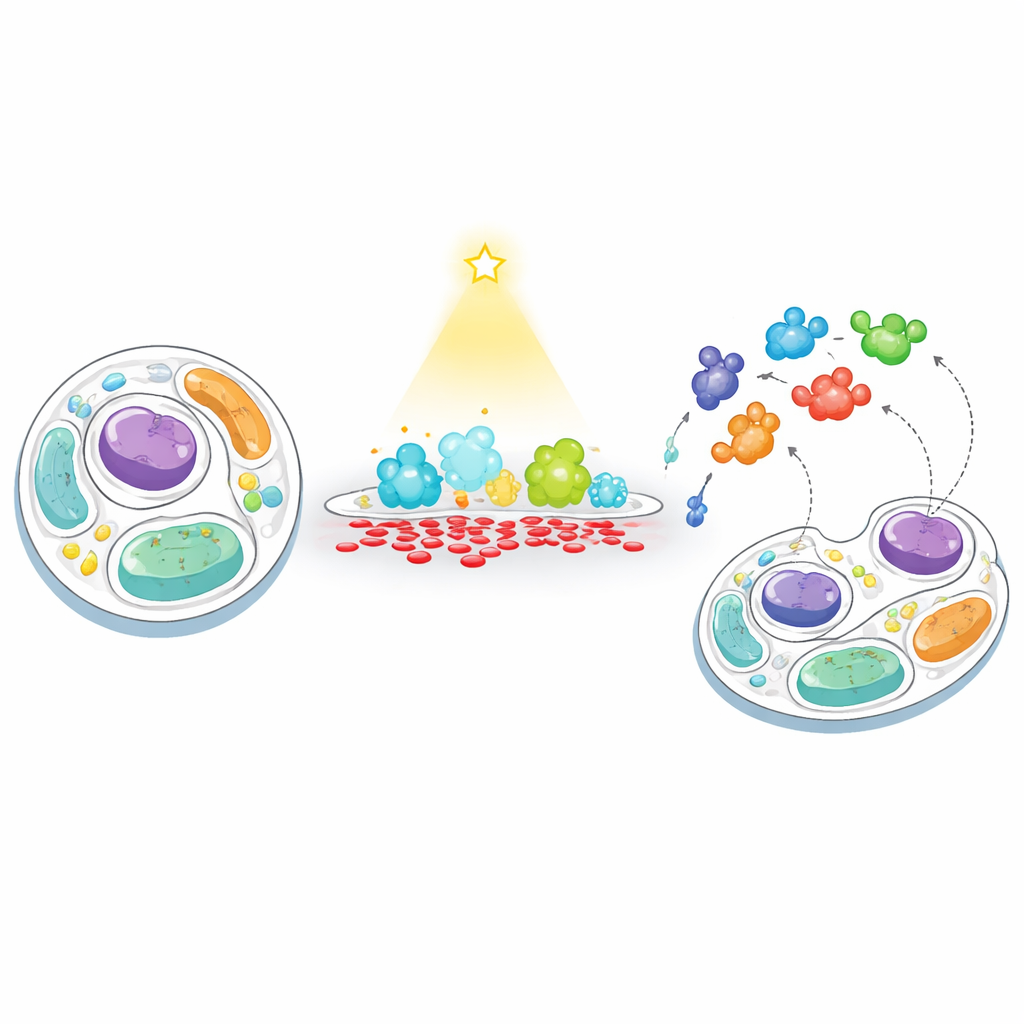
Forskarna utvecklade en tvåstegsstrategi som de kallar ”mata–fiska” för att följa hur celler svarar när ett membrans PA-nivå konstgjort sätts ur balans. Först ”matar” de ett valt membran med PA med hjälp av ett ljusstyrt enzym, en modifierad version av fosfolipas D som kan aktiveras med blått ljus. Genom att rikta detta enzym till antingen cellens yta eller till lysosomer (cellens återvinningscentraler) kunde de framkalla korta, lokaliserade PA-utbrott. Sedan ”fiskar” de efter närliggande proteiner genom att fästa ett biotinmärkande enzym (TurboID) vid samma membran. Alla proteiner som passerar i närheten blir märkta och kan senare fångas in och identifieras med högkapacitets masspektrometri, vilket avslöjar vilka proteiner som dras till eller avstöts från PA-rika regioner.
Vem dyker upp när PA skjuter i höjden?
När metoden tillämpades på humana celler identifierade teamet tusentals proteiner nära plasmamembranet och lysosomerna, och pekade sedan ut de som ändrade i mängd när PA-nivåerna steg. Många av de starkaste responserna kom från proteiner som redan var kända för att hantera PA eller närliggande lipider, vilket validerar tillvägagångssättet. Enzymer kallade lipiner, som bryter ner PA till en annan signalmolekyl, diacylglycerol (DAG), var förhöjda på PA-belagda membran, medan ett DAG-framställande enzym som genererar PA syntes mindre ofta, vilket antyder ett inbyggt feedbacksystem. Den mest kända PA-transportören, Nir2, flyttade också till både PA-rika plasmamembran och lysosomer, vilket understryker dess centrala roll i shuttling av PA mellan organeller. Analysen avslöjade dessutom förändringar i proteiner kopplade till mitokondrier och kolesterolhantering, vilket tyder på att PA-ökningar får genomslag i många delar av cellens metabolism.
Dolda kurirer som flyttar och avlägsnar PA
För att testa vilka rekryterade proteiner som faktiskt hjälper till att rensa överskott av PA fokuserade forskarna på flera lipidtransportproteiner—molekylära kurirer som flyttar fetter mellan membran. Genom att överuttrycka dessa kurirer och följa en fluorescerande PA-sensor fann de att Nir2 och ett protein kallat SCP2 markant minskade PA-ansamling vid plasmamembranet och i lysosomer. SCP2, tidigare känt för att transportera kolesterol och fettsyror, visade även PA-bärande aktivitet i en renad liposom-assay, vilket breddar dess funktionsbeskrivning. Andra transportproteiner, inklusive PDZD8 och TEX2, sänkte inte direkt PA-nivåerna men verkade istället stärka de fysiska kontakterna mellan endoplasmatiska retikulumet och lysosomer, sannolikt för att underlätta riktning av lipider för vidare bearbetning. I kontrast orsakade ett oxysterolbindande protein, ORP1L, oväntat ytterligare PA-ökning, på ett sätt som var beroende av dess kolesterolbindande sajt, vilket antyder en mer komplex korsprat mellan PA- och kolesterolflöden.
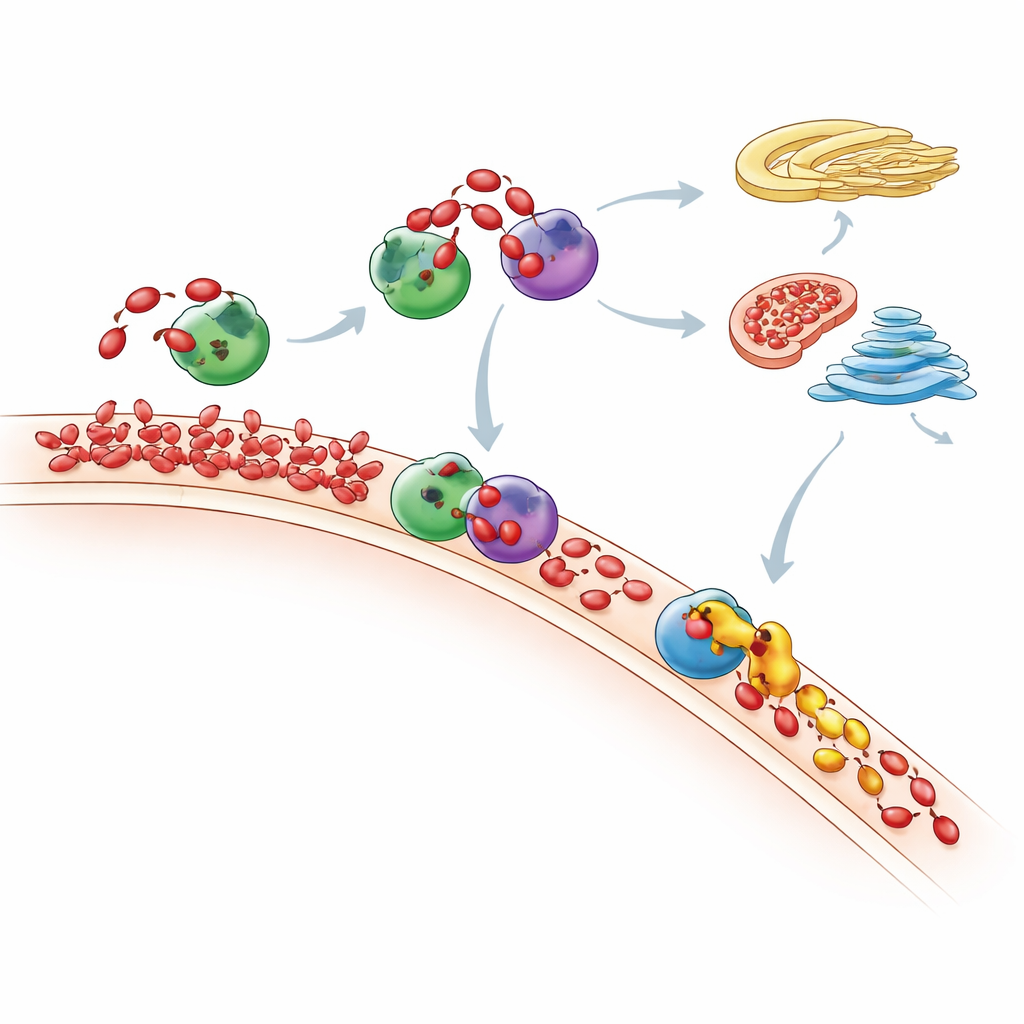
Vart tar det extra PA:t vägen
Genom att mäta hela lipidlandskapet med känslig masspektrometri följde forskarna hur cellens hela fosfolipidmix förändrades efter PA-”mating”. De såg att PA-toppar är kortlivade: med tiden omvandlas många PA-molekyler antingen till DAG och därefter till vanliga membranlipider via Kennedy-vägen, eller till andra lipider via CDP-DAG-vägen. Mitokondrier verkar spela en nyckelroll genom att använda ett enzym kallat TAMM41 för att hjälpa omvandla inkommande PA till fosfatidylglycerol, en byggsten för mitokondriella membran. När Nir2 utarmades stannade inte nysyntetiserad PA kvar där den producerats utan ackumulerades istället i Golgiområdet, vilket visar att störning av en kurir kan omdirigera lipidtrafiken i cellen och ändra viktiga signalvägar såsom mTOR, en central regulator av tillväxt.
Varför detta arbete är viktigt för cellhälsa
Genom att kombinera preciserad ”membranredigering” med närhetsmärkning ger denna studie en kraftfull mall för att upptäcka hur celler känner av och korrigerar obalanser i sin lipiduppsättning. För PA kartlägger arbetet ett nätverk av enzymer och transportproteiner som strömmar till överlastade membraner, förflyttar PA till säkrare platser och omvandlar den till andra lipider, samtidigt som viktiga signalvägar hålls i schack. Eftersom liknande lipidstörningar är kopplade till cancer, metabola sjukdomar och neurodegeneration, kan mata–fiska-ansatsen användas för att hitta nya läkemedelsmål i många tillstånd där membranlipider tyst formar cellbeteende.
Citering: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Nyckelord: fosfatidsyra, lipidbalans, membranproteomik, lipidtransportproteiner, optogenetisk membranredigering