Clear Sky Science · ar
تحرير الغشاء باستخدام الوسم بالتقارب يكشف منظِّمي توازن الدهون
كيف تحافظ الخلايا على توازن طبقاتها الدهنية
كل خلية في جسمك مغطاة بطبقة رقيقة دهنية تُسمى غشاء. هذه الأغشية ليست مجرد حواجز بسيطة: فالتكوين الدقيق للدهون فيها يساعد على التحكم في كيفية نمو الخلايا وتواصلها واستجابتها للضغط. أحد الدهون القوية بشكل خاص، حمض الفسفاتيديك (PA)، يعمل كجرس إنذار جزيئي. يمكن لاندفاعات PA أن تشغّل أو تطفئ مسارات إشارات رئيسية، لذلك يجب على الخلايا رفع وخفض مستوياته بسرعة ودقّة. تكشف هذه الدراسة كيف تستشعر الخلايا الارتفاعات المفاجئة في PA وتستدعي بروتينات محددة لإعادة هذا الدهون القوي تحت السيطرة.
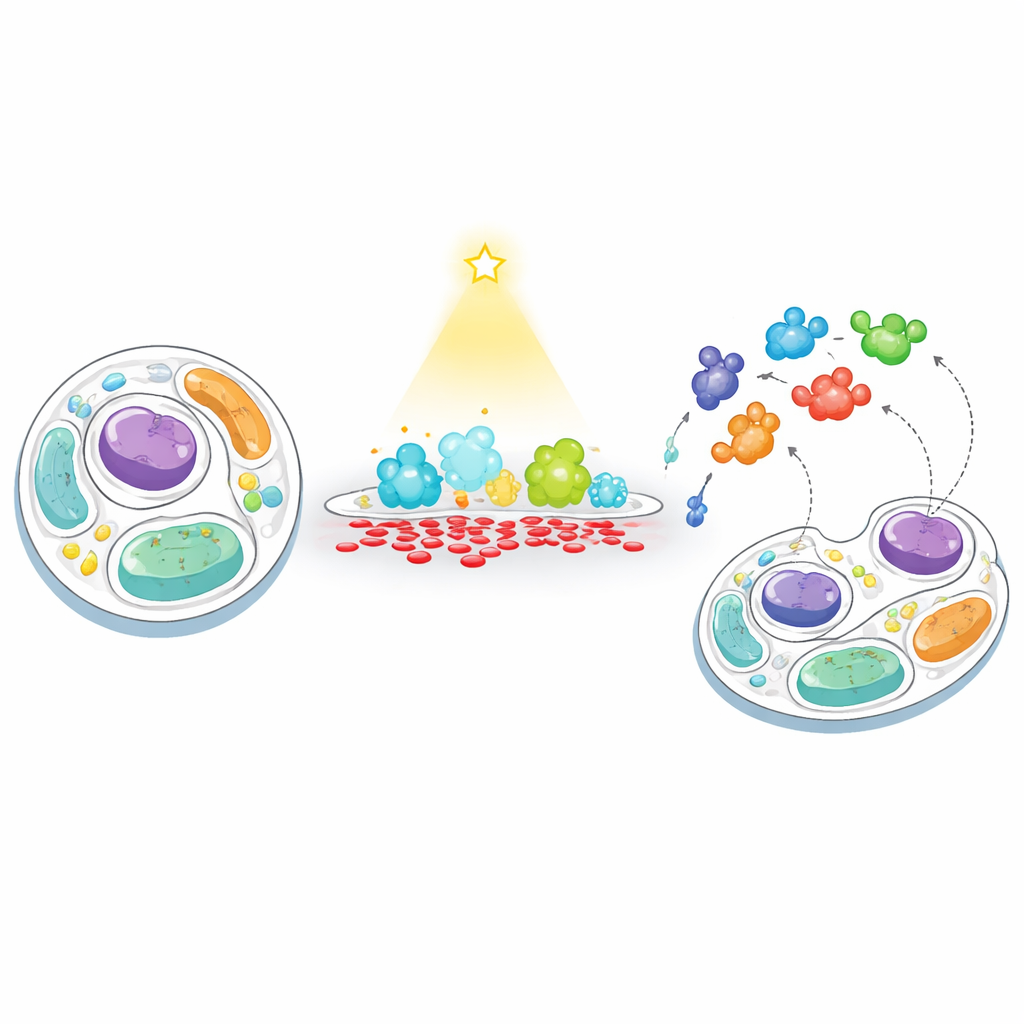
طريقة جديدة لـ «إطعام» و«اصطياد» في أغشية الخلايا
طوّر الباحثون استراتيجية من خطوتين يسمونها «الإطعام–الاصطياد» لتتبع كيفية استجابة الخلايا عندما يُدفع مستوى PA في غشاء ما إلى خارج التوازن بشكل مصطنع. أولاً، «يطعمون» غشاء محدداً بـ PA باستخدام إنزيم يمكن التحكم فيه بضوء، وهو نسخة مهندسة من فسفوليباز D يمكن تشغيلها عند الرغبة باستخدام ضوء أزرق. باستهداف هذا الإنزيم إما إلى السطح الخارجي للخلية أو إلى الليزوزومات (مراكز إعادة التدوير داخل الخلية)، أمكنهم تحفيز اندفاعات قصيرة ومحصورة من إنتاج PA. ثانياً، «يصطادون» البروتينات القريبة عن طريق ربط إنزيم وسم بالبِيوتِين (TurboID) بنفس الغشاء. أي بروتين يقترب يتم وسمه لاحقاً ثم التقاطه وتحديد هويته بواسطة قياس طيفي عالي الإنتاجية، مكشوفاً أي البروتينات تنجذب إلى مناطق غنية بـ PA أو تُبعد عنها.
من يظهر عندما يرتفع PA؟
بتطبيق هذه الطريقة على خلايا بشرية، حدّد الفريق آلاف البروتينات قرب الغشاء البلازمي والليزوزومات، ثم عيّن أولئك الذين تغيّر وجودهم عندما ارتفعت مستويات PA. العديد من أقوى المستجيبين كانت معروفًة بالفعل بتعاملها مع PA أو الدهون ذات الصلة، مما يثبت صحة النهج. كانت الإنزيمات المسماة لبينز (lipins)، التي تكسر PA إلى دهون إشارات أخرى، الدياسيلغليسيرول (DAG)، مُكثفة على الأغشية المحمّلة بـ PA، بينما ظهر إنزيم يصنع DAG ويُنتج PA بوتيرة أقل، مما يوحي بوجود نظام تغذية راجعة مضمّن. البروتين الناقل الأبرز لـ PA، Nir2، تحرّك أيضاً إلى كل من الأغشية البلازمية والليزوزومية الغنية بـ PA، مما يؤكد دوره المركزي في نقل PA بين العضيات. وكشفت التحليلات أيضاً تغيّرات في بروتينات مرتبطة بالميتوكوندريا وتعامل الكوليسترول، مما يشير إلى أن اندفاعات PA تترك تأثيراً عبر جوانب كثيرة من أيض الخلية.
الرسل الخفية التي تحرّك وتزيل PA
لاختبار أي البروتينات المُستدعاة تُسهم فعلاً في إزالة الفائض من PA، ركّز العلماء على عدة بروتينات نقل دهون — رسولات جزيئية تنقل الدهون بين الأغشية. من خلال الإفراط في إنتاج هذه الرسولات وتتبع حساس فلوري لـ PA، وجدوا أن Nir2 وبروتيناً يُدعى SCP2 قلّلا بشكل ملحوظ من تراكم PA على الغشاء البلازمي والليزوزومات. أظهر SCP2، المعروف سابقاً بنقله للكوليسترول والأحماض الدهنية، نشاطاً في حمل PA أيضاً في تجربة مع ليبوزومات مُنقّاة، موسعاً وصف مهمته. بروتينات ناقلة أخرى، بما في ذلك PDZD8 وTEX2، لم تخفض مستويات PA مباشرةً لكنها بدت أنها تشدّ الاتصالات الفيزيائية بين الشبكة الإندوبلازمية والليزوزومات، مما يساعد على توجيه الدهون للمعالجة لاحقاً. بالمقابل، تبيّن أن بروتين ربط الأوكسستيرول ORP1L تسبب بشكل غير متوقع في ارتفاع إضافي لـ PA، بطريقة اعتمدت على موقعه لربط الكوليسترول، مما يوحي بوجود حوار أكثر تعقيداً بين تدفّقات PA والكوليسترول.
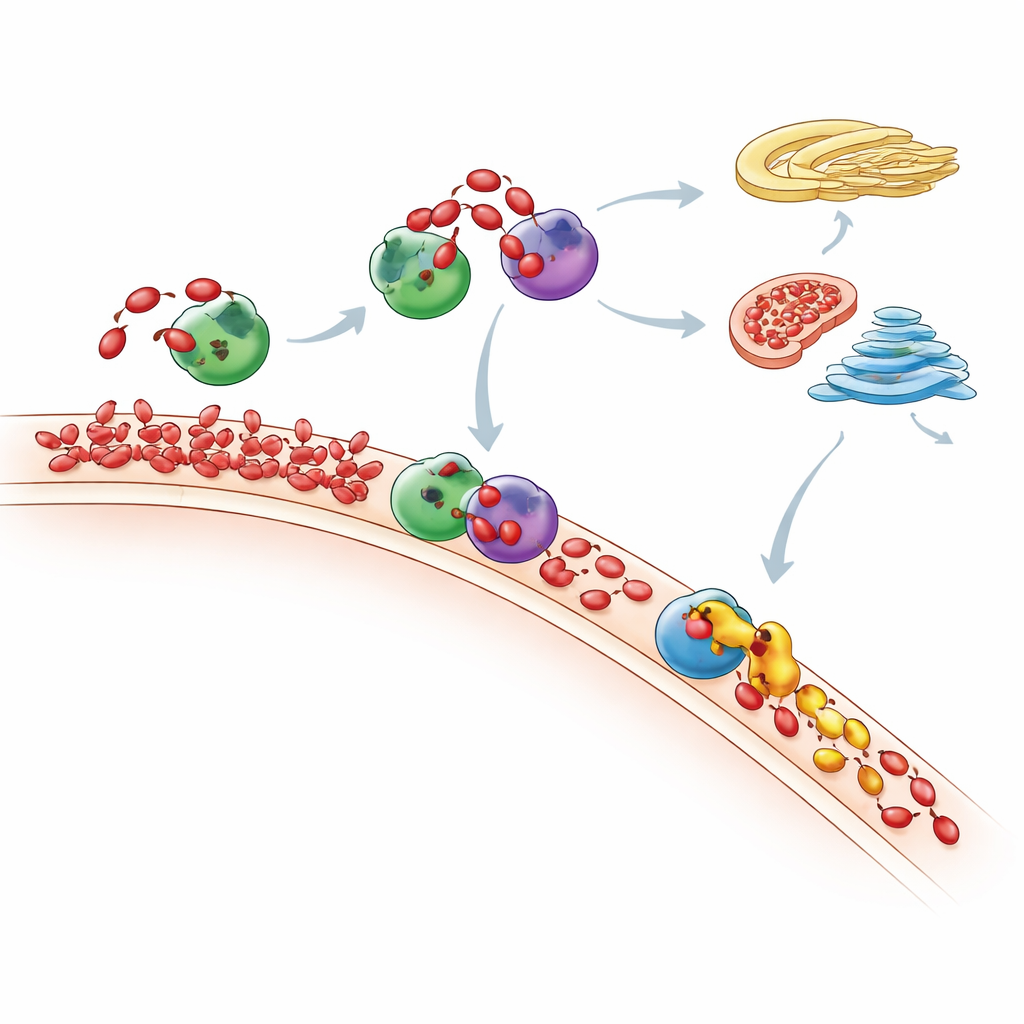
أين تذهب PA الإضافية في النهاية
بقياس المشهد الكامل للدهون بواسطة قياس طيفي حساس، تتبّع الباحثون كيف تغيّر مزيج الفسفوليبيدات في الخلية بعد «الإطعام» بـ PA. لاحظوا أن اندفاعات PA قصيرة العمر: مع مرور الوقت، يتحول كثير من جزيئات PA إما إلى DAG ثم إلى دهون غشائية شائعة عبر مسار كينيدي، أو إلى دهون أخرى عبر مسار CDP-DAG. تبدو الميتوكوندريا أنها تلعب دوراً رئيسياً، مستخدمة إنزيمًا يُسمى TAMM41 للمساعدة في تحويل PA الوافد إلى فسفاتيديلغليسيرول، وهو لبنة بناء لأغشية الميتوكوندريا. عندما نُقص Nir2، لم يعد PA الجديد يبقى في موقع إنتاجه بل تراكم بدلاً من ذلك في منطقة جهاز غولجي، مما يبيّن أن تعطيل رسول واحد يمكن أن يعيد توجيه حركة الدهون داخل الخلية ويغيّر مسارات إشارات مهمة مثل mTOR، المنظم الرئيسي للنمو.
لماذا تهم هذه الدراسة لصحة الخلايا
من خلال الجمع بين «تحرير الغشاء» الدقيق والوسم بالتقارب، توفر هذه الدراسة مخططاً قوياً لاكتشاف كيف تكشف الخلايا عن اختلالات في تكوين الدهون لديها وتصحيحها. بالنسبة لـ PA، ترسم الدراسة شبكة من الإنزيمات وبروتينات النقل التي تتدافع إلى الأغشية المحمّلة، وتنقل PA إلى مواقع أكثر أماناً، وتحوله إلى دهون أخرى، كل ذلك مع الحفاظ على دوائر الإشارة الأساسية تحت السيطرة. وبما أن اضطرابات مماثلة في الدهون مرتبطة بالسرطان وأمراض التمثيل الغذائي والتنكس العصبي، يمكن أن تُستخدم طريقة الإطعام–الاصطياد للكشف عن أهداف دوائية جديدة في العديد من الحالات التي تشكّل فيها دهون الأغشية سلوك الخلايا بصمت.
الاستشهاد: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
الكلمات المفتاحية: حمض الفسفاتيديك, توازن الدهون, بروتيوميات الأغشية, بروتينات نقل الدهون, تحرير الغشاء البصري الوراثي