Clear Sky Science · de
Membran‑Bearbeitung mit Proximity‑Labeling enthüllt Regulatoren der Lipid‑Homöostase
Wie Zellen ihre fetten Hüllen im Gleichgewicht halten
Jede Zelle in Ihrem Körper ist von einer dünnen Fett‑Hülle umgeben, der Membran. Diese Membranen sind mehr als einfache Barrieren: Ihre genaue Lipid‑Zusammensetzung steuert, wie Zellen wachsen, kommunizieren und auf Stress reagieren. Ein besonders wirkungsvolles Lipid, die Phosphatidsäure (PA), wirkt wie eine molekulare Alarmglocke. PA‑Schübe können wichtige Signalwege an‑ oder ausschalten, weshalb Zellen die PA‑Spiegel sehr schnell und sehr präzise erhöhen und senken müssen. Diese Studie zeigt, wie Zellen plötzliche PA‑Anstiege erkennen und bestimmte Proteine anwerben, um dieses potente Lipid wieder unter Kontrolle zu bringen.
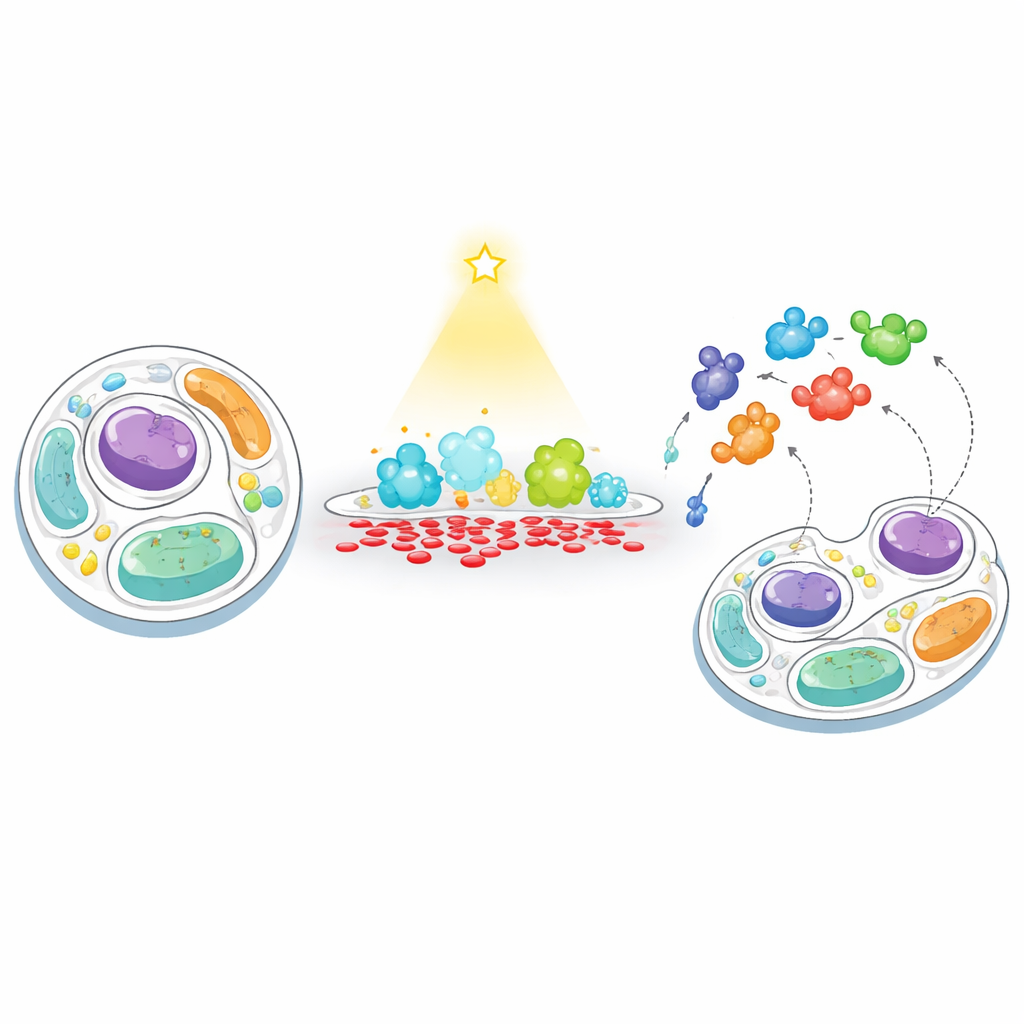
Eine neue Methode zum „Füttern“ und „Fischen“ in Zellmembranen
Die Forschenden entwickelten eine zweistufige Strategie, die sie „Füttern–Fischen“ nennen, um zu verfolgen, wie Zellen reagieren, wenn der PA‑Gehalt einer Membran künstlich aus dem Gleichgewicht gebracht wird. Zuerst „füttern“ sie eine ausgewählte Membran mit PA mittels eines lichtgesteuerten Enzyms, einer gentechnisch veränderten Phospholipase D, die sich auf Wunsch mit blauem Licht aktivieren lässt. Durch das Anvisieren dieses Enzyms entweder an die Zellaußenfläche oder an Lysosomen (die Recyclingzentren der Zelle) konnten sie kurze, lokal begrenzte PA‑Produktion auslösen. Dann „fischen“ sie nach in der Nähe befindlichen Proteinen, indem sie ein Biotin‑Markierenzym (TurboID) an dieselbe Membran anbringen. Jedes Protein, das sich nähert, wird markiert und später durch hochdurchsatzfähige Massenspektrometrie eingefangen und identifiziert, wodurch sichtbar wird, welche Proteine von PA‑reichen Regionen angezogen oder abgestoßen werden.
Wer taucht auf, wenn PA ansteigt?
Wenden die Forschenden diese Methode auf humane Zellen an, identifizieren sie Tausende von Proteinen in der Nähe der Plasmamembran und der Lysosomen und finden dann diejenigen, deren Häufigkeit sich bei erhöhtem PA ändert. Viele der stärksten Reaktanten waren bereits dafür bekannt, mit PA oder verwandten Lipiden umzugehen, was den Ansatz validiert. Enzyme namens Lipins, die PA in ein anderes Signallipid, Diacylglycerol (DAG), abbauen, waren auf PA‑beladenen Membranen angereichert, während ein DAG‑bildendes Enzym, das PA erzeugt, seltener auftauchte — ein Hinweis auf ein eingebautes Feedbacksystem. Das am besten bekannte PA‑Transferprotein Nir2 wanderte ebenfalls sowohl zur PA‑reichen Plasmamembran als auch zu Lysosomen, was seine zentrale Rolle beim Shuttle von PA zwischen Organellen unterstreicht. Die Analyse deckte zudem Veränderungen bei Proteinen auf, die mit Mitochondrien und Cholesterin‑Handhabung verknüpft sind, was nahelegt, dass PA‑Schübe viele Aspekte des Zellstoffwechsels beeinflussen.
Verborgene Kuriere, die PA bewegen und entfernen
Um zu testen, welche der rekrutierten Proteine tatsächlich helfen, überschüssiges PA zu entfernen, konzentrierten sich die Wissenschaftler auf mehrere Lipid‑Transferproteine — molekulare Kuriere, die Fette zwischen Membranen transportieren. Durch Überexpression dieser Kuriere und Verfolgung eines fluoreszenten PA‑Sensors fanden sie, dass Nir2 und ein Protein namens SCP2 die PA‑Anhäufung an Plasmamembran und Lysosomen deutlich verringerten. SCP2, zuvor bekannt für den Transport von Cholesterin und Fettsäuren, zeigte in einem gereinigten Liposomen‑Assay ebenfalls PA‑Trägeraktivität und erweiterte damit sein Aufgabenspektrum. Andere Transferproteine, darunter PDZD8 und TEX2, senkten PA nicht direkt, schienen aber die physischen Kontakte zwischen endoplasmatischem Retikulum und Lysosomen zu verstärken, was vermutlich hilft, Lipide zur weiteren Verarbeitung zu leiten. Im Gegensatz dazu führte ein Oxysterol‑bindendes Protein, ORP1L, unerwartet zu weiterem PA‑Anstieg — auf eine Weise, die von seiner Cholesterin‑Bindestelle abhängt — und deutet auf eine komplexere Wechselwirkung zwischen PA‑ und Cholesterinflüssen hin.
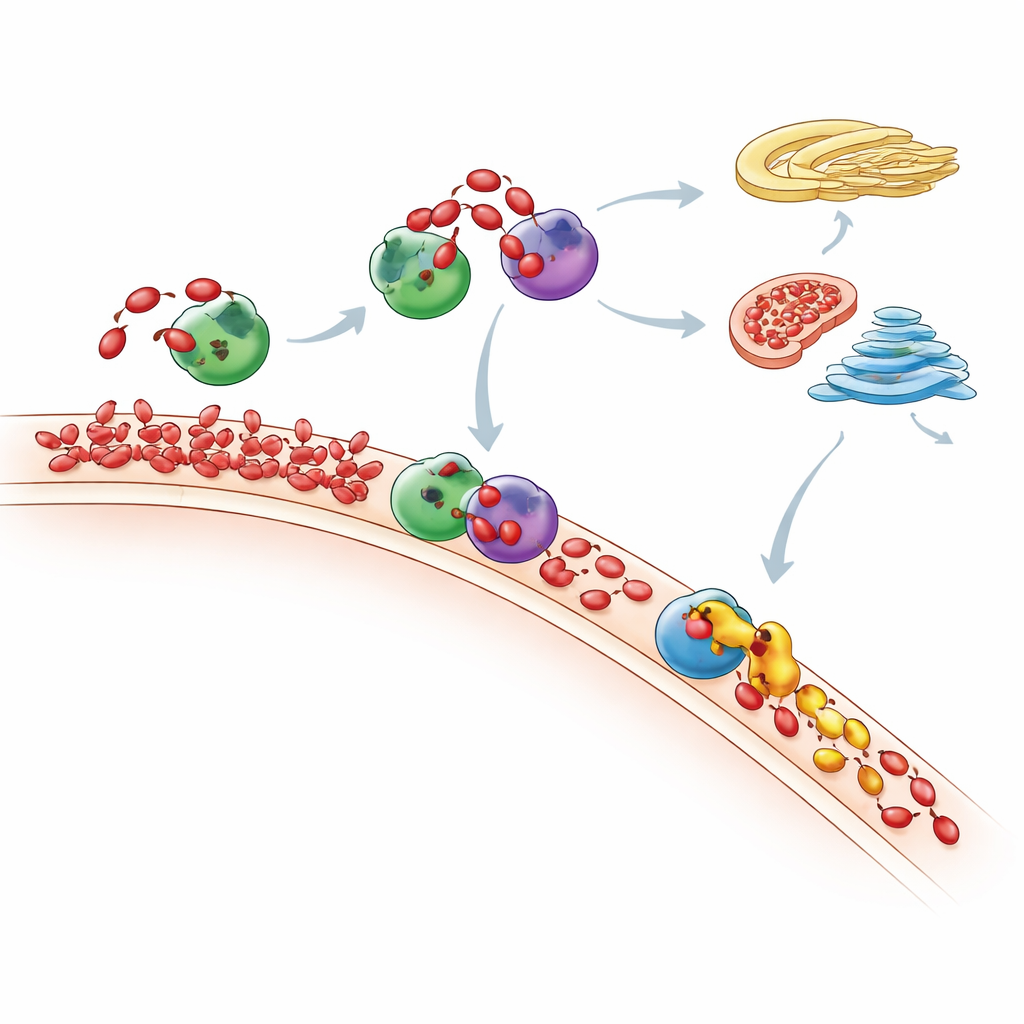
Wohin das zusätzliche PA schließlich gelangt
Mit sensibler Massenspektrometrie erfassten die Forschenden die gesamte Lipidlandschaft und verfolgten, wie sich die Phospholipid‑Zusammensetzung der Zelle nach dem PA‑„Füttern“ veränderte. Sie beobachteten, dass PA‑Spitzen kurzlebig sind: Im Laufe der Zeit werden viele PA‑Moleküle entweder in DAG und dann über den Kennedy‑Weg in gängige Membranlipide umgewandelt oder über den CDP‑DAG‑Weg in andere Lipide überführt. Mitochondrien scheinen eine Schlüsselrolle zu spielen: Ein Enzym namens TAMM41 hilft offenbar eingehendes PA in Phosphatidylglycerol umzuwandeln, einen Baustein für mitochondriale Membranen. Bei Depletion von Nir2 blieb neu synthetisiertes PA nicht mehr dort, wo es erzeugt wurde, sondern sammelte sich stattdessen im Golgi‑Bereich an — ein Befund, der zeigt, dass die Störung eines Kuriers den Lipidverkehr in der Zelle umlenken und wichtige Signalwege wie mTOR, einen zentralen Wachstumsregulator, verändern kann.
Warum diese Arbeit für die Zellgesundheit wichtig ist
Durch die Kombination präziser „Membran‑Bearbeitung“ mit Proximity‑Tagging liefert diese Studie einen leistungsfähigen Plan für die Entdeckung, wie Zellen Ungleichgewichte in ihrer Lipid‑Zusammensetzung erkennen und korrigieren. Für PA skizziert die Arbeit ein Netzwerk aus Enzymen und Transportproteinen, die zu überlasteten Membranen eilen, PA an sicherere Orte verlagern und es in andere Lipide umwandeln — und dabei zentrale Signalnetzwerke im Zaum halten. Da ähnliche Lipid‑Störungen mit Krebs, Stoffwechselerkrankungen und Neurodegeneration verknüpft sind, könnte der Füttern–Fischen‑Ansatz genutzt werden, um neue Wirkstoffziele in vielen Erkrankungen zu entdecken, in denen Membranlipide still und heimlich das Zellverhalten prägen.
Zitation: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Schlüsselwörter: phosphatidsäure, Lipid‑Homöostase, Membran‑Proteomik, Lipid‑Transportproteine, optogenetische Membran‑Bearbeitung