Clear Sky Science · es
Edición de membranas con etiquetado por proximidad revela reguladores de la homeostasis de lípidos
Cómo las células mantienen en equilibrio sus capas grasas
Cada célula de tu cuerpo está envuelta en una fina capa grasa llamada membrana. Estas membranas son más que simples barreras: su mezcla exacta de lípidos ayuda a controlar cómo las células crecen, se comunican y responden al estrés. Un lípido especialmente potente, el ácido fosfatídico (PA), actúa como una alarma molecular. Los picos de PA pueden activar o desactivar vías de señalización clave, por lo que las células deben elevar y reducir sus niveles de forma muy rápida y precisa. Este estudio revela cómo las células detectan aumentos bruscos de PA y reclutan proteínas específicas para devolver este lípido potente bajo control.
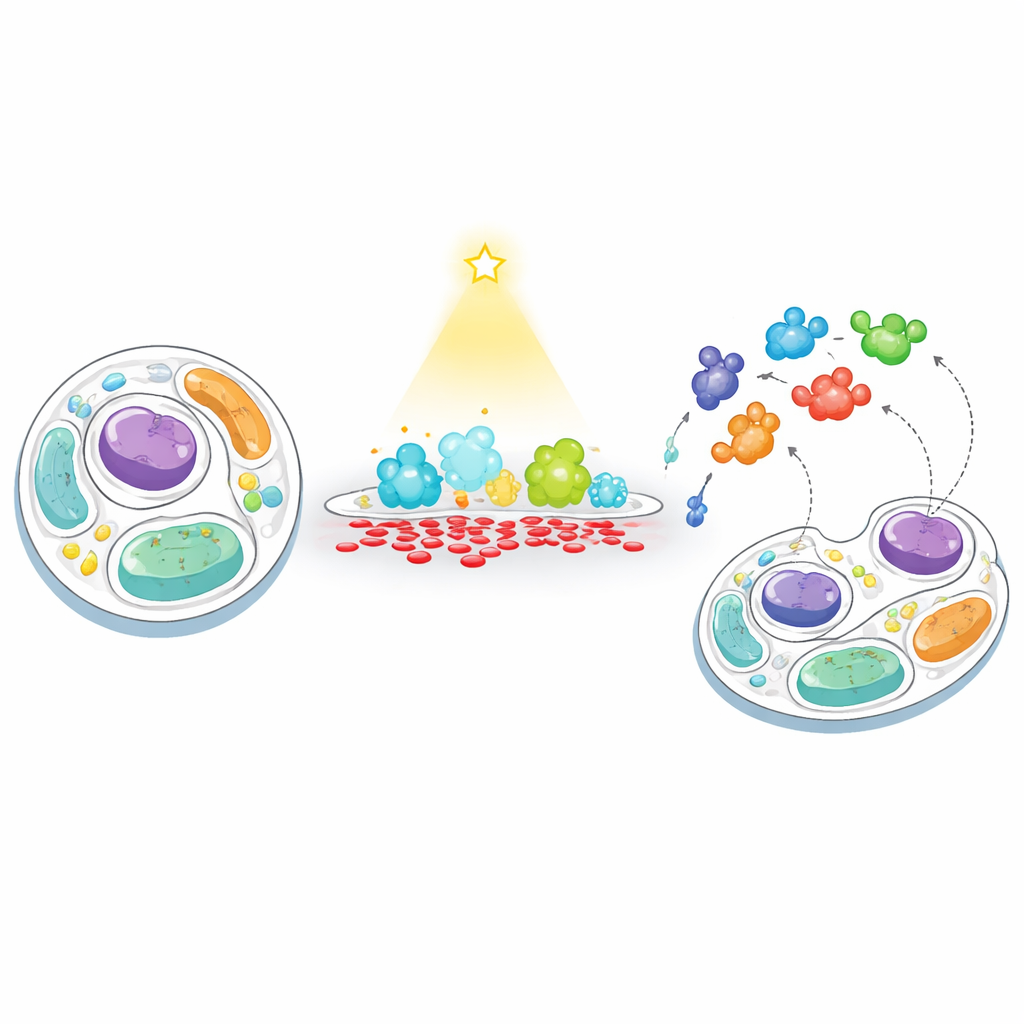
Una nueva manera de “alimentar” y “pescar” en las membranas celulares
Los investigadores desarrollaron una estrategia en dos pasos que llaman “alimentar–pescar” para seguir la respuesta celular cuando el nivel de PA en una membrana se desequilibra de forma artificial. Primero, “alimentan” una membrana elegida con PA usando una enzima controlada por luz, una versión diseñada de fosfolipasa D que puede activarse a voluntad con luz azul. Al dirigir esta enzima a la superficie externa de la célula o a los lisosomas (los centros de reciclaje celular), pudieron desencadenar ráfagas cortas y localizadas de producción de PA. Segundo, “pescan” proteínas cercanas adjuntando una enzima de marcado con biotina (TurboID) a la misma membrana. Cualquier proteína que pase por ahí queda etiquetada y luego se captura e identifica mediante espectrometría de masas de alto rendimiento, revelando qué proteínas son atraídas por las regiones ricas en PA o cuáles son repelidas.
¿Quién aparece cuando el PA aumenta?
Aplicando este método a células humanas, el equipo identificó miles de proteínas cerca de la membrana plasmática y de los lisosomas, y luego determinó cuáles cambiaban en abundancia cuando subían los niveles de PA. Muchos de los respondedores más fuertes ya eran conocidos por manejar PA o lípidos relacionados, validando el enfoque. Enzimas llamadas lipinas, que degradan PA a otro lípido señalizador, el diacilglicerol (DAG), se enriquecieron en membranas cargadas de PA, mientras que una enzima que fabrica DAG a partir de PA apareció con menos frecuencia, lo que sugiere un sistema de retroalimentación interno. La proteína de transferencia de PA más conocida, Nir2, también se desplazó tanto a membranas plasmáticas como a lisosomas ricas en PA, subrayando su papel central en el transporte de PA entre orgánulos. El análisis además reveló cambios en proteínas vinculadas con mitocondrias y el manejo del colesterol, lo que sugiere que los picos de PA repercuten en muchos aspectos del metabolismo celular.
Mensajeros ocultos que movilizan y eliminan PA
Para probar qué proteínas reclutadas ayudan realmente a eliminar el exceso de PA, los científicos se centraron en varias proteínas de transferencia de lípidos: mensajeros moleculares que mueven grasas entre membranas. Al sobreproducir estos mensajeros y seguir un sensor fluorescente de PA, encontraron que Nir2 y una proteína llamada SCP2 redujeron notablemente la acumulación de PA en la membrana plasmática y en los lisosomas. SCP2, conocida previamente por transportar colesterol y ácidos grasos, también mostró actividad de transporte de PA en un ensayo con liposomas purificados, ampliando su descripción funcional. Otras proteínas de transferencia, incluidas PDZD8 y TEX2, no disminuyeron directamente los niveles de PA pero parecieron reforzar los contactos físicos entre el retículo endoplásmico y los lisosomas, probablemente ayudando a encaminar lípidos para su posterior procesamiento. En contraste, una proteína unida a oxisteroles, ORP1L, provocó inesperadamente un aumento adicional de PA, de una manera dependiente de su sitio de unión al colesterol, lo que apunta a una comunicación más compleja entre los flujos de PA y colesterol.
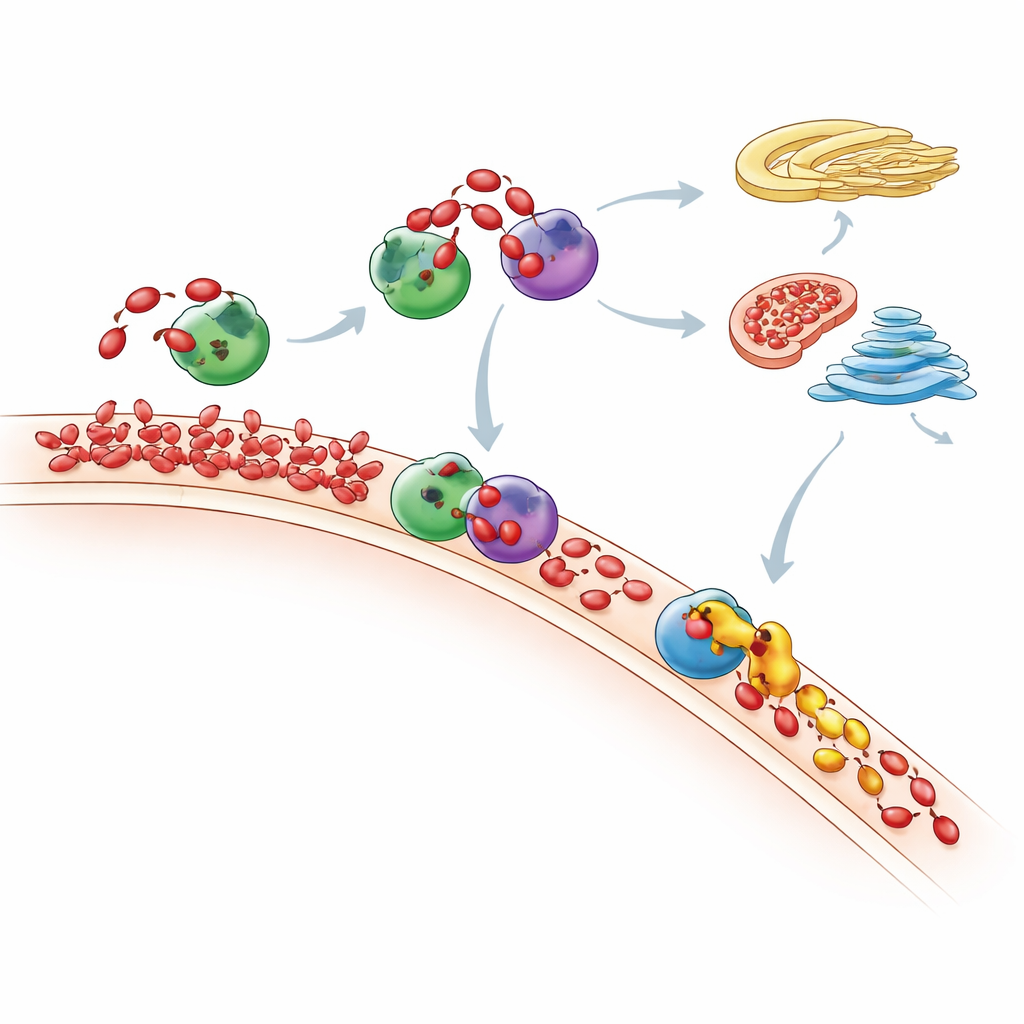
Hacia dónde acaba el PA extra
Midiendo el paisaje lipídico completo con espectrometría de masas sensible, los investigadores siguieron cómo cambiaba la mezcla total de fosfolípidos de la célula tras la “alimentación” con PA. Observaron que los picos de PA son de corta duración: con el tiempo, muchas moléculas de PA se convierten bien en DAG y luego en lípidos de membrana comunes a través de la vía de Kennedy, o bien en otros lípidos mediante la ruta CDP-DAG. Las mitocondrias parecen jugar un papel clave, usando una enzima llamada TAMM41 para ayudar a convertir el PA entrante en fosfatidilglicerol, un bloque de construcción para las membranas mitocondriales. Cuando Nir2 se agotó, el PA recién formado dejaba de permanecer donde se producía y se acumuló en la región del Golgi, mostrando que alterar un mensajero puede desviar el tráfico lipídico por la célula y alterar vías de señalización importantes como mTOR, un regulador principal del crecimiento.
Por qué este trabajo importa para la salud celular
Al combinar una “edición de membranas” precisa con el etiquetado por proximidad, este estudio ofrece un plano poderoso para descubrir cómo las células detectan y corrigen desequilibrios en su composición lipídica. Para el PA, el trabajo mapea una red de enzimas y proteínas de transporte que acuden a las membranas sobrecargadas, llevan el PA a lugares más seguros y lo transforman en otros lípidos, todo mientras mantienen en jaque circuitos de señalización clave. Dado que perturbaciones lipídicas similares se asocian con cáncer, enfermedades metabólicas y neurodegeneración, el enfoque alimentar–pescar podría usarse para descubrir nuevos objetivos farmacológicos en muchas condiciones donde los lípidos de membrana influyen de manera silenciosa en el comportamiento celular.
Cita: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Palabras clave: ácido fosfatídico, homeostasis de lípidos, proteómica de membranas, proteínas de transferencia de lípidos, edición de membranas optogenética