Clear Sky Science · ru
Редактирование мембраны с помощью проксимити-маркировки выявляет регуляторы липидного гомеостаза
Как клетки поддерживают баланс своих жировых покровов
Каждая клетка вашего тела окружена тонкой жировой оболочкой, называемой мембраной. Эти мембраны — не просто барьеры: их точный состав липидов помогает регулировать рост клеток, их коммуникацию и реакцию на стресс. Один особенно мощный липид — фосфатидная кислота (ФК, PA) — действует как молекулярный сигнал тревоги. Всплески ФК могут включать или выключать ключевые сигнальные пути, поэтому клетки должны очень быстро и точно повышать и понижать её уровни. В этом исследовании показано, как клетки ощущают внезапные выбросы ФК и привлекают определённые белки, чтобы вернуть этот мощный липид под контроль.
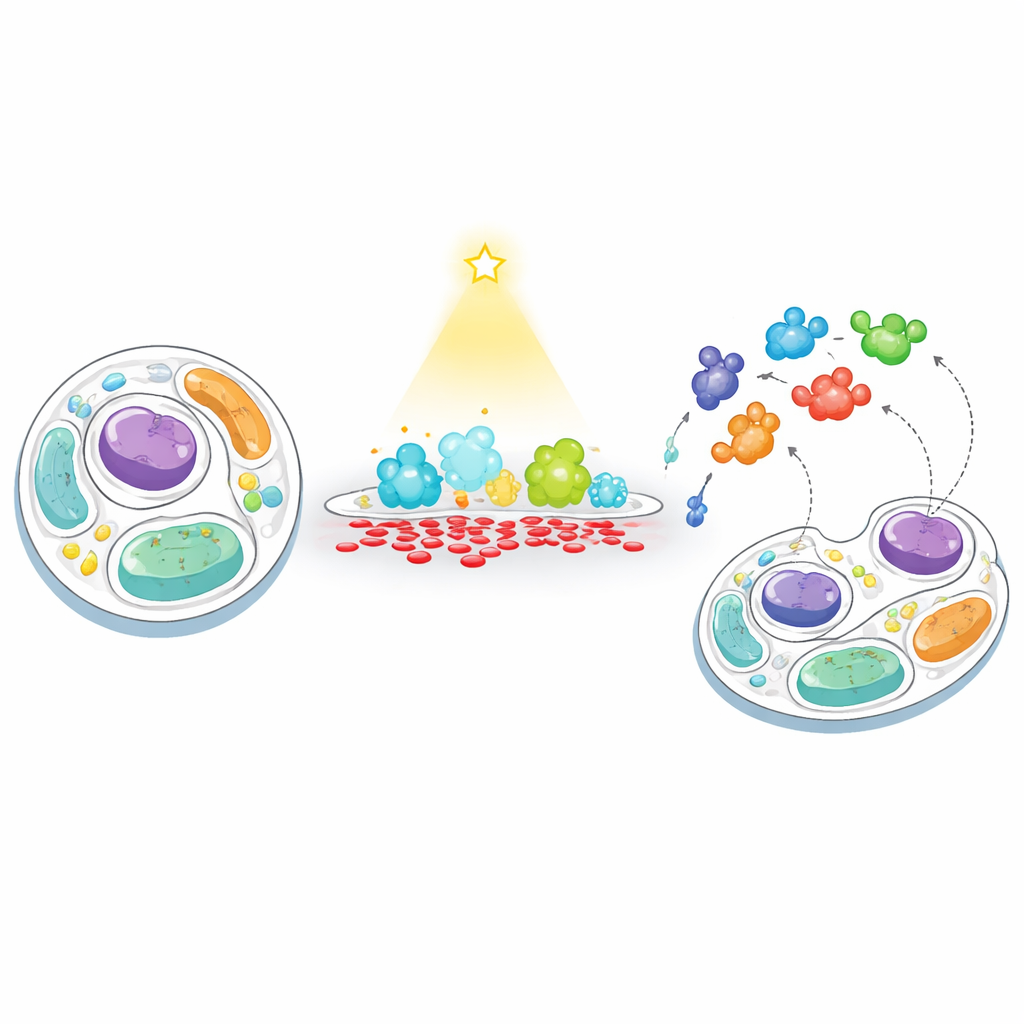
Новый способ «накормить» и «половить» в мембранах клеток
Исследователи разработали двухэтапную стратегию, которую они называют «накормить–половить», чтобы отследить, как клетки реагируют, когда уровень ФК в мембране искусственно выводят из равновесия. Сначала они «кормят» выбранную мембрану ФК с помощью управляемого светом фермента — инженерной версии фосфолипазы D, которую можно включать синим светом по желанию. Направляя этот фермент либо на поверхность клеточной мембраны, либо на лизосомы (центр утилизации клетки), они могли вызывать короткие локальные всплески производства ФК. Затем они «ловят» близлежащие белки, прикрепляя к той же мембране фермент для биотиновой метки (TurboID). Любой белок, оказавшийся рядом, маркируется, а затем извлекается и идентифицируется с помощью высокопропускной масс-спектрометрии, что показывает, какие белки притягиваются к регионам, богатым ФК, а какие — отталкиваются от них.
Кто появляется при всплесках ФК?
Применив этот метод к человеческим клеткам, команда выявила тысячи белков у плазматической мембраны и лизосом, затем выделила те, чья концентрация менялась при повышении уровней ФК. Многие из самых сильных откликов приходились на уже известных участников обмена ФК или родственных липидов, что подтверждает работоспособность подхода. Ферменты класса липинов, которые разрушают ФК до другого сигнального липида — диацилглицерола (DAG), — обогащались на мембранах, насыщенных ФК, тогда как фермент, синтезирующий DAG из ФК, встречался реже, что намекает на встроенный механизм отрицательной обратной связи. Наилучше известный переносчик ФК, Nir2, также перемещался как к ФК-богатой плазматической мембране, так и к лизосомам, подчеркивая его центральную роль в переброске ФК между органеллами. Анализ также выявил изменения в белках, связанных с митохондриями и обменом холестерина, что говорит о том, что всплески ФК распространяют эффект на многие аспекты клеточного метаболизма.
Скрытые курьеры, которые перемещают и удаляют ФК
Чтобы проверить, какие из рекрутированных белков действительно помогают убирать избыток ФК, учёные сосредоточились на нескольких белках переноса липидов — молекулярных курьерах, переносящих жиры между мембранами. При переэкспрессии этих курьеров и наблюдении за флуоресцентным сенсором ФК они обнаружили, что Nir2 и белок SCP2 заметно уменьшают накопление ФК на плазматической мембране и в лизосомах. SCP2, ранее известный переносом холестерина и жирных кислот, также показал способность переносить ФК в чистом липосомном тесте, расширяя своё функциональное описание. Другие переносчики, включая PDZD8 и TEX2, не снижали уровни ФК напрямую, но, по-видимому, укрепляли физические контакты между эндоплазматическим ретикулумом и лизосомами, вероятно направляя липиды на дальнейшую переработку. Напротив, оксистерол-связывающий белок ORP1L неожиданно вызывал дополнительный рост ФК, и этот эффект зависел от его сайта связывания холестерина, что намекает на более сложное взаимодействие потоков ФК и холестерина.
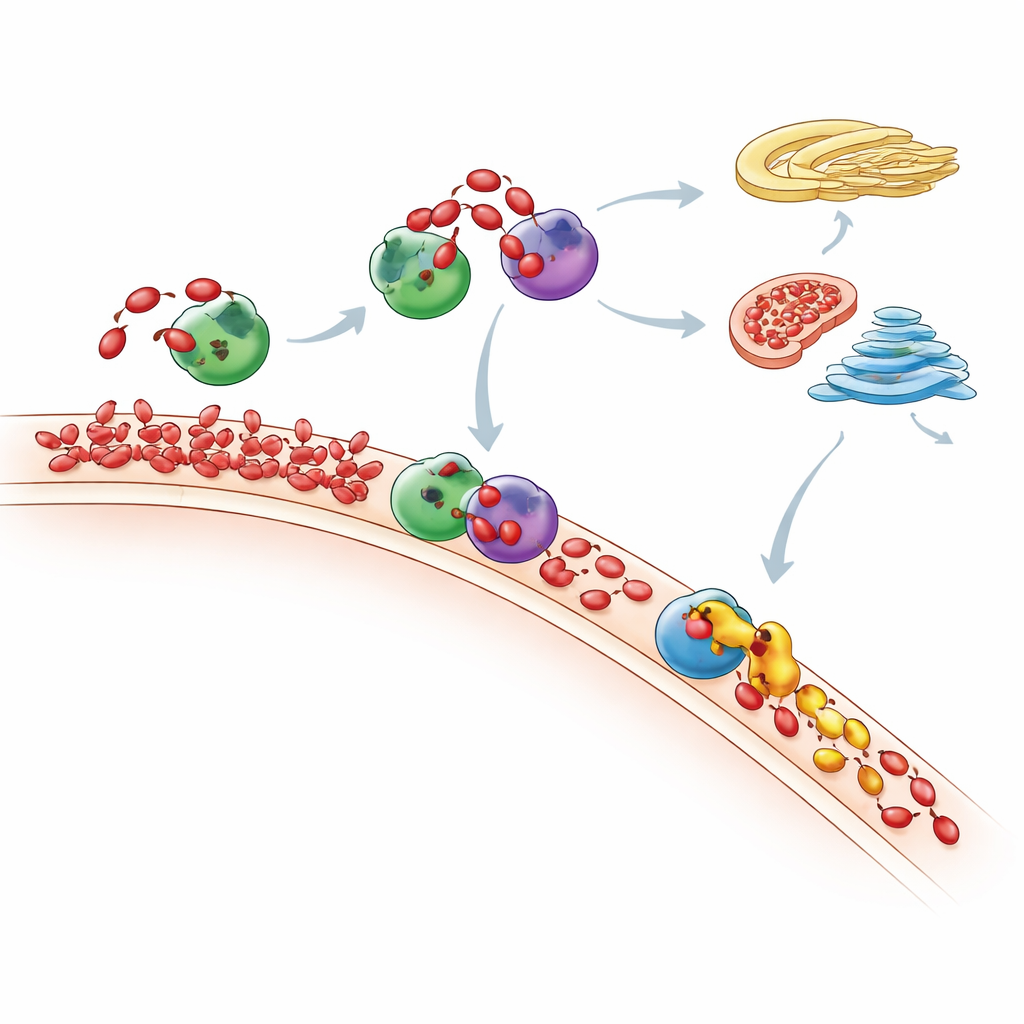
Куда в конечном итоге уходит лишняя ФК
Измеряя глобальный липидный ландшафт с помощью чувствительной масс-спектрометрии, исследователи проследили, как весь фосфолипидный состав клетки меняется после «кормления» ФК. Они обнаружили, что всплески ФК непродолжительны: со временем многие молекулы ФК конвертируются либо в DAG, а затем в обычные мембранные липиды через путём Кеннеди, либо в другие липиды через путь CDP-DAG. Митохондрии играют ключевую роль, используя фермент TAMM41 для превращения приходящей ФК в фосфатидилглицерин — строительный блок митохондриальных мембран. При истощении Nir2 вновь синтезированная ФК переставала оставаться в месте образования и вместо этого накапливалась в области аппарата Гольджи, показывая, что нарушение работы одного курьера может перенаправить липидный трафик по клетке и изменить важные сигнальные пути, такие как mTOR, крупный регулятор роста.
Почему эта работа важна для здоровья клеток
Комбинируя точное «редактирование мембран» с проксимити-маркировкой, это исследование даёт мощную схему для обнаружения того, как клетки обнаруживают и исправляют дисбалансы в своём липидном составе. Для ФК работа картирует сеть ферментов и переносчиков, которые устремляются к перегруженным мембранам, перемещают ФК в более безопасные места и превращают его в другие липиды, одновременно удерживая ключевые сигнальные цепи в равновесии. Поскольку похожие нарушения липидов связаны с раком, метаболическими заболеваниями и нейродегенерацией, подход «накормить–половить» может помочь выявить новые лекарственные мишени в ряде состояний, где мембранные липиды молча формируют поведение клеток.
Цитирование: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Ключевые слова: фосфатидная кислота, липидный гомеостаз, мембранная протеомика, белки переноса липидов, оптогенетическое редактирование мембран