Clear Sky Science · nl
Membraanbewerking met nabijheidslabeling onthult regelgevers van lipidenhomeostase
Hoe cellen hun vette jassen in evenwicht houden
Elke cel in je lichaam is omhuld door een dunne, vettige laag die een membraan wordt genoemd. Deze membranen zijn meer dan louter barrières: hun precieze samenstelling van lipiden helpt bepalen hoe cellen groeien, communiceren en reageren op stress. Eén bijzonder krachtig lipide, fosfatidzuur (PA), werkt als een moleculaire alarmbel. Pieken in PA kunnen belangrijke signaalroutes aan- of uitzetten, dus cellen moeten de niveaus snel en precies kunnen verhogen en verlagen. Deze studie laat zien hoe cellen plotselinge stijgingen in PA waarnemen en specifieke eiwitten aantrekken om dit krachtige lipide weer onder controle te krijgen.
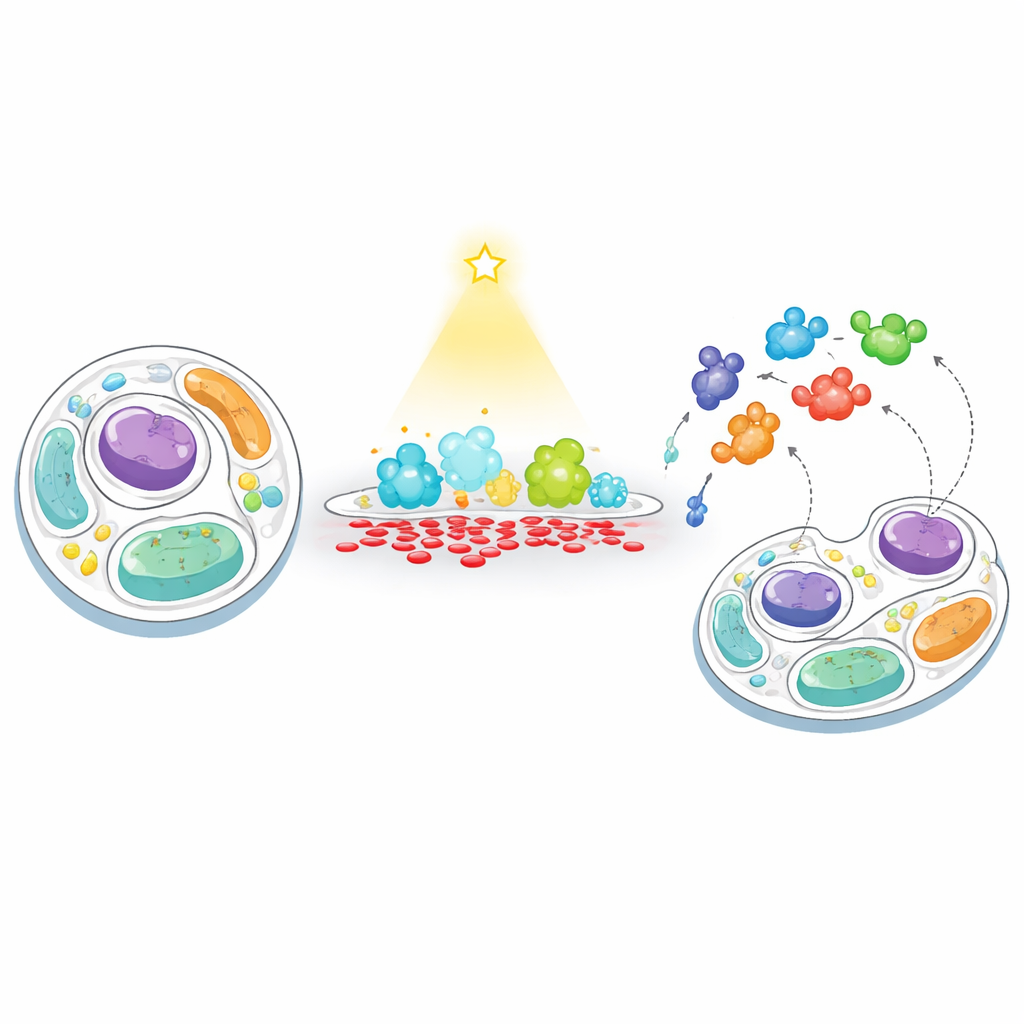
Een nieuwe manier om in membranen te “voeden” en te “vissen”
De onderzoekers ontwikkelden een twee-stappenstrategie die zij “voeden–vissen” noemen om te volgen hoe cellen reageren wanneer het PA-niveau van een membraan kunstmatig uit balans wordt gebracht. Eerst “voeden” ze een gekozen membraan met PA met behulp van een lichtgestuurde enzym, een gemodificeerde versie van fosfolipase D die op commando met blauw licht kan worden ingeschakeld. Door dit enzym te richten op óf het buitenoppervlak van de cel óf op lysosomen (de recyclingcentra van de cel), konden ze korte, gelokaliseerde pieken van PA-productie veroorzaken. Ten tweede “vissen” ze naar nabije eiwitten door een biotinerend enzym (TurboID) aan hetzelfde membraan te koppelen. Elk eiwit dat in de buurt komt, wordt gemerkt en later gevangen en geïdentificeerd met hoogdoorvoer massaspectrometrie, waarmee wordt onthuld welke eiwitten worden aangetrokken tot, of juist weggehouden van, PA-rijke regio's.
Wie verschijnt er als PA piekt?
Toegepast op menselijke cellen identificeerde het team duizenden eiwitten nabij het plasmamembraan en de lysosomen, en vervolgens diegenen waarvan de aanwezigheid veranderde toen de PA-niveaus stegen. Veel van de sterkste responders waren al bekend als spelers in PA- of verwante lipidenverwerking, wat de aanpak valideert. Enzymen genaamd lipinen, die PA afbreken naar een ander signaallipide, diacylglycerol (DAG), waren verrijkt op PA-beladen membranen, terwijl een DAG-producerend enzym dat PA produceert minder vaak voorkwam, wat wijst op een ingebouwd terugkoppelingssysteem. Het best bekende PA-transporteiwit, Nir2, verschoof ook naar zowel PA-rijke plasmamembranen als lysosomen, wat zijn centrale rol bij het shuttelen van PA tussen organellen onderstreept. De analyse toonde verder wijzigingen in eiwitten verbonden met mitochondriën en cholesterolhuishouding, wat suggereert dat PA-pieken een stempel drukken op veel aspecten van de celstofwisseling.
Verborgen koeriers die PA verplaatsen en verwijderen
Om te testen welke aangetrokken eiwitten daadwerkelijk helpen overtollige PA te verwijderen, richtten de wetenschappers zich op meerdere lipidetransporteiwitten—moleculaire koeriers die vetten tussen membranen verplaatsen. Door deze koeriers te overproduceren en een fluorescerende PA-sensor te volgen, ontdekten ze dat Nir2 en een eiwit genaamd SCP2 de PA-ophoping bij het plasmamembraan en de lysosomen duidelijk verminderden. SCP2, eerder bekend om het verplaatsen van cholesterol en vetzuren, toonde ook PA-transportactiviteit in een gezuiverde liposoomassay, waarmee zijn takenpakket werd uitgebreid. Andere transporteiwitten, waaronder PDZD8 en TEX2, verlaagden PA-niveaus niet direct maar leken de fysieke contacten tussen het endoplasmatisch reticulum en lysosomen te versterken, wat waarschijnlijk helpt lipiden voor verdere verwerking te routeren. Daarentegen veroorzaakte een oxysterol-bindend eiwit, ORP1L, onverwacht een verdere stijging van PA, op een manier die afhing van zijn cholesterolbindingsplaats, wat wijst op een complexere wisselwerking tussen PA- en cholesterolstromen.
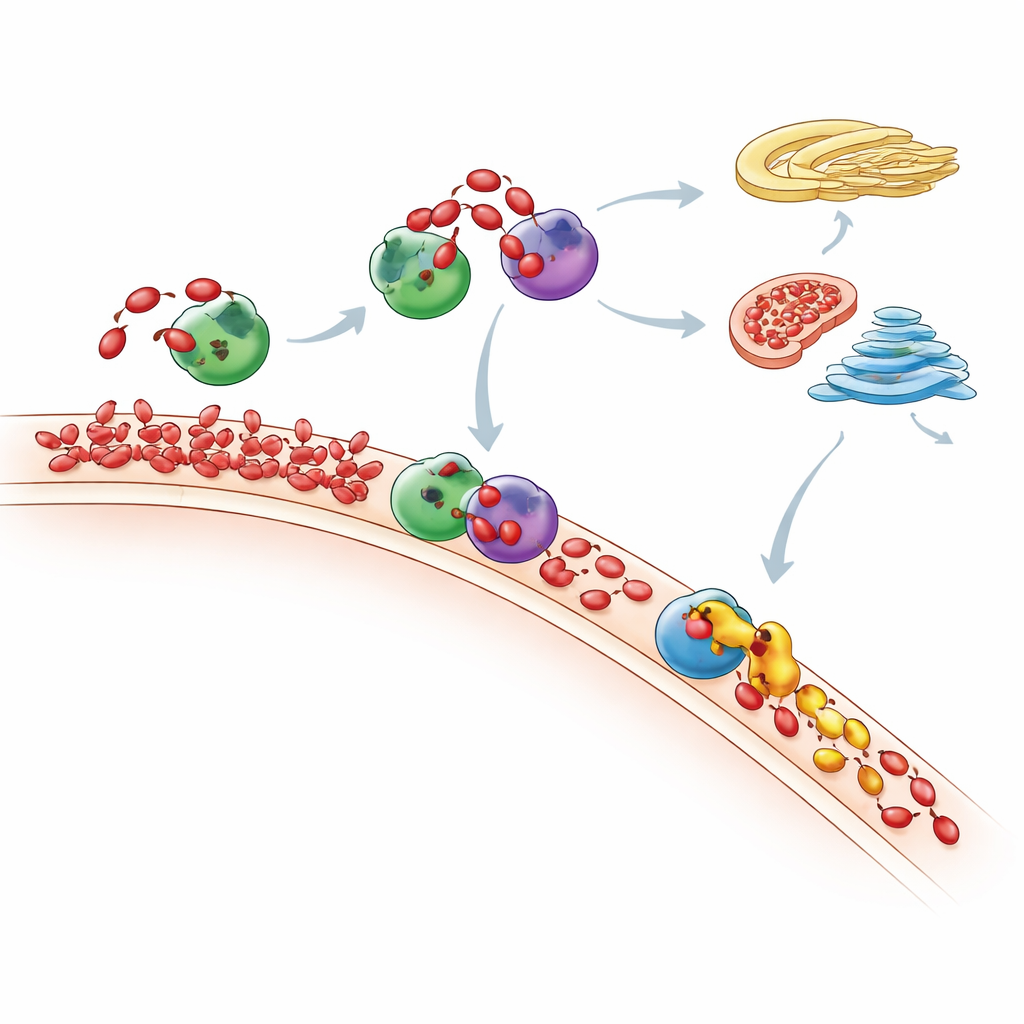
Waar extra PA uiteindelijk naartoe gaat
Met gevoelige massaspectrometrie maten de onderzoekers het volledige lipidenlandschap en volgden hoe de algehele fosfolipidemix van de cel veranderde na PA-“voeding.” Ze zagen dat PA-pieken van korte duur zijn: na verloop van tijd worden veel PA-moleculen óf omgezet in DAG en vervolgens in veelvoorkomende membraanlipiden via de Kennedy-route, óf in andere lipiden via het CDP-DAG-pad. Mitochondriën lijken een sleutelrol te spelen en gebruiken een enzym genaamd TAMM41 om binnenkomende PA te helpen omzetten naar fosfatidylglycerol, een bouwsteen voor mitochondriale membranen. Wanneer Nir2 werd uitgeput, bleef nieuwgemaakt PA niet op de plaats van productie maar stapelde het zich op in het Golgi-gebied, wat laat zien dat het verstoren van één koerier het lipideverkeer door de cel kan omleiden en belangrijke signaalroutes zoals mTOR, een belangrijke groeiregulator, kan veranderen.
Waarom dit werk van belang is voor celgezondheid
Door precieze “membraanbewerking” te combineren met nabijheidslabeling biedt deze studie een krachtig stappenplan om te ontdekken hoe cellen onevenwichtigheden in hun lipidenprofiel detecteren en corrigeren. Voor PA brengt het werk een netwerk in kaart van enzymen en transporteiwitten die naar overbeladen membranen snellen, PA naar veiligere locaties verplaatsen en het omzetten in andere lipiden, terwijl cruciale signaalcircuits onder controle blijven. Omdat soortgelijke lipideverstoring in verband wordt gebracht met kanker, stofwisselingsziekten en neurodegeneratie, kan de voeden–vissen-aanpak worden gebruikt om nieuwe medicijntargets te ontdekken voor vele aandoeningen waarbij membraanlipiden stilletjes het celgedrag bepalen.
Bronvermelding: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Trefwoorden: fosfatidzuur, lipidenhomeostase, membraanproteomics, lipidetransporteiwitten, optogenetische membraanbewerking