Clear Sky Science · tr
Zamanlama etiketleme ile membran düzenlemesi, lipid homeostazisinin düzenleyicilerini ortaya çıkarıyor
Hücreler Yağlı Kapaklarını Nasıl Dengede Tutuyor
Vücudunuzdaki her hücre, membran adı verilen ince, yağlı bir katmanla çevrilidir. Bu membranlar basit birer bariyerden daha fazlasıdır: lipidlerinin kesin bileşimi hücrelerin nasıl büyüdüğünü, iletişim kurduğunu ve strese nasıl yanıt verdiğini kontrollemeye yardımcı olur. Özellikle etkili bir lipid olan fosfatidik asit (PA), moleküler bir alarm zili gibi davranır. PA patlamaları kritik sinyal yollarını açıp kapatabilir, bu yüzden hücreler onun seviyelerini çok hızlı ve çok hassas biçimde yükseltip düşürmelidir. Bu çalışma, hücrelerin PA’daki ani artışları nasıl algıladığını ve bu güçlü lipidi kontrol altına almak için hangi spesifik proteinleri seferber ettiklerini ortaya koyuyor.
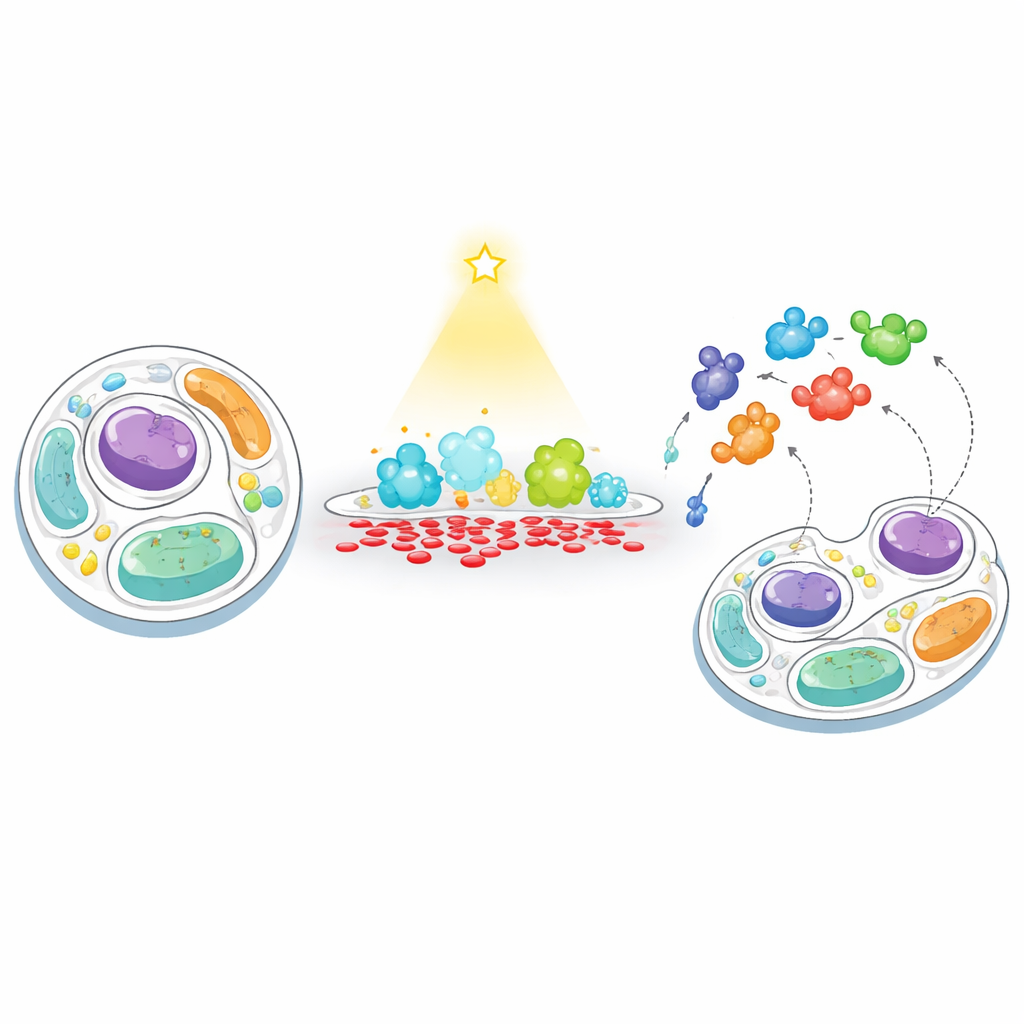
Hücre Membranlarında “Besleme” ve “Balık Tutma”nın Yeni Bir Yolu
Araştırmacılar, membranın PA seviyesinin yapay olarak dengesizleştirildiği durumda hücrelerin nasıl yanıt verdiğini izlemek için “besleme–balık tutma” adını verdikleri iki aşamalı bir strateji geliştirdiler. Önce, mavi ışıkla istenildiğinde açılıp kapanabilen mühendislik ürünü bir fosfolipaz D enzimi kullanarak seçilen bir membranı PA ile “beslediler”. Bu enzimi hücrenin dış yüzeyine ya da lizozomlara (hücrenin geri dönüşüm merkezleri) yönlendirerek, kısa ve lokalize PA üretimi patlamaları tetikleyebildiler. İkinci olarak, aynı membrana bir biotin etiketleme enzimi (TurboID) bağlayarak yakınlardaki proteinleri “balık tutarak” yakaladılar. Yakına gelen herhangi bir protein etiketleniyor, ardından yüksek verimli kütle spektrometrisiyle yakalanıp tanımlanarak hangi proteinlerin PA bakımından zengin bölgelere çekildiği veya bu bölgelerden uzaklaştığı ortaya kondu.
PA Zirvelendiğinde Kimler Ortaya Çıkıyor?
Bu yöntemi insan hücrelerine uygulayan ekip, plazma membranı ve lizozomların yakınındaki binlerce proteini belirleyip PA seviyeleri yükseldiğinde bollukları değişenleri saptadı. En güçlü yanıt verenlerin birçoğu PA veya ilişkili lipidlerle başa çıktıkları daha önce bilinen proteinlerdi; bu da yaklaşımı doğruladı. PA’yı diasilgliserole (DAG) dönüştüren lipinler, PA ile yüklü membranlarda zenginleşirken, PA üreten DAG yapıcı bir enzim daha az bulundu; bu durum yerleşik bir geri besleme sistemine işaret ediyor. En bilinen PA taşıyıcı proteini Nir2 de hem PA bakımından zengin plazma membranlarına hem de lizozomlara hareket etti; bu da organeller arasında PA taşınmasında merkezi rolünü vurguluyor. Analiz ayrıca mitokondri ve kolesterol işlemesiyle ilişkili proteinlerde değişimler gösterdi; bu da PA patlamalarının hücre metabolizmasının birçok yönünde dalgalar oluşturduğunu düşündürüyor.
PA’yı Taşıyan ve Gideren Gizli Kurye'ler
Araştırmacılar, hangi işe çağrılan proteinlerin fazladan PA’yı gerçekten temizlemeye yardımcı olduğunu test etmek için birkaç lipid taşıma proteinine—yağları membranlar arasında taşıyan moleküler kuryelere—odaklandı. Bu kuryeleri fazla üreterek ve floresan bir PA sensörünü izleyerek Nir2 ile SCP2 adlı bir proteinin plazma membranı ve lizozomlarda PA birikimini belirgin şekilde azalttığını buldular. Daha önce kolesterol ve yağ asitleri taşımayla bilinen SCP2, saflaştırılmış lipozom deneyinde PA taşıma aktivitesi de gösterdi; bu da iş tanımını genişletiyor. PDZD8 ve TEX2 dahil diğer taşıyıcı proteinler doğrudan PA seviyelerini düşürmedi, ancak endoplazmik retikulum ile lizozomlar arasındaki fiziksel temasları sıkılaştırarak lipitlerin daha sonra işlenmek üzere yönlendirilmesine yardımcı oluyor gibi görünüyordu. Buna karşılık, bir oksisterol-bağlayıcı protein olan ORP1L beklenmedik şekilde PA’nın daha da artmasına neden oldu; bu etki kolesterol bağlama bölgesine bağlıydı ve PA ile kolesterol akımları arasında daha karmaşık bir çift yönlü iletişime işaret ediyor.
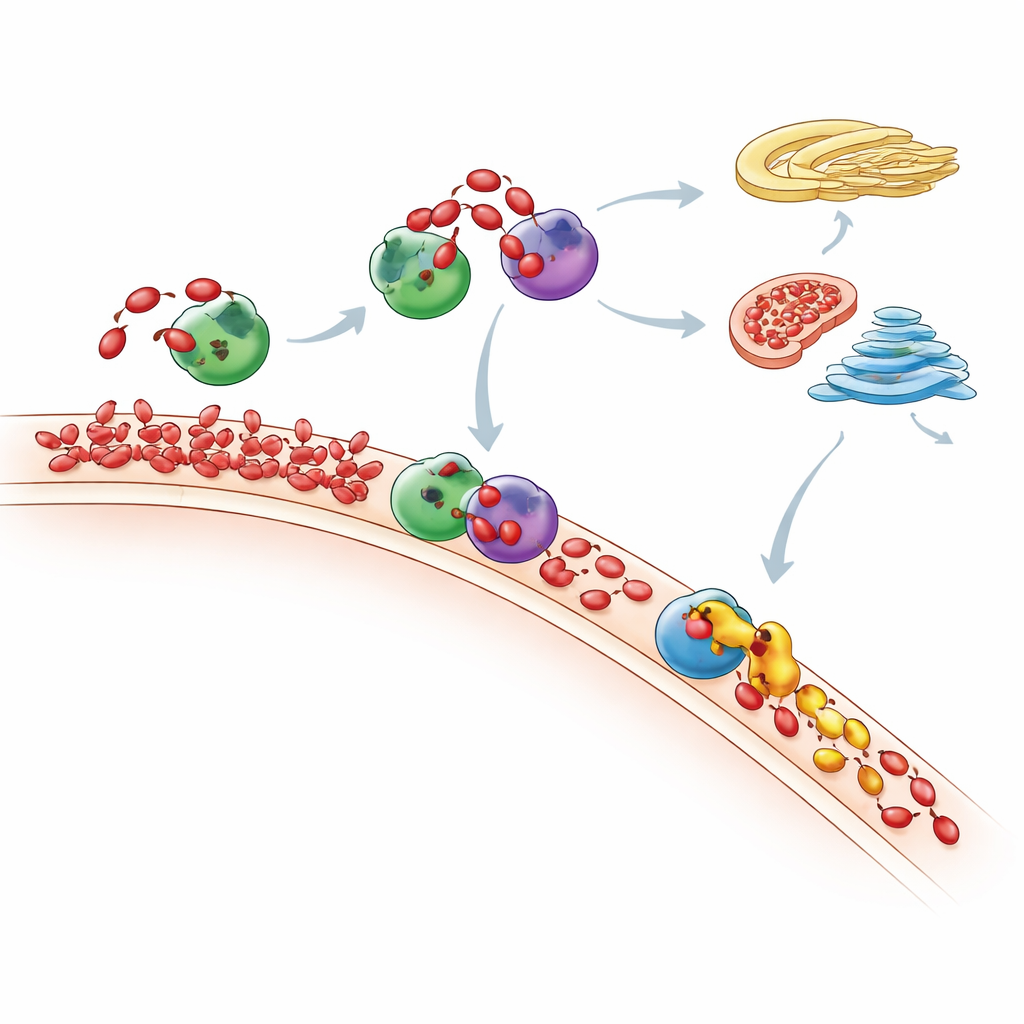
Fazladan PA Sonunda Nereye Gidiyor
Duyarlı kütle spektrometrisiyle tüm lipid manzarasını ölçen araştırmacılar, PA “beslemesinden” sonra hücrenin tüm fosfolipid karışımının nasıl değiştiğini izlediler. PA patlamalarının kısa ömürlü olduğunu gördüler: zamanla birçok PA molekülü ya DAG’a dönüştürülüp Kennedy yoluyla yaygın membran lipidlerine dönüştürülüyor ya da CDP-DAG rotası aracılığıyla diğer lipidlere dönüştürülüyordu. Mitokondriler gelen PA’yı fosfatidilgliserole dönüştürmeye yardımcı olan TAMM41 adlı bir enzim kullanarak önemli bir rol oynuyor gibi görünüyordu; bu lipid mitokondri membranlarının yapı taşıdır. Nir2 tükenince, yeni üretilen PA üretildiği yerde kalmadı; bunun yerine Golgi bölgesinde birikti; bu da bir kuryenin devre dışı kalmasının lipid trafiğini hücre içinde yeniden yönlendirebileceğini ve mTOR gibi önemli büyüme düzenleyici sinyal yollarını değiştirebileceğini gösteriyor.
Bu Çalışma Hücre Sağlığı İçin Neden Önemli
Hassas “membran düzenlemesi”ni yakınlık etiketlemeyle birleştirerek bu çalışma, hücrelerin lipid bileşimindeki dengesizlikleri nasıl algılayıp düzelttiğini keşfetmek için güçlü bir yol haritası sunuyor. PA için çalışma, aşırı yüklenmiş membranlara koşan, PA’yı daha güvenli yerlere taşıyan ve onu diğer lipidlere dönüştüren bir enzim ve taşıyıcı protein ağını haritalıyor; bunların hepsi anahtar sinyal devrelerini kontrol altında tutuyor. Benzer lipid bozukluklarının kanser, metabolik hastalık ve nörodejenerasyonla ilişkili olması nedeniyle, besleme–balık tutma yaklaşımı membran lipidlerinin hücre davranışını sessizce şekillendirdiği birçok durumda yeni ilaç hedeflerini ortaya çıkarmak için kullanılabilir.
Atıf: Tei, R., Li, XL., Luan, L. et al. Membrane editing with proximity labeling reveals regulators of lipid homeostasis. Nat Chem Biol 22, 728–739 (2026). https://doi.org/10.1038/s41589-025-02104-x
Anahtar kelimeler: fosfatidik asit, lipid homeostazisi, membran proteomikleri, lipid taşıyıcı proteinler, optogenetik membran düzenleme