Clear Sky Science · zh
活细胞中TRiC伴侣蛋白系统的单分子动力学
细胞如何让新生蛋白免于出错
你的细胞每秒合成数千个新蛋白——这些微小的分子工具必须折叠成恰当的构象才能发挥功能。折叠错误的蛋白会堵塞细胞机器,导致从神经退行性疾病到发育紊乱等多种疾病。本文在活的人类细胞中以单分子分辨率实时观察,记录主要折叠团队——TRiC伴侣蛋白及其辅助因子prefoldin——如何引导新生蛋白达到正确构象,以及在折叠失败时如何处置。
细胞质量控制小组在行动
在细胞内,称为伴侣蛋白的特殊帮助蛋白在蛋白合成和折叠过程中引导其他蛋白。TRiC是一个大型桶状复合体,可以暂时封闭不听话的蛋白链,而prefoldin是较小、触手状的复合体,负责将客户蛋白递送给TRiC。早期多数体外研究表明TRiC能折叠重要蛋白,如肌动蛋白和微管蛋白。但在拥挤熙攘的细胞内实情如何——TRiC和prefoldin与客户蛋白相遇的频率、停留时间以及在困难个案中的反应——一直不明朗。作者在活的人类细胞中开发了先进的单颗粒追踪显微技术,以跟踪单个TRiC和prefoldin分子及其与新生蛋白的相遇。
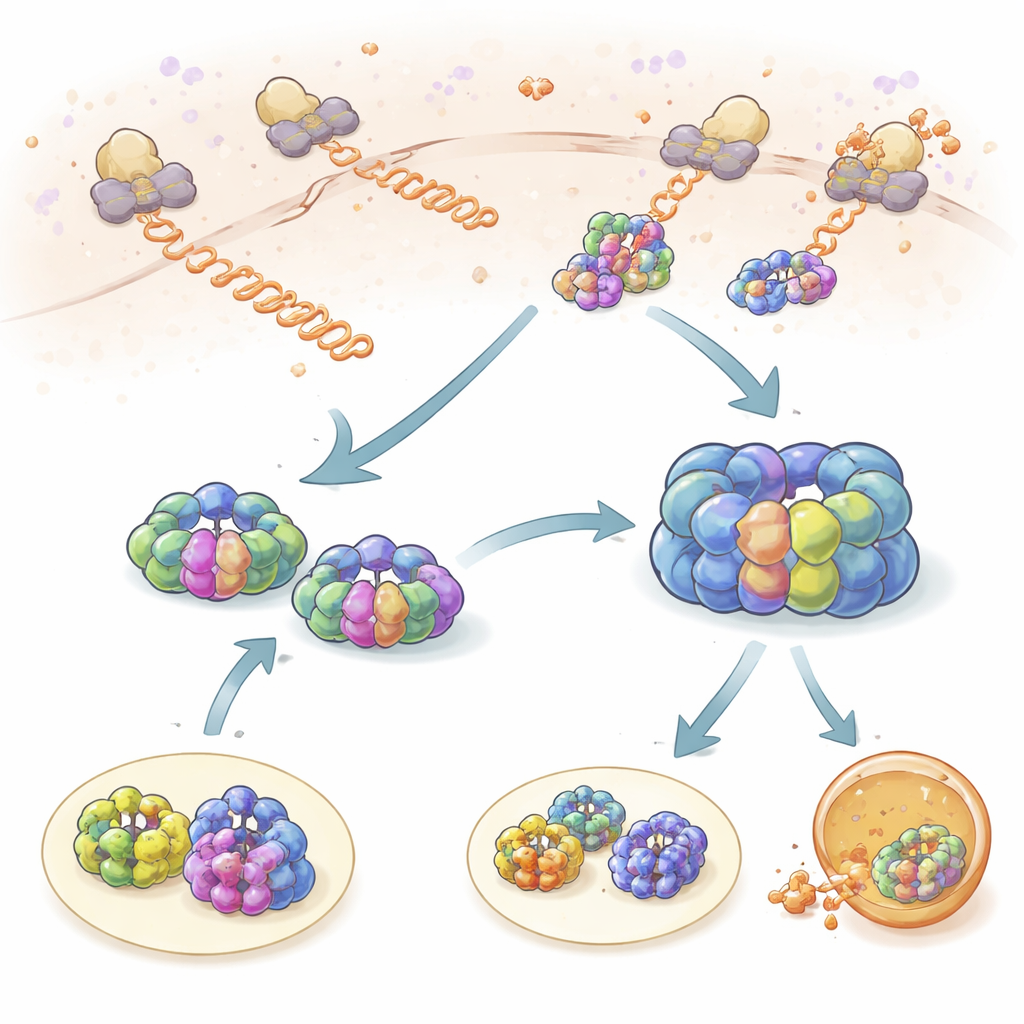
蛋白合成时的短暂检查
研究组首先观察TRiC和prefoldin如何与从核糖体——细胞的蛋白工厂——刚露头的新生多肽链相互作用。通过用不同荧光染料标记核糖体、TRiC和prefoldin,他们得以观察这些组分在时空上何时联动。TRiC和prefoldin都会以约一秒的短暂“探测”事件反复接触新生链。prefoldin接触新链的频率高于TRiC,降低prefoldin水平会显著减少TRiC对这些客户的接触,表明prefoldin起招募作用。通过核糖体测序分析,作者发现数百种不同蛋白以这种方式被监测,TRiC和prefoldin的客户高度重叠,强调了这一组合对维持健康蛋白群体的核心作用。
临近终点时的持续参与
为了聚焦单一的必需客户,研究者追踪了肌动蛋白——细胞骨架的关键构件。他们并未直接标记肌动蛋白,而是标记了其信使RNA,从而跟踪肌动蛋白合成的位点。随着肌动蛋白链逐渐增长,prefoldin和TRiC的访问频率和停留时间都增加。在翻译结束临近时,prefoldin常常结合数秒,握持接近完成的肌动蛋白链并帮助招募TRiC进入下一阶段折叠。当研究者人为将全长肌动蛋白锚定在靠近核糖体的位置时,他们观察到TRiC以约2.5秒为周期重复作用,这与多步折叠过程一致。prefoldin对于更长、更有效的TRiC结合至关重要,提示其不仅递送客户,还调节TRiC的工作方式。
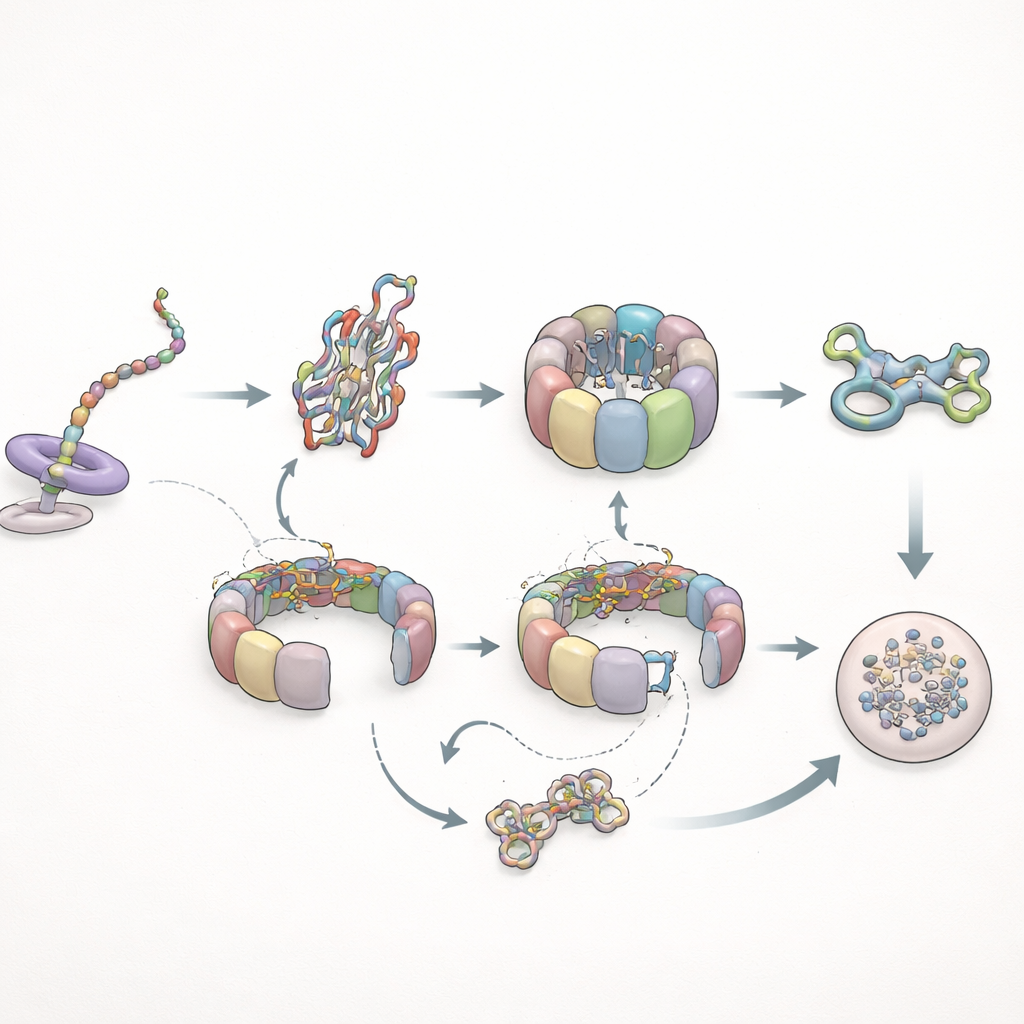
折叠失败时的循环与清理
作者随后测试了该系统如何处理有问题的客户:一种已知折叠不良的肌动蛋白突变体。在蛋白合成过程中,该突变体与TRiC的早期相互作用几乎正常,但未能出现健康蛋白那种延长的prefoldin接触,表明生长中的链的细微构象变化决定了prefoldin能保持结合的时间。合成结束后,情形发生了明显变化。突变肌动蛋白在TRiC上停留更久——可达正常停留时间的好几倍,并在伴侣蛋白内反复循环而未达到稳定的折叠态。最终,该突变体未能加入细胞结构网络,而是被移交给细胞的降解机制。同时,prefoldin的相互作用变得更频繁但更短暂,且其与TRiC的直接接触减少,这与TRiC围绕错误折叠客户更多处于闭合包裹状态相一致。
为折叠构建的局部保护区
一个显著的观察是,TRiC和prefoldin在结合轮次之间常常在客户附近逗留,而非扩散到细胞质的大范围中。释放蛋白后,TRiC通常在翻译位点周围的一个小区域内被限制最长可达两秒,然后重新结合同一条或相邻的链。作者还检测到依赖于持续蛋白合成的不同TRiC复合体之间的瞬时接触。这些行为共同支持“受保护折叠区”的概念——一类松散、动态的伴侣蛋白与翻译机器集群,新合成的蛋白被保持在靠近其帮助因子的区域,直到命运确定,从而避免有害相互作用。
对健康细胞与疾病的意义
简而言之,这项工作表明TRiC和prefoldin构成一对灵活的质量控制组合:它们短暂检查大量新合成的蛋白链,随着链接近完成而集中注意力,然后在核糖体周围的一个小局部“气泡”内快速运行折叠循环。像正常肌动蛋白这样的行为良好的蛋白通常在多次快速通过TRiC后达到正确构象。相反,缺陷变体会陷入延长循环并最终被引导向降解,同时占用伴侣蛋白的能力。这些单分子层面的见解有助于解释细胞在拥挤环境中如何应对持续的折叠风险,以及为什么客户蛋白或伴侣蛋白的突变会将平衡推向疾病方向。
引用: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
关键词: 蛋白质折叠, 分子伴侣蛋白, TRiC伴侣蛋白, 肌动蛋白动力学, 细胞蛋白稳态