Clear Sky Science · pl
Dynamika pojedynczych cząsteczek systemu chaperoniny TRiC in vivo
Jak komórki chronią nowe białka przed problemami
Co sekundę twoje komórki wytwarzają tysiące nowych białek — maleńkich narzędzi molekularnych, które muszą złożyć się w dokładnie właściwy kształt, by działać. Nieprawidłowo sfałdowane białka mogą zatykać wewnętrzne maszyny komórkowe i przyczyniać się do chorób, od neurodegeneracji po zaburzenia rozwojowe. W tym badaniu przyglądamy się żywym komórkom ludzkim na poziomie pojedynczych cząsteczek, aby na żywo obserwować, jak główny zespół odpowiadający za składanie — chaperonina TRiC i jej pomocnik prefoldyna — prowadzi nowe białka do właściwej struktury i decyduje, co robić, gdy składanie przebiega nieprawidłowo.
Zespół kontroli jakości w akcji
W naszych komórkach specjalne białka pomocnicze zwane chaperonami kierują innymi białkami podczas ich syntezy i fałdowania. TRiC to duży, baryłkowaty kompleks, który może tymczasowo zamykać niesforny łańcuch białkowy, podczas gdy prefoldyna to mniejszy kompleks o kształcie macki, dostarczający klienty do TRiC. Wcześniejsze prace, głównie in vitro, wykazały, że TRiC potrafi fałdować ważne białka, takie jak aktyna i tubulina. Jednak w zatłoczonym, tętniącym życiem wnętrzu prawdziwej komórki — jak często TRiC i prefoldyna spotykają swoich klientów, jak długo ich przytrzymują i jak reagują na trudne przypadki — pozostawało niejasne. Autorzy opracowali zaawansowaną mikroskopię śledzenia pojedynczych cząstek w żywych komórkach ludzkich, by obserwować pojedyncze cząsteczki TRiC i prefoldyny oraz ich spotkania z nowo powstającymi białkami.
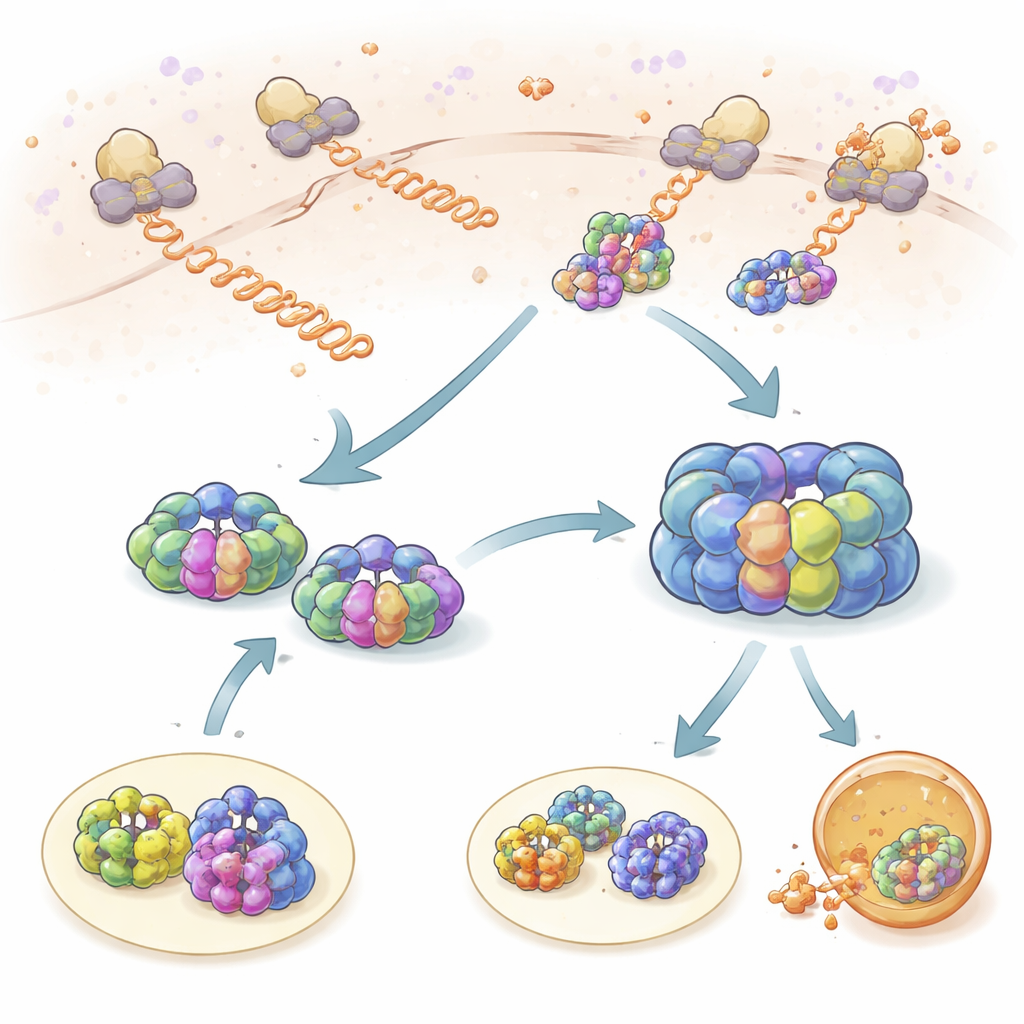
Krótkie kontrole w trakcie syntezy białek
Zespół najpierw przyjrzał się, jak TRiC i prefoldyna wchodzą w interakcje ze świeżo syntetyzowanymi łańcuchami białkowymi wychodzącymi z rybosomów, fabryk białek komórki. Oznaczając rybosomy, TRiC i prefoldynę różnymi barwnikami fluorescencyjnymi, mogli obserwować, kiedy ich ruchy stały się powiązane w przestrzeni i czasie. Zarówno TRiC, jak i prefoldyna wielokrotnie dotykały nowo powstających łańcuchów w krótkich „sondujących” zdarzeniach trwających około jednej sekundy. Prefoldyna kontaktowała nowe łańcuchy częściej niż TRiC, a obniżenie poziomu prefoldyny wyraźnie zmniejszało dostęp TRiC do tych klientów, co pokazuje, że prefoldyna działa jak rekruter. Dzięki profilowaniu rybosomów autorzy stwierdzili, że setki różnych białek są monitorowane w ten sposób, z silnym nakładaniem się klientów TRiC i prefoldyny, co podkreśla, że to partnerstwo jest kluczowe dla utrzymania zdrowej populacji białek.
Trwalsze zaangażowanie pod koniec syntezy
Aby przyjrzeć się uważniej pojedynczemu obowiązkowemu klientowi, badacze śledzili aktynę, kluczowy budulec cytoszkieletu komórki. Zamiast znakować białko aktyny bezpośrednio, opatrzyli jego mRNA, co pozwoliło śledzić miejsca, w których aktyna była syntetyzowana. W miarę wydłużania się łańcucha aktyny, zarówno prefoldyna, jak i TRiC odwiedzały częściej i pozostawały dłużej. Pod koniec translacji prefoldyna często wiązała się przez kilka sekund, przytrzymując niemal kompletne łańcuchy aktyny i pomagając w rekrutacji TRiC do następnej fazy fałdowania. Gdy badacze sztucznie tetherowali pełnej długości aktynę blisko rybosomu, mogli zaobserwować, że TRiC wchodzi z nią w powtarzające się cykle trwające około 2,5 sekundy każdy, co jest zgodne z wieloetapowym procesem fałdowania. Prefoldyna była kluczowa dla dłuższych, bardziej produktywnych zaangażowań TRiC, sugerując, że nie tylko dostarcza klientów, lecz także reguluje sposób działania TRiC.
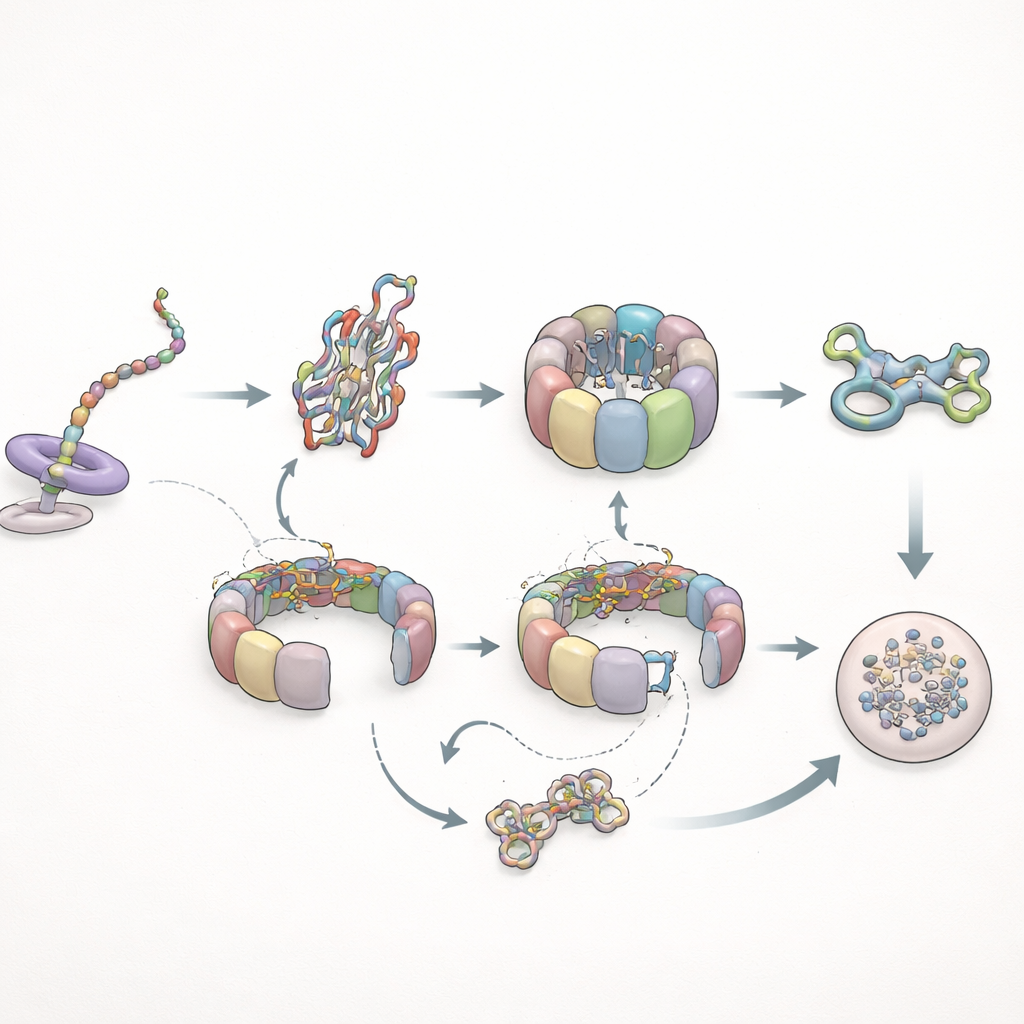
Gdy składanie zawodzi — cyklowanie i czyszczenie
Autorzy następnie przetestowali, jak system radzi sobie z problematycznym klientem: mutantną formą aktyny, która wiadomo, że źle się fałduje. Podczas syntezy białka ten mutant zachowywał się prawie normalnie względem TRiC, ale nie rozwijał wydłużonych kontaktów z prefoldyną widocznych dla zdrowej wersji, co wskazuje, że subtelne zmiany konformacyjne w rosnącym łańcuchu kontrolują, jak długo prefoldyna może go trzymać. Po syntezie historia zmieniła się dramatycznie. Mutantna aktyna pozostawała na TRiC znacznie dłużej — nawet kilka razy dłużej niż normalny czas pobytu — i cyklicznie przechodziła przez chaperoninę bez osiągnięcia stabilnej, sfałdowanej postaci. Ostatecznie, zamiast włączać się do strukturalnej sieci komórkowej, mutant został przekazany maszynerii degradacyjnej komórki. Równocześnie interakcje prefoldyny stały się częstsze, lecz krótsze, a jej bezpośrednie spotkania z TRiC zmalały, co jest zgodne z tym, że TRiC spędza więcej czasu w stanie zamkniętym, otaczającym źle sfałdowanego klienta.
Lokalna strefa ochronna dla fałdowania
Zauważalnym obserwowanym zjawiskiem było to, że TRiC i prefoldyna często przebywały w pobliżu swojego klienta między rundami wiązania, zamiast dyfundować z dala do masowej cytoplazmy. Po uwolnieniu białka TRiC zazwyczaj pozostawał ograniczony w niewielkim regionie wokół miejsca translacji przez okres do dwóch sekund, po czym ponownie wiązał ten sam lub sąsiedni łańcuch. Autorzy wykryli też przejściowe kontakty między różnymi kompleksami TRiC, zależne od trwającej syntezy białek. Razem te zachowania wspierają koncepcję „chronionej strefy fałdowania” — luźnej, dynamicznej skupiny chaperonów i maszynerii translacyjnej, w której nowo wytwarzane białka utrzymywane są blisko swoich pomocników i chronione przed szkodliwymi interakcjami, dopóki nie zostanie podjęta decyzja o ich losie.
Co to znaczy dla zdrowych komórek i chorób
Mówiąc prosto, ta praca pokazuje, że TRiC i prefoldyna działają jako zwinny duet kontroli jakości: krótko sprawdzają wiele nowych łańcuchów białkowych, koncentrują uwagę w miarę zbliżania się łańcucha do zakończenia, a następnie przeprowadzają szybkie cykle fałdowania w małej, lokalnej bańce wokół rybosomu. Dobrze rokujące białka, jak normalna aktyna, zazwyczaj osiągają prawidłową strukturę po wielokrotnych szybkich przejściach przez TRiC. Warianty wadliwe z kolei utkniają w przedłużonych cyklach i ostatecznie trafiają do degradacji, angażując przy tym zasoby chaperonów. Te obserwacje na poziomie pojedynczych cząsteczek pomagają wyjaśnić, jak komórki radzą sobie z ciągłym ryzykiem nieprawidłowego fałdowania w zatłoczonym środowisku i dlaczego mutacje w klientach lub chaperonach mogą przechylić równowagę w stronę choroby.
Cytowanie: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Słowa kluczowe: składanie białek, molekularne chaperony, chaperonina TRiC, dynamika aktyny, komórkowa proteostaza