Clear Sky Science · he
דינמיקה של מולקולה יחידה במערכת השפרונים TRiC בתאים חיים
איך תאים שומרים על חלבונים חדשים מבעיות
כל שנייה התאים שלכם מייצרים אלפי חלבונים חדשים — כלים מולקולריים זעירים החייבים להתקפל לצורה הנכונה כדי לתפקד. חלבונים מקופלים בצורה שגויה עלולים לחסום את המנגנונים התאיתיים ולתרום למחלות שמתחילות בהתנוונות עצבית ועד הפרעות בהתפתחות. עבודה זו מביטה בתוך תאים אנושיים חיים ברמת מולקולה יחידה כדי לצפות, בזמן אמת, כיצד צוות קיפול מרכזי בתא — השפרון TRiC ועוזרו פרפולדין — מנווטים חלבונים חדשים לצורה הנכונה ומחליטים מה לעשות כשהקיפול נכשל.
צוות בקרת איכות תאי בפעולה
בתוך תאים ישנם חלבונים מסייעים מיוחדים הקרויים שפרונים שמדריכים חלבונים אחרים בעת יצירתם וקיפולם. TRiC הוא קומפלקס גדול בצורת חבית שיכול לכלוא זמנית שרשרת חלבון מרדנית, בעוד פרפולדין הוא קומפלקס קטן עם מעין לולאות שמוביל לקוחות אל TRiC. מחקרים קודמים, בעיקר במבחנה, הראו ש-TRiC יכול לקפל חלבונים חשובים כגון אקטין וטובולין. אך מה מתרחש בסביבה הצפופה והרועשת של תא אמיתי — באיזו תדירות TRiC ופרפולדין פוגשים את לקוחותיהם, כמה זמן הם מחזיקים בהם, וכיצד הם מגיבים במקרים קשים — נותר לא ברור. החוקרים פיתחו מיקרוסקופיה מתקדמת למעקב אחר חלקיקים בודדים בתאים אנושיים חיים כדי לעקוב אחר מולקולות TRiC ופרפולדין בודדות והמפגשים שלהן עם חלבונים שזה עתה נוצרו.
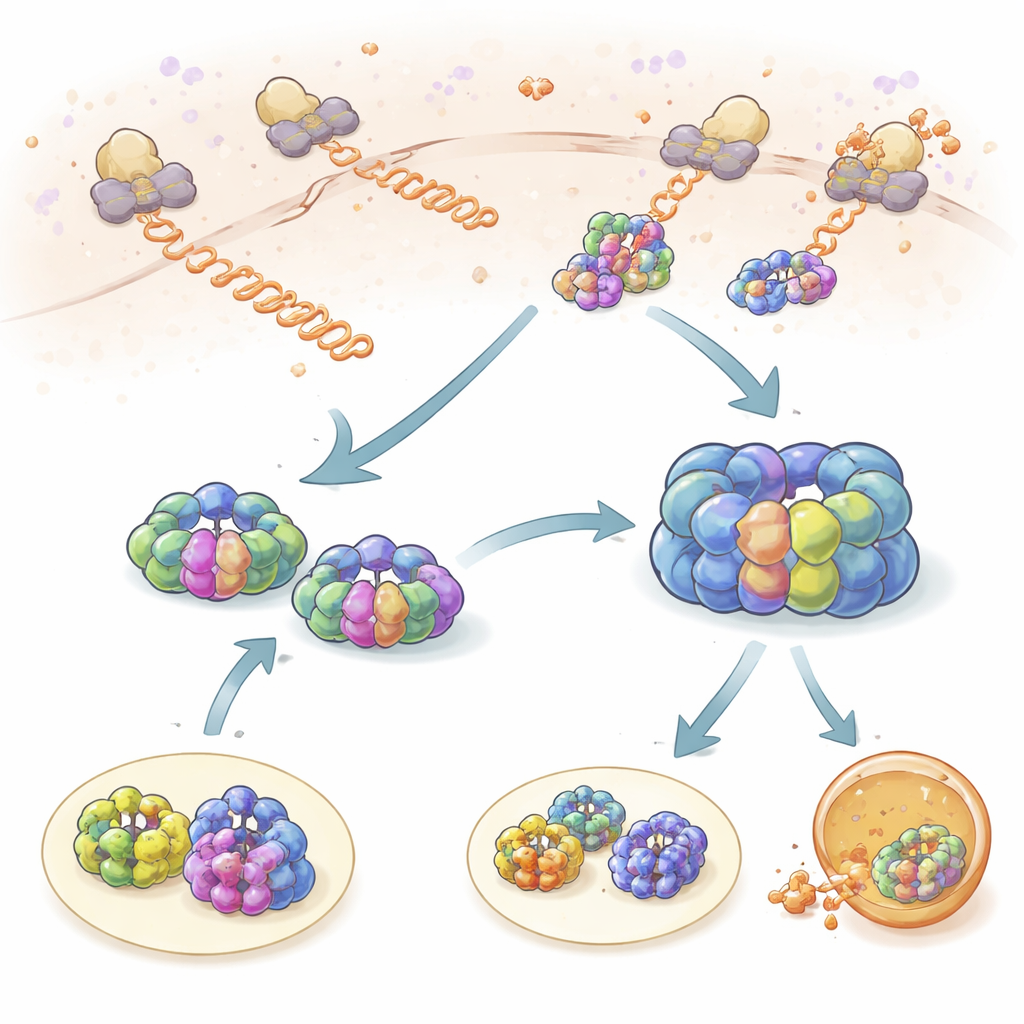
בדיקות קצרות בזמן הייצור של החלבון
הקבוצה בחנה ראשית כיצד TRiC ופרפולדין מתקשרים עם שרשראות חלבון שהורכבו זה עתה כאשר הן יוצאות מהריבוזומים, בתי החרושת לחלבון בתא. בעזרת תיוג של הריבוזומים, TRiC ופרפולדין בצבעי פלורסנציה שונים, יכלו לצפות מתי תנועתם הושוותה במרחב ובזמן. גם TRiC וגם פרפולדין נגעו בשרשראות נדירות באירועי "בדיקה" קצרים שנמשכו כנעילה שנייה. פרפולדין יצר מגע עם שרשראות חדשות בתדירות גבוהה יותר מ-TRiC, והפחתת רמות פרפולדין הקטינה באופן חד את הגישה של TRiC ללקוחות אלה, מה שמראה שפרפולדין פועל כמגייס. בעזרת פרופילינג של ריבוזומים מצאו המחברים שמאות חלבונים שונים מפוקחים בדרך זו, עם חפיפה חזקה בין לקוחות TRiC ופרפולדין, דבר המדגיש שהשותפות הזו חשובה לשמירה על בריאות מאגר החלבונים.
מעורבות ממושכת לקראת קו הסיום
כדי להתמקד בלקוח הכרחי יחיד, החוקרים עקבו אחרי אקטין, מרכיב מרכזי של שלד התא. במקום לתייג את חלבון האקטין ישירות, הם תייגו את ה-mRNA שלו, מה שאיפשר להם לעקוב אחרי האתרים שבהם אקטין נבנה. ככל ששרשרת האקטין התארכה, גם פרפולדין וגם TRiC ביקרו בתדירות גבוהה יותר והישארו זמן רב יותר. לקראת סוף התרגום, פרפולדין לעתים התקשר למשך כמה שניות, החזיק שרשראות אקטין כמעט שלמות וסייע במגייסות TRiC לשלב הבא של הקיפול. כאשר החוקרים קשרו באופן מלאכותי אקטין בעל אורך מלא בסמוך לריבוזום, הם יכלו לראות את מעורבות TRiC בחזרות שנמשכו כ-2.5 שניות כל אחת, בהתאם לתהליך קיפול רב-שלבי. פרפולדין היה קריטי למעורבויות הארוכות והפרודוקטיביות יותר של TRiC, מה שמרמז שהוא לא רק מספק לקוחות אלא גם מכוונן כיצד TRiC פועל.
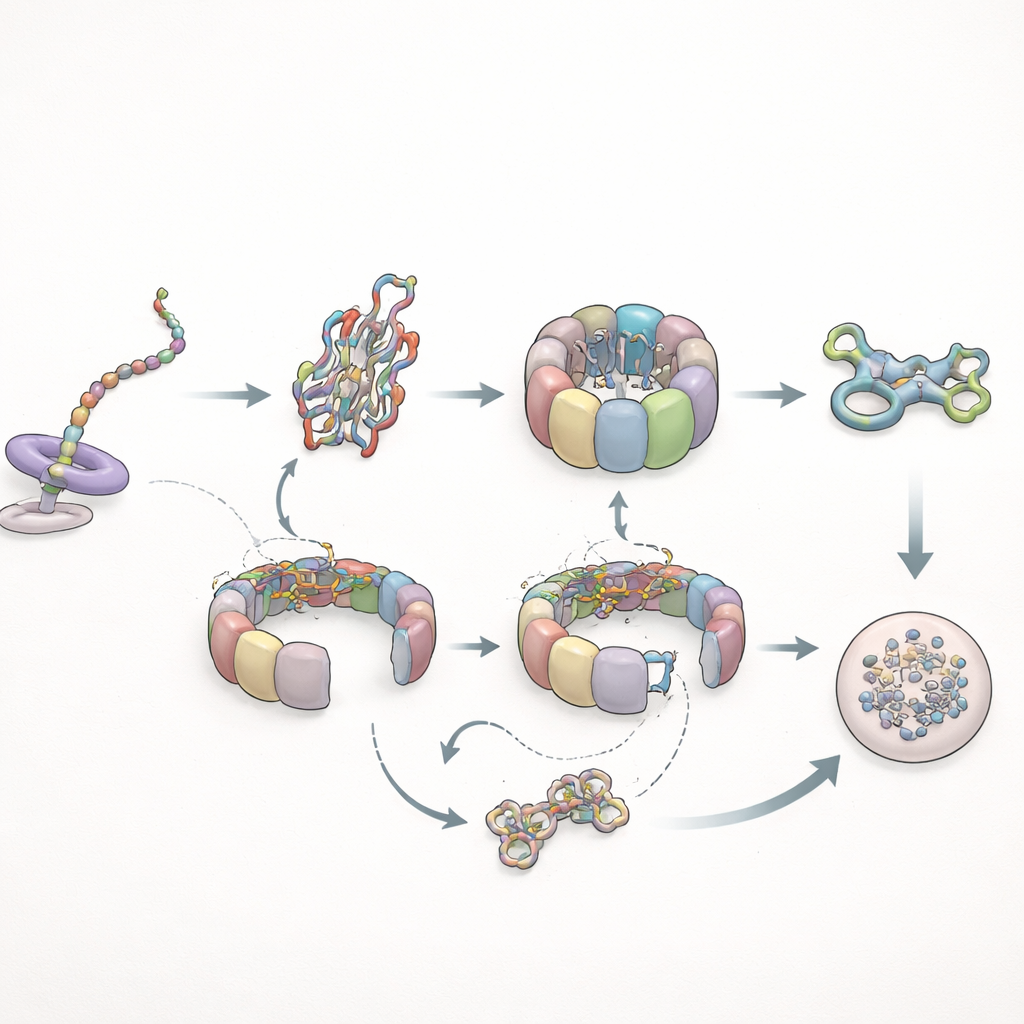
כשקיפול נכשל, מחזורים וניקוי
המחברים בחנו לאחר מכן כיצד המערכת מטפלת בלקוח בעייתי: צורת מוטנטית של אקטין הידועה בקיפולה הלקוי. במהלך הסינתזה, מוטנט זה התנהג כמעט כרגיל מול TRiC אך נכשל בפיתוח המגעים הממושכים עם פרפולדין שנצפו בגרסה הבריאה, דבר המעיד ששינויים קונפורמציוניים עדינים בשרשרת המתארכת קובעים כמה זמן פרפולדין יכול להחזיק. לאחר הסינתזה, התמונה השתנתה דרמטית. אקטין המוטנט נשאר על TRiC זמן רב יותר — עד כמה פעמים זמן המגורים הרגיל — והסתובב שוב ושוב דרך השפרון ללא הגעה למצב מקופל יציב. לבסוף, במקום להצטרף לרשת המבנית של התא, המוטנט הועבר למכונות הפירוק של התא. במקביל, המגעים של פרפולדין הפכו תכופים יותר אך קצרים יותר, והמגעים הישירים שלו עם TRiC פחתו, בהתאם לכך ש-TRiC בילה יותר זמן במצב סגור המכיל את הלקוח המקופל באופן שגוי.
אזור מָגֵן מקומי לקיפול
תצפית בולטת הייתה ש-TRiC ופרפולדין לעתים קרובות נשארו באזור הסמוך ללקוח בין סיבובי קשירה במקום לפזר למרחב הציטופלזמה. אחרי ששחררו חלבון, TRiC בדרך כלל נשארת מוגבלת בתוך אזור קטן סביב אתר התרגום עד כשתי שניות, ואז נקשרת מחדש לאותה שרשרת או לשרשרת סמוכה. המחברים גם זיהו מגעים חולפים בין קומפלקסי TRiC שונים שתלויים בהמשכיות סינתזת החלבון. ביחד, התנהגויות אלה תומכות ברעיון של "אזור קיפול מוגן" — צבר רופף ודינמי של שפרונים ומכונות תרגום שבו חלבונים שזה עתה יוצרו נשארים קרובים למסייעיהם ומוגנים ממגעים מזיקים עד שעתידם יוכרע.
מה משמעות הדבר לתאים בריאים ולמחלות
במלים פשוטות, עבודה זו מראה ש-TRiC ופרפולדין פועלים כדואו זריז של בקרת איכות: הם בודקים בקצרה שרשראות חלבון רבות, ממקדים את תשומת ליבם כשהשרשרת מתקרבת להשלמה, ואז מריצים סבבי קיפול מהירים בתוך בועה מקומית קטנה סביב הריבוזום. חלבונים מתפקדים היטב כמו אקטין הנורמלי בדרך כלל מגיעים לצורתם הנכונה אחרי מספר מעברים מהירים דרך TRiC. לעומת זאת, וריאנטים פגומים נלכדים במחזורים ממושכים ולבסוף מנותבים לפירוק, תוך שהם קושרים קיבולת שפרונים לאורך הדרך. התובנות ברמת מולקולת יחידה אלה מסייעות להסביר כיצד תאים מנהלים את הסיכון המתמיד של קיפול שגוי בסביבה צפופה, ולמה מוטציות בלקוחות או בשפרונים יכולות להטות את האיזון לעבר מחלה.
ציטוט: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
מילות מפתח: קוֹמְפַּקְטִצְיָת חלבון, שפרונים מולקולריים, שפרון TRiC, דינמיקות אקטין, פְרוֹטֵאוֹסטָזָה תאית