Clear Sky Science · ru
Динамика отдельных молекул системы шаперонина TRiC in vivo
Как клетки защищают вновь синтезированные белки
Каждую секунду ваши клетки продуцируют тысячи новых белков — крошечных молекулярных инструментов, которые должны свернуться в точную форму, чтобы выполнять свою функцию. Неправильно свернутые белки могут забивать клеточные механизмы и способствовать заболеваниям — от нейродегенерации до нарушений развития. В этом исследовании заглядывают внутрь живых человеческих клеток на уровне отдельных молекул, чтобы в реальном времени наблюдать, как крупная клеточная система сворачивания — шаперонин TRiC и его помощник префолдин — сопровождают новые белки к правильной форме и решают, что делать, когда сворачивание идет плохо.
Команда клеточного контроля качества в действии
Внутри наших клеток специальные белки‑помощники, называемые шаперонами, направляют другие белки в процессе их синтеза и сворачивания. TRiC — крупный бочкообразный комплекс, который может временно заключать неуправляемую полипептидную цепь, а префолдин — более мелкий комплекс с «щупальцами», доставляющий клиентов к TRiC. Ранее, главным образом в пробирках, показали, что TRiC способен сворачивать ключевые белки, такие как актин и тубулин. Но что происходит в плотном, оживленном внутреннем пространстве реальной клетки — как часто TRiC и префолдин встречают своих клиентов, как долго их удерживают и как реагируют на сложные случаи — оставалось неясным. Авторы разработали передовую методику трекинга отдельных частиц в живых человеческих клетках, чтобы проследить за отдельными молекулами TRiC и префолдiна и их столкновениями с недавно синтезированными белками.
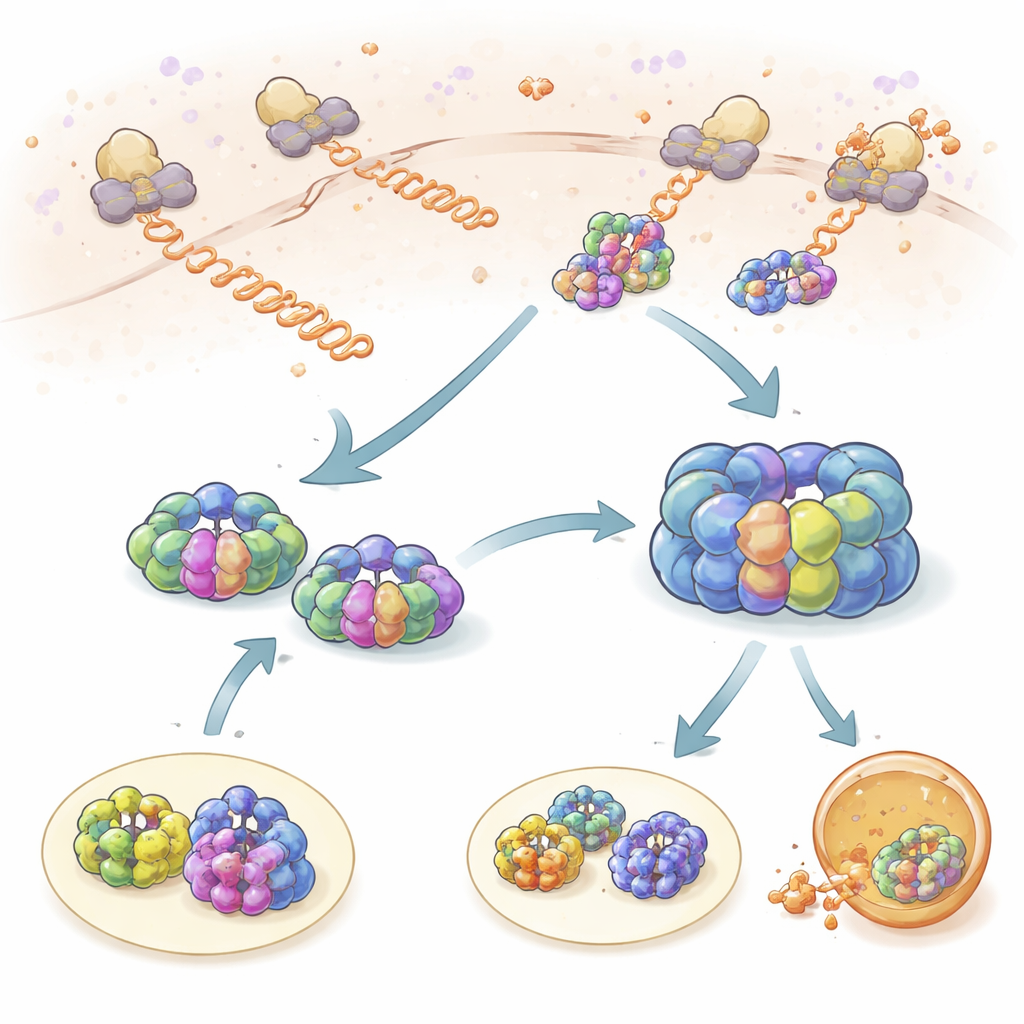
Краткие проверки во время синтеза белков
Сначала команда изучила, как TRiC и префолдин взаимодействуют со свежесинтезированными полипептидными цепями по мере их выхода из рибосом — фабрик по производству белков в клетке. Метив рибосомы, TRiC и префолдин разными флуоресцентными метками, они могли наблюдать, когда их движения становились связанными во времени и пространстве. И TRiC, и префолдин многократно касались набирающих цепей в коротких «пробных» событиях длительностью около секунды. Префолдин контактировал с новыми цепями чаще, чем TRiC, и снижение уровня префолдiна резко уменьшало доступ TRiC к этим клиентам, что указывает на роль префолдiна как рекрутера. С помощью рибосомного профайлинга авторы обнаружили, что сотни различных белков мониторятся таким образом, с сильным пересечением между клиентами TRiC и префолдiна, подчеркивая, что это партнерство является центральным для поддержания здорового пула белков.
Длительное взаимодействие к концу синтеза
Чтобы прицелиться в один обязательный клиент, исследователи отслеживали актин — ключевой строительный элемент клеточного скелета. Вместо прямого метки самого белка актин они меченовали его мРНК, что позволяло следить за местами синтеза актинa. По мере удлинения актиновой цепи и префолдин, и TRiC посещали ее чаще и задерживались дольше. Ближе к концу трансляции префолдин часто связывался на несколько секунд, держа почти завершенные цепи актинa и помогая привлечь TRiC для следующей фазы сворачивания. Когда исследователи искусственно прикрепили полноразмерный актин рядом с рибосомой, они наблюдали, как TRiC вовлекается в повторяющиеся циклы продолжительностью около 2,5 секунд каждый, что согласуется с многошаговым процессом сворачивания. Префолдин был важен для более длинных, более продуктивных взаимодействий с TRiC, что указывает на то, что он не только доставляет клиентов, но и настраивает работу TRiC.
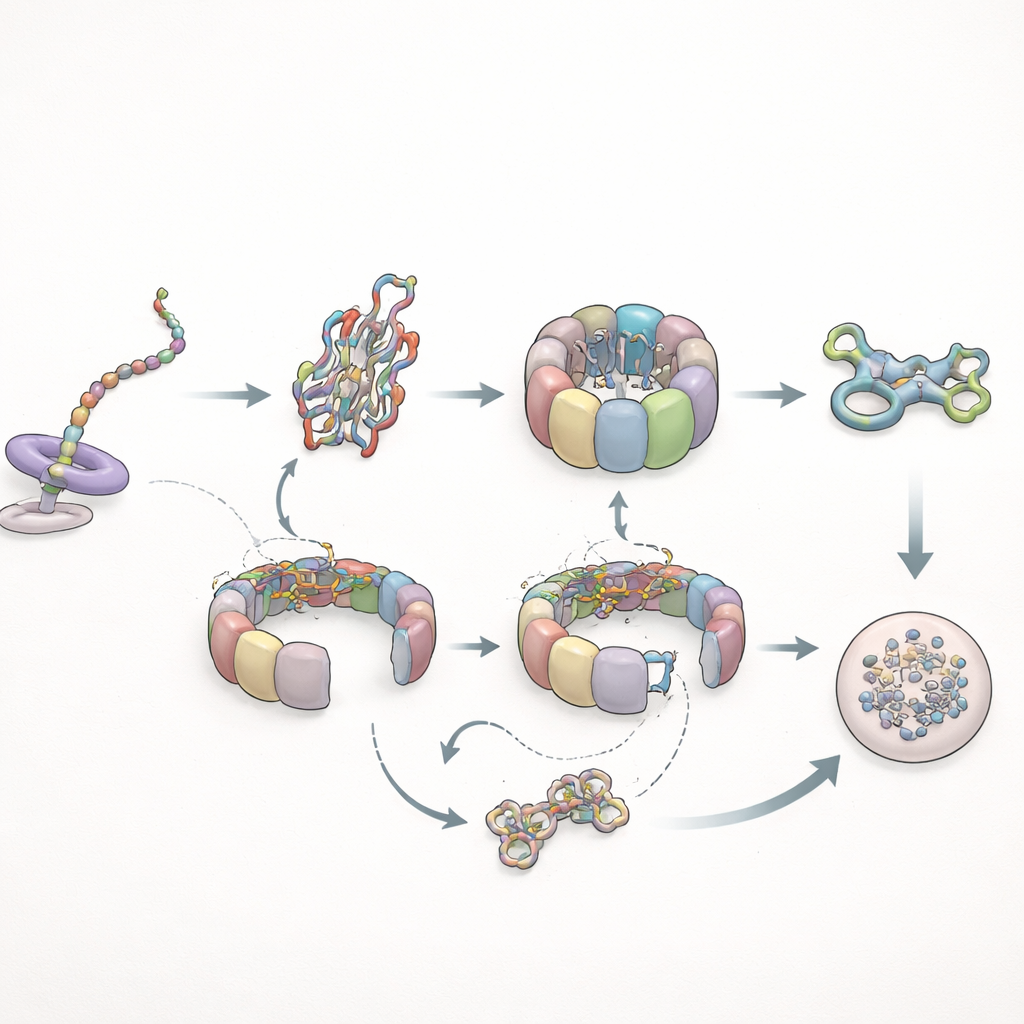
Когда сворачивание не удается: циклы и утилизация
Далее авторы проверили, как система справляется с проблемным клиентом: мутантной формой актинa, известной своей плохой способностью к сворачиванию. В ходе синтеза этот мутант вел себя почти нормально относительно взаимодействий с TRiC, но не развивал длительных контактов с префолдiном, характерных для здоровой версии, что указывает на то, что тонкие конформационные изменения в растущей цепи контролируют, как долго префолдин может удерживать субстрат. После завершения синтеза картина резко менялась. Мутантный актин дольше оставался связанным с TRiC — до нескольких раз превышая нормальное время пребывания — и многократно проходил через цикл шаперонина, не достигая стабильной свернутой формы. В конце концов, вместо встраивания в структурную сеть клетки мутант передавался на утилизацию в деградационные механизмы. Параллельно взаимодействия префолдiна становились более частыми, но короче, и его прямые контакты с TRiC уменьшались, что согласуется с тем, что TRiC проводит больше времени в закрытом, инкапсулирующем состоянии вокруг неверно свернувшегося клиента.
Локальная защитная зона для сворачивания
Поразительным наблюдением стало то, что TRiC и префолдин часто задерживались рядом со своим клиентом между раундами связывания, вместо того чтобы диффундировать в общую цитоплазму. После отпускания белка TRiC типично оставался в ограниченной области вокруг места синтеза до двух секунд, а затем вновь связывался с той же или соседней цепью. Авторы также зафиксировали кратковременные контакты между разными комплексами TRiC, зависящие от продолжающегося синтеза белков. В совокупности эти поведения поддерживают идею «защищенной зоны сворачивания» — рыхлого, динамичного скопления шаперонов и трансляционного аппарата, в котором вновь синтезированные белки держатся близко к помощникам и защищены от вредных взаимодействий до тех пор, пока о них не решат.
Что это значит для здоровых клеток и болезней
Проще говоря, эта работа показывает, что TRiC и префолдин действуют как подвижная пара контроля качества: они кратко инспектируют многие новые полипептидные цепи, сосредотачивают внимание по мере приближения цепи к завершению и затем запускают быстрые циклы сворачивания в небольшом локальном пузыре вокруг рибосомы. Хорошо себя проявляющие белки, такие как нормальный актин, обычно достигают правильной формы после нескольких быстрых проходов через TRiC. Напротив, дефектные варианты застревают в удлиненных циклах и в конечном итоге направляются на деградацию, при этом временно занимая ресурсы шаперонов. Эти наблюдения на уровне отдельных молекул помогают объяснить, как клетки управляют постоянным риском неверного сворачивания в плотной среде и почему мутации как в клиентах, так и в шаперонах могут сместить баланс в сторону заболеваний.
Цитирование: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Ключевые слова: сворачивание белков, молекулярные шапероны, шаперонин TRiC, динамика актинa, клеточный протеостаз