Clear Sky Science · de
Einzelmolekulare Dynamik des TRiC-Chaperonin-Systems in vivo
Wie Zellen neue Proteine aus Schwierigkeiten heraushalten
Jede Sekunde produzieren Ihre Zellen tausende neuer Proteine — winzige molekulare Werkzeuge, die sich in genau die richtige Form falten müssen, um zu funktionieren. Fehlgefaltete Proteine können die zellulären Maschinen verstopfen und zu Erkrankungen von Neurodegeneration bis zu Entwicklungsstörungen beitragen. Diese Studie blickt in lebende menschliche Zellen auf Einzelmolekülebene und beobachtet in Echtzeit, wie ein zentrales zelluläres Faltteam, das TRiC-Chaperonin und sein Helfer Prefoldin, neue Proteine in die richtige Form begleitet und entscheidet, was passiert, wenn die Faltung schiefläuft.
Ein zelluläres Qualitätskontrollteam bei der Arbeit
Im Inneren unserer Zellen leiten spezielle Helferproteine, sogenannte Chaperone, andere Proteine während ihrer Herstellung und Faltung. TRiC ist ein großer, fassförmiger Komplex, der vorübergehend eine widerspenstige Protein-Kette einschließen kann, während Prefoldin ein kleiner, tentakelähnlicher Komplex ist, der Kunden an TRiC liefert. Frühere Arbeiten, überwiegend in Reagenzgläsern, zeigten, dass TRiC wichtige Proteine wie Aktin und Tubulin falten kann. Aber was im dichten, geschäftigen Inneren einer echten Zelle passiert — wie oft TRiC und Prefoldin ihre Kunden treffen, wie lange sie sie halten und wie sie auf schwierige Fälle reagieren — war bisher unklar. Die Autoren entwickelten eine fortschrittliche Einzelpartikel-Tracking-Mikroskopie in lebenden menschlichen Zellen, um einzelne TRiC- und Prefoldin-Moleküle und ihre Begegnungen mit neu hergestellten Proteinen zu verfolgen.
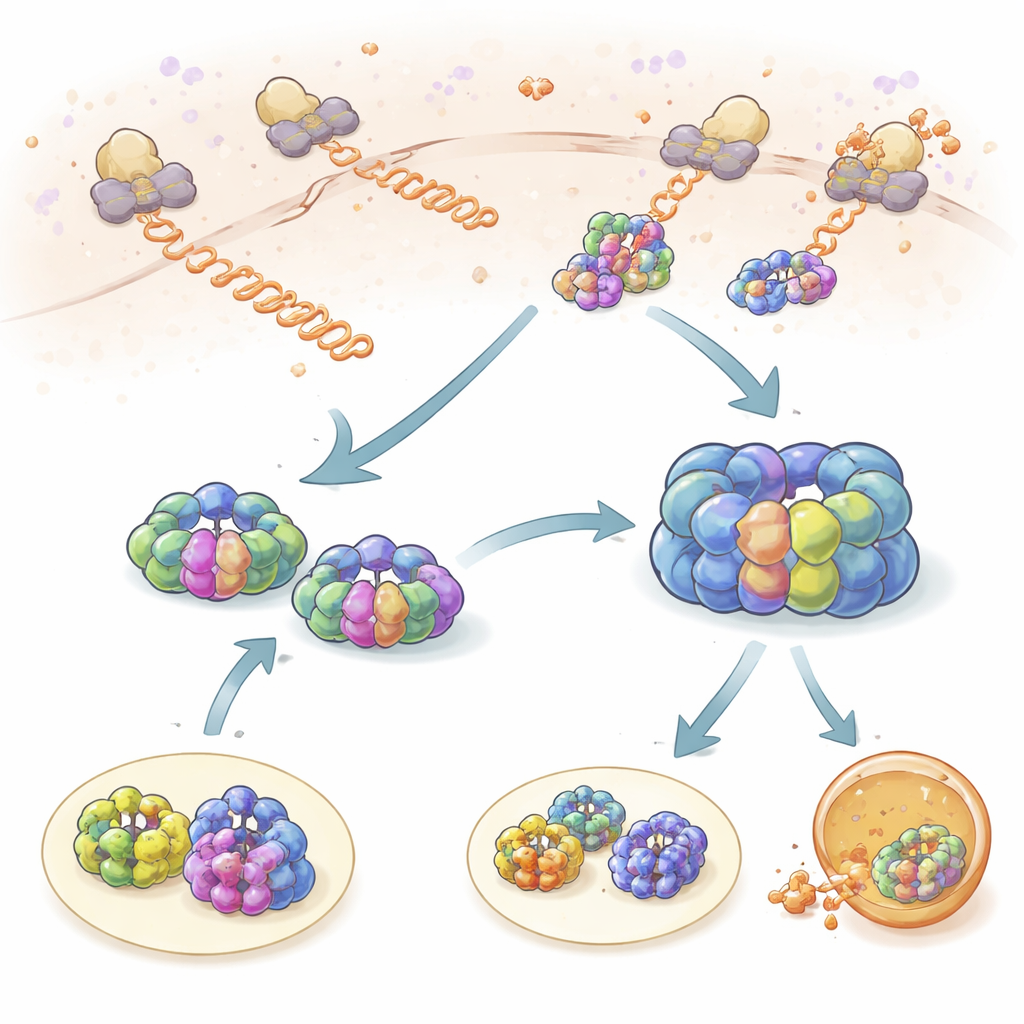
Kurzzeitige Kontrollen während der Proteinsynthese
Das Team betrachtete zuerst, wie TRiC und Prefoldin mit frisch synthetisierten Proteinketten interagieren, wenn diese aus den Ribosomen, den Proteinfabriken der Zelle, herauskommen. Durch das Markieren von Ribosomen, TRiC und Prefoldin mit verschiedenen fluoreszenten Farbstoffen konnten sie beobachten, wann sich ihre Bewegungen räumlich und zeitlich verknüpften. Sowohl TRiC als auch Prefoldin berührten neu entstehende Ketten wiederholt in kurzen „Sondierungs“-Ereignissen von etwa einer Sekunde Dauer. Prefoldin nahm häufiger Kontakt zu neuen Ketten auf als TRiC, und eine Reduktion der Prefoldin-Menge verringerte TRiCs Zugang zu diesen Kunden deutlich, was zeigt, dass Prefoldin als Rekrutierer wirkt. Mit Ribosom-Profiling fanden die Autoren, dass Hunderte verschiedener Proteine auf diese Weise überwacht werden, mit großer Überschneidung zwischen TRiC- und Prefoldin-Klienten, was betont, dass diese Partnerschaft zentral für die Aufrechterhaltung einer gesunden Proteinfracht ist.
Länger anhaltende Bindungen nahe dem Ziel
Um sich auf einen einzelnen obligaten Klienten zu konzentrieren, verfolgten die Forscher Aktin, einen wichtigen Baustein des zellulären Skeletts. Statt das Aktinprotein direkt zu markieren, markierten sie seine Boten-RNA, wodurch sie die Orte verfolgen konnten, an denen Aktin synthetisiert wurde. Mit zunehmender Länge der Aktinkette besuchten sowohl Prefoldin als auch TRiC häufiger und blieben länger. Gegen Ende der Translation band sich Prefoldin oft für mehrere Sekunden, hielt nahezu fertige Aktinketten und half, TRiC für die nächste Faltungsphase zu rekrutieren. Als die Forscher künstlich vollstädniges Aktin in der Nähe des Ribosoms verankerten, konnten sie sehen, dass TRiC es in wiederholten Zyklen von etwa 2,5 Sekunden Dauer engagierte, was mit einem mehrstufigen Faltungsprozess übereinstimmt. Prefoldin war entscheidend für die längeren, produktiveren TRiC-Interaktionen, was darauf hindeutet, dass es nicht nur Kunden liefert, sondern auch die Funktionsweise von TRiC abstimmt.
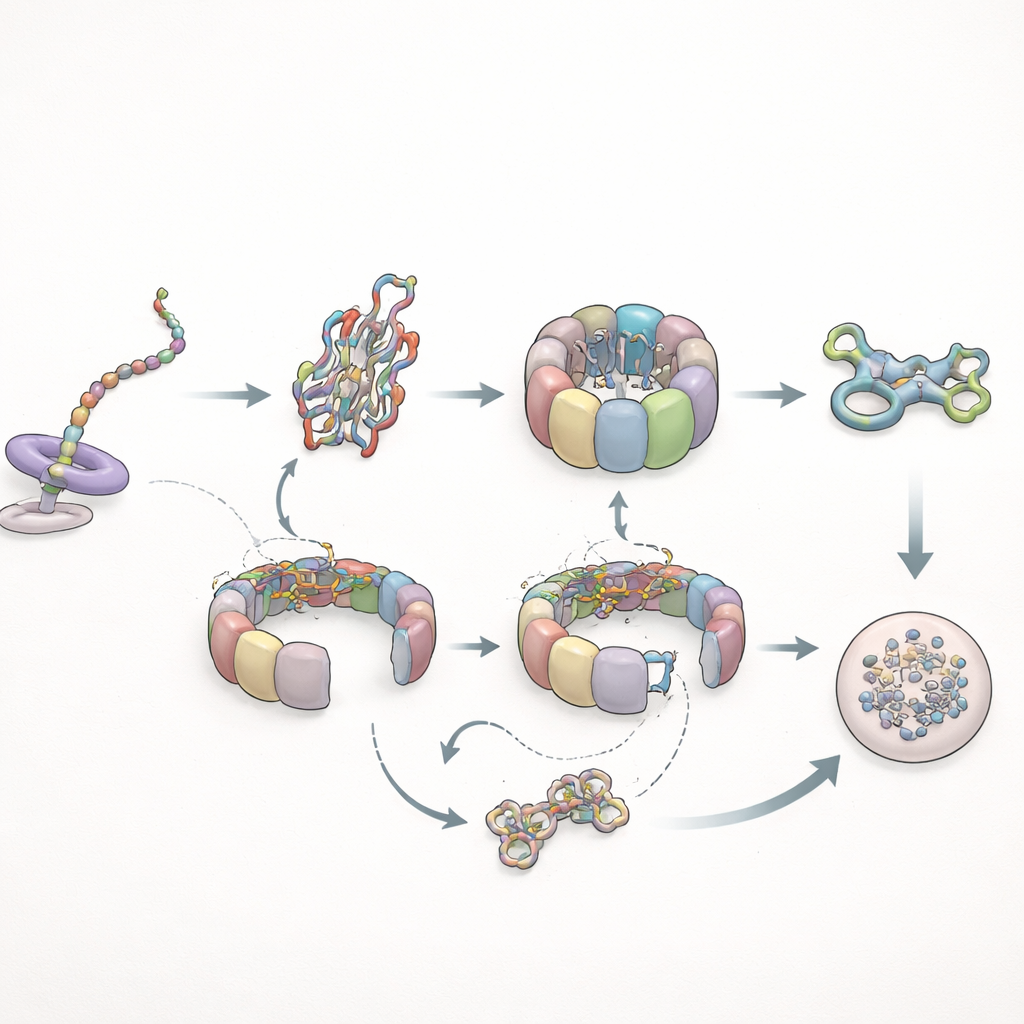
Wenn Faltung scheitert: Zyklen und Abbau
Die Autoren untersuchten dann, wie dieses System mit einem problematischen Klienten umgeht: einer mutanten Form von Aktin, die dafür bekannt ist, schlecht zu falten. Während der Proteinsynthese verhielt sich dieses Mutant fast normal gegenüber TRiC, zeigte jedoch nicht die verlängerten Prefoldin-Kontakte, die beim gesunden Protein beobachtet wurden, was darauf hindeutet, dass subtile Konformationsänderungen in der wachsenden Kette die Bindungsdauer von Prefoldin steuern. Nach der Synthese änderte sich das Bild dramatisch. Das mutante Aktin verweilte viel länger auf TRiC — bis zu mehreren Male der normalen Verweilzeit — und durchlief wiederholt Zyklen im Chaperonin, ohne einen stabilen gefalteten Zustand zu erreichen. Schließlich wurde es, statt in das strukturelle Netzwerk der Zelle einzutreten, an die Abbaumaschinerie der Zelle weitergereicht. Parallel dazu wurden Prefoldin-Interaktionen häufiger, aber kürzer, und seine direkten Begegnungen mit TRiC nahmen ab, was mit einer längeren, verschlossenen Einschlussphase von TRiC um den fehlgefalteten Klienten vereinbar ist.
Eine lokale Schutzzone für die Faltung
Eine auffällige Beobachtung war, dass TRiC und Prefoldin zwischen Bindungsrunden häufig in der Nähe ihres Klienten verweilten, anstatt in das umgebende Cytoplasma zu diffundieren. Nach der Freisetzung eines Proteins blieb TRiC typischerweise für bis zu zwei Sekunden in einem kleinen Bereich um die Translationsstelle eingeschränkt und band sich dann erneut an dieselbe oder eine benachbarte Kette. Die Autoren detektierten zudem vorübergehende Kontakte zwischen verschiedenen TRiC-Komplexen, die von anhaltender Proteinsynthese abhängig waren. Zusammen stützen diese Verhaltensweisen die Vorstellung einer „geschützten Faltungszone“ — einem lockeren, dynamischen Cluster aus Chaperonen und Translationsmaschinerie, in dem neu entstandene Proteine nahe bei ihren Helfern gehalten und vor schädlichen Interaktionen abgeschirmt werden, bis über ihr Schicksal entschieden ist.
Was das für gesunde Zellen und Krankheit bedeutet
Kurz gesagt zeigt diese Arbeit, dass TRiC und Prefoldin als agiles Qualitätskontrollduo fungieren: Sie inspizieren kurz viele neue Proteinketten, konzentrieren ihre Aufmerksamkeit, wenn die Kette der Fertigstellung näher kommt, und führen dann schnelle Faltungszyklen innerhalb einer kleinen lokalen Blase um das Ribosom aus. Gutartige Proteine wie normales Aktin erreichen in der Regel nach mehreren schnellen Durchgängen durch TRiC ihre korrekte Gestalt. Fehlerhafte Varianten dagegen werden in verlängerten Zyklen gefangen und schließlich dem Abbau zugeführt, wobei sie gleichzeitig Chaperonekapazität binden. Diese Einzelmolekül-Einblicke helfen zu erklären, wie Zellen das ständige Risiko von Fehlfaltung in einer überfüllten Umgebung managen und warum Mutationen in Klienten oder Chaperonen das Gleichgewicht zugunsten von Krankheit kippen können.
Zitation: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Schlüsselwörter: Proteinfaltung, molekulare Chaperone, TRiC-Chaperonin, Aktin-Dynamik, zelluläres Proteostase