Clear Sky Science · sv
Enkelmolekylsdynamik hos TRiC-chaperoninssystemet in vivo
Hur celler håller nya proteiner ur trubbel
Varje sekund producerar dina celler tusentals nya proteiner—små molekylära verktyg som måste vika sig i precis rätt form för att fungera. Felvikta proteiner kan täppa igen cellens maskineri och bidra till sjukdomar från neurodegeneration till utvecklingsstörningar. Denna studie skådar in i levande humana celler på enkelmolekylnivå för att i realtid se hur ett stort cellulärt vikningslag, TRiC-chaperoninet och dess hjälpare prefoldin, lotsar nya proteiner till korrekt form och avgör vad som ska göras när vikningen går fel.
En cellulär kvalitetskontrollgrupp i arbete
Inuti våra celler vägleder särskilda hjälpproteiner kallade chaperoner andra proteiner medan de syntetiseras och viks. TRiC är ett stort tunnelformat komplex som temporärt kan omsluta en stökig proteinpolymer, medan prefoldin är ett mindre tentakelliknande komplex som levererar klienter till TRiC. Tidigare arbete, mestadels i provrör, visade att TRiC kan vika viktiga proteiner såsom aktin och tubulin. Men vad som händer i den trånga, livliga inre miljön i en riktig cell—hur ofta TRiC och prefoldin möter sina klienter, hur länge de håller dem och hur de reagerar på svåra fall—har förblivit oklart. Författarna utvecklade avancerad enkelpartikelföljning i mikroskopi i levande humana celler för att följa individuella TRiC- och prefoldinmolekyler och deras möten med nyskapade proteiner.
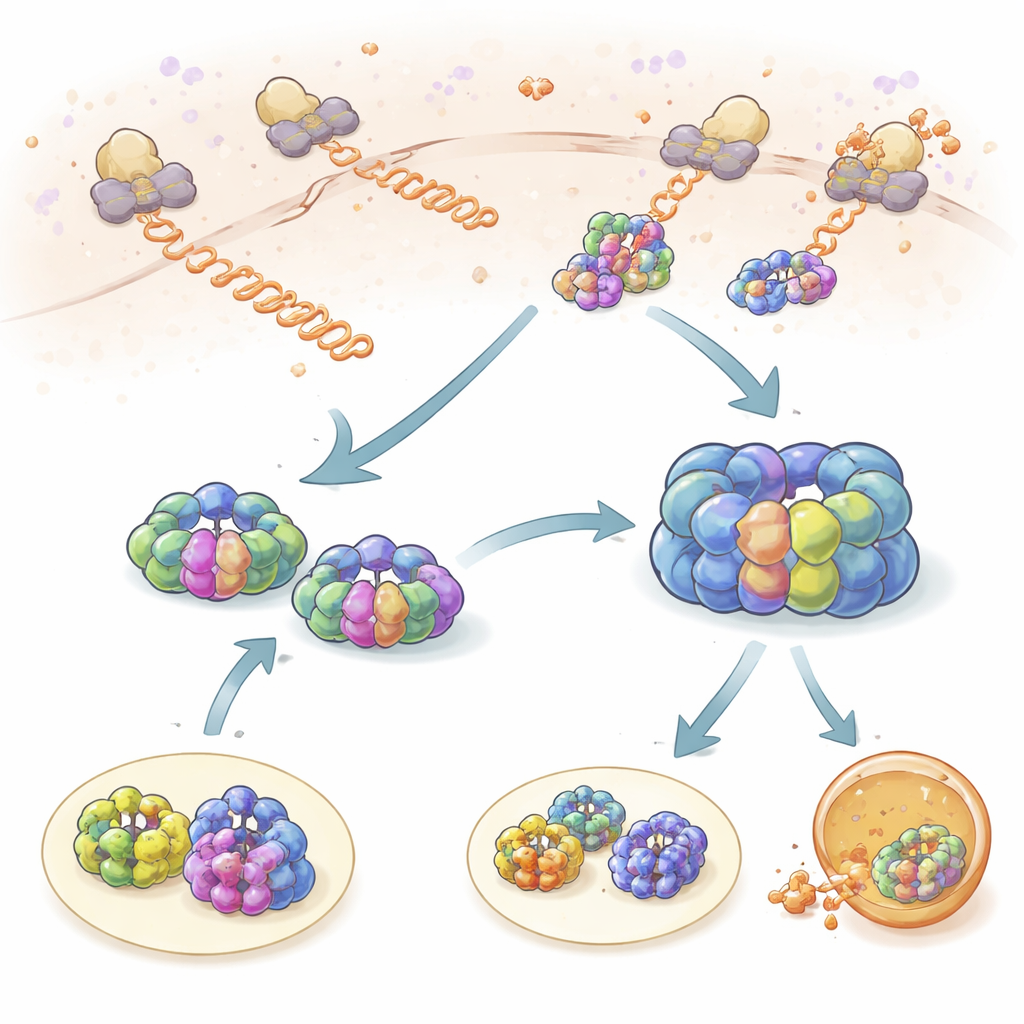
Korta kontroller medan proteinerna tillverkas
Teamet undersökte först hur TRiC och prefoldin interagerar med nysyntetiserade proteinkedjor när de tränger fram ur ribosomerna, cellens proteinfabriker. Genom att märka ribosomer, TRiC och prefoldin med olika fluorescerande färgämnen kunde de se när deras rörelser länkat samman i tid och rum. Både TRiC och prefoldin rörde vid nascenta kedjor upprepade gånger i korta ”provnings”-händelser som varade ungefär en sekund. Prefoldin kontaktade nya kedjor oftare än TRiC, och att minska prefoldinnivåerna sänkte kraftigt TRiC:s tillgång till dessa klienter, vilket visar att prefoldin fungerar som rekryterare. Genom ribosomprofilering fann författarna att hundratals olika proteiner övervakas på detta sätt, med stark överlappning mellan TRiC- och prefoldinklienter, vilket betonar att detta partnerskap är centralt för att upprätthålla en frisk proteinpott.
Varaktigt engagemang nära mållinjen
För att zooma in på en enskild obligat klient spårade forskarna aktin, en nyckelkomponent i cellens skelett. Istället för att märka aktinproteinet direkt märkte de dess budbärar-RNA, vilket gjorde det möjligt att följa platserna där aktin syntetiserades. När aktinkedjan växte längre besökte både prefoldin och TRiC oftare och stannade längre. I slutet av translationen band sig prefoldin ofta i flera sekunder, höll nästan fullängds aktinkedjor och hjälpte till att rekrytera TRiC för nästa vikningsfas. När forskarna konstgjort förankrade fullängdsaktin nära ribosomen kunde de se TRiC engagera det i upprepade cykler på cirka 2,5 sekunder vardera, i linje med en flerstegs vikningsprocess. Prefoldin var avgörande för de längre, mer produktiva TRiC-engagemangen, vilket antyder att det inte bara levererar klienter utan också finjusterar hur TRiC arbetar.
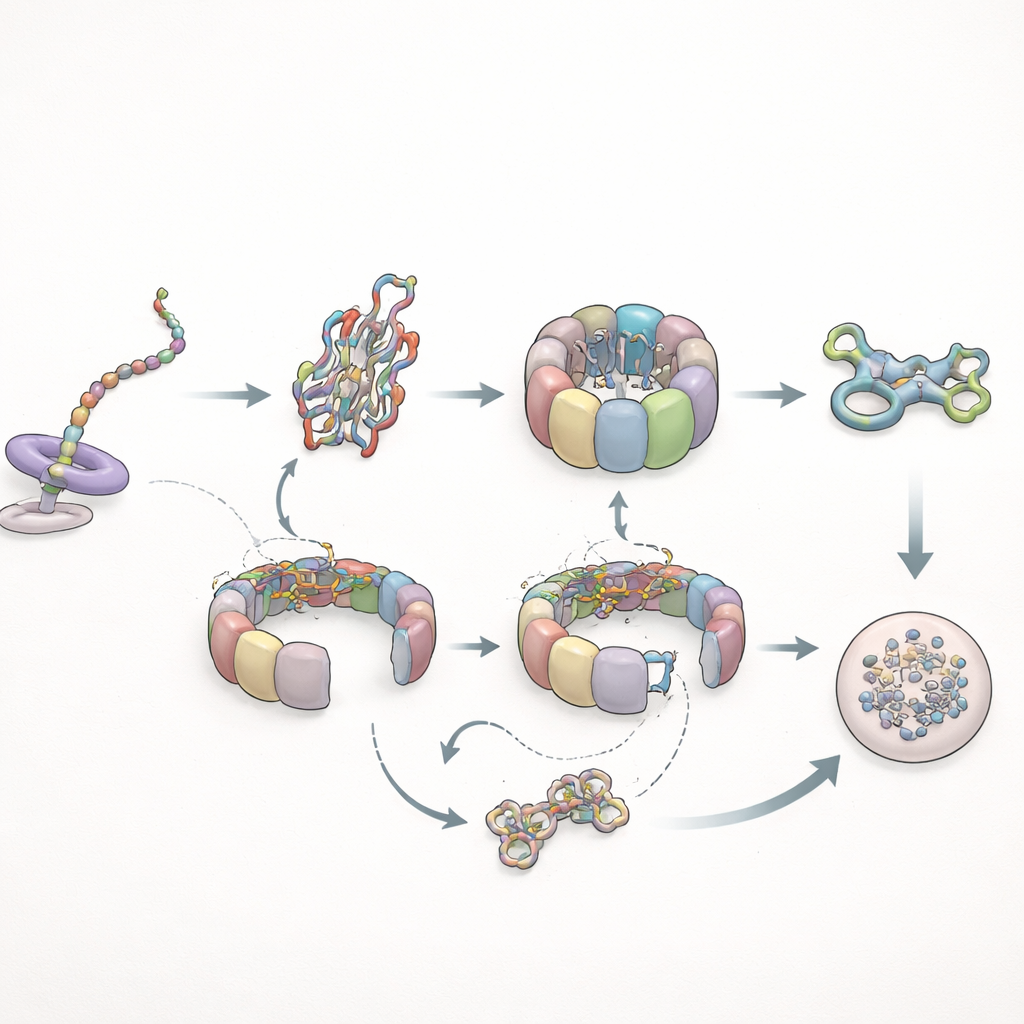
När vikning misslyckas: cykling och nedstädning
Författarna testade sedan hur detta system hanterar en problematisk klient: en mutant form av aktin som är känd för att vikta dåligt. Under proteinsyntesen betedde sig denna mutant nästan normalt gentemot TRiC men misslyckades med att utveckla de förlängda prefoldinkontakterna som sågs för den friska versionen, vilket indikerar att subtila konformationsförändringar i den växande kedjan styr hur länge prefoldin kan hålla kvar. Efter syntesen förändrades bilden dramatisk. Mutantaktin stannade kvar på TRiC mycket längre—upp till flera gånger normal vistelsetid—och cyklade upprepade gånger genom chaperoninet utan att nå ett stabilt format. Så småningom, istället för att gå med i cellens strukturella nätverk, skickades mutanten vidare till cellens nedbrytningsmaskineri. Parallellt blev prefoldins interaktioner mer frekventa men kortare, och dess direkta möten med TRiC minskade, i linje med att TRiC tillbringade mer tid i ett slutet, omslutande tillstånd kring den felvikta klienten.
En lokal skyddszon för vikning
En iögonfallande observation var att TRiC och prefoldin ofta stannade kvar nära sin klient mellan bindningsrundorna istället för att diffusivt lämna ut i cytoplasman. Efter att ha frigivit ett protein förblev TRiC vanligen begränsat inom ett litet område runt translationsstället i upp till två sekunder, för att sedan binda om samma eller en närliggande kedja. Författarna detekterade också kortvariga kontakter mellan olika TRiC-komplex som var beroende av pågående proteinsyntes. Tillsammans stöder dessa beteenden idén om en ”skyddad vikningszon”—en lös, dynamisk klusterbildning av chaperoner och translationsmaskineri där nyskapade proteiner hålls nära sina hjälpare och skyddas från skadliga interaktioner tills deras öde avgörs.
Vad detta betyder för friska celler och sjukdom
Enkelt uttryckt visar detta arbete att TRiC och prefoldin fungerar som ett rörligt kvalitetskontrollpar: de inspekterar kortfattat många nya proteinkedjor, fokuserar sin uppmärksamhet när kedjan närmar sig färdigställande och kör sedan snabba vikningscykler inom en liten lokal bubbla runt ribosomen. Välfungerande proteiner som normalt aktin når i allmänhet korrekt form efter flera snabba pass genom TRiC. Defekta varianter däremot fastnar i förlängda cykler och leds slutligen till nedbrytning, vilket binder upp chaperonkapacitet på vägen. Dessa enkelmolekylinsikter hjälper till att förklara hur celler hanterar den konstanta risken för felvikning i en trång miljö, och varför mutationer i antingen klienter eller chaperoner kan rubba balansen mot sjukdom.
Citering: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Nyckelord: proteinfällning, molekylära chaperoner, TRiC-chaperonin, aktin-dynamik, cellulär proteostas