Clear Sky Science · es
Dinámica de una sola molécula del sistema chaperonina TRiC in vivo
Cómo las células evitan problemas con las proteínas recién hechas
Cada segundo, tus células producen miles de proteínas nuevas: pequeñas herramientas moleculares que deben plegarse en la forma correcta para funcionar. Las proteínas mal plegadas pueden obstruir la maquinaria celular y contribuir a enfermedades que van desde la neurodegeneración hasta trastornos del desarrollo. Este estudio mira dentro de células humanas vivas a nivel de molécula única para observar, en tiempo real, cómo un equipo principal de plegamiento celular —la chaperonina TRiC y su ayudante prefoldina— guía a las proteínas novedosas hacia la conformación adecuada y decide qué hacer cuando el plegamiento falla.
Un equipo de control de calidad celular en acción
Dentro de nuestras células, proteínas ayudantes especiales llamadas chaperonas guían a otras proteínas mientras se sintetizan y pliegan. TRiC es un gran complejo con forma de barril que puede encerrar temporalmente una cadena proteica revoltosa, mientras que la prefoldina es un complejo más pequeño con apéndices que entrega a los clientes a TRiC. Trabajos anteriores, mayormente en tubos de ensayo, mostraron que TRiC puede plegar proteínas importantes como la actina y la tubulina. Pero lo que ocurre en el interior abarrotado y dinámico de una célula real —con qué frecuencia TRiC y la prefoldina se encuentran con sus clientes, cuánto tiempo los retienen y cómo responden a casos difíciles— seguía siendo confuso. Los autores desarrollaron microscopía avanzada de seguimiento de partículas individuales en células humanas vivas para seguir moléculas aisladas de TRiC y prefoldina y sus encuentros con proteínas recién sintetizadas.
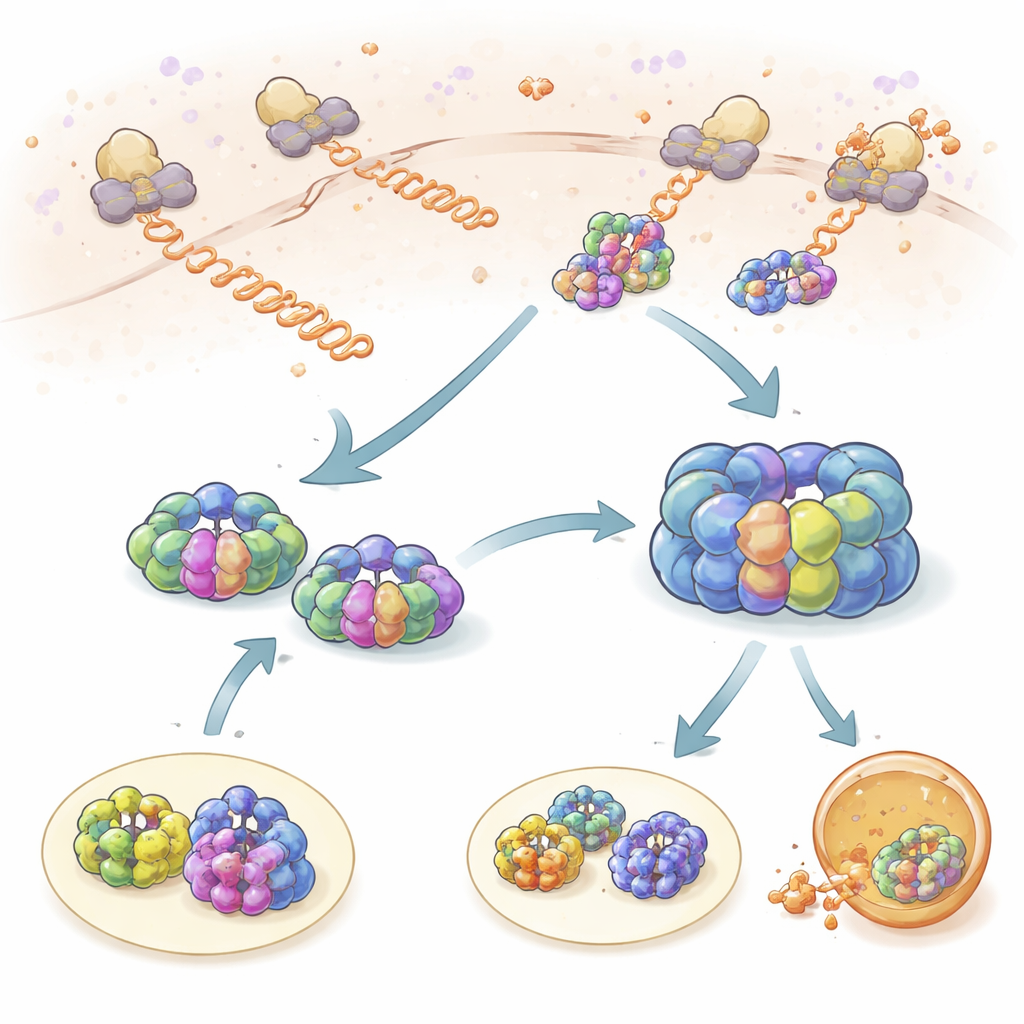
Revisiones breves mientras se fabrican las proteínas
El equipo examinó primero cómo interactúan TRiC y la prefoldina con cadenas proteicas recién sintetizadas a medida que emergen de los ribosomas, las fábricas de proteínas de la célula. Etiquetando ribosomas, TRiC y prefoldina con diferentes tintes fluorescentes, pudieron observar cuándo sus movimientos se vinculaban en espacio y tiempo. Tanto TRiC como la prefoldina tocaron repetidamente las cadenas nacientes en breves eventos de “sondeo” que duraban alrededor de un segundo. La prefoldina contactaba las nuevas cadenas con más frecuencia que TRiC, y reducir los niveles de prefoldina disminuyó drásticamente el acceso de TRiC a estos clientes, mostrando que la prefoldina actúa como reclutadora. Mediante perfilado de ribosomas, los autores encontraron que cientos de proteínas diferentes se vigilan de esta manera, con una fuerte superposición entre los clientes de TRiC y prefoldina, lo que subraya que esta asociación es central para mantener una población proteica saludable.
Compromisos prolongados cerca de la línea de meta
Para acercarse a un único cliente obligado, los investigadores siguieron la actina, un componente clave del esqueleto celular. En lugar de marcar la proteína actina directamente, etiquetaron su ARN mensajero, lo que les permitió seguir los sitios donde se sintetizaba la actina. A medida que la cadena de actina crecía, tanto la prefoldina como TRiC la visitaban con mayor frecuencia y permanecían más tiempo. Cerca del final de la traducción, la prefoldina a menudo se unía durante varios segundos, reteniendo cadenas de actina casi completas y ayudando a reclutar a TRiC para la siguiente fase del plegamiento. Cuando los investigadores fijaron artificialmente actina de cadena completa cerca del ribosoma, pudieron observar que TRiC la comprometía en ciclos repetidos de aproximadamente 2,5 segundos cada uno, consistente con un proceso de plegamiento en varios pasos. La prefoldina fue crucial para los compromisos más largos y productivos de TRiC, lo que sugiere que no solo entrega clientes, sino que también modula el funcionamiento de TRiC.
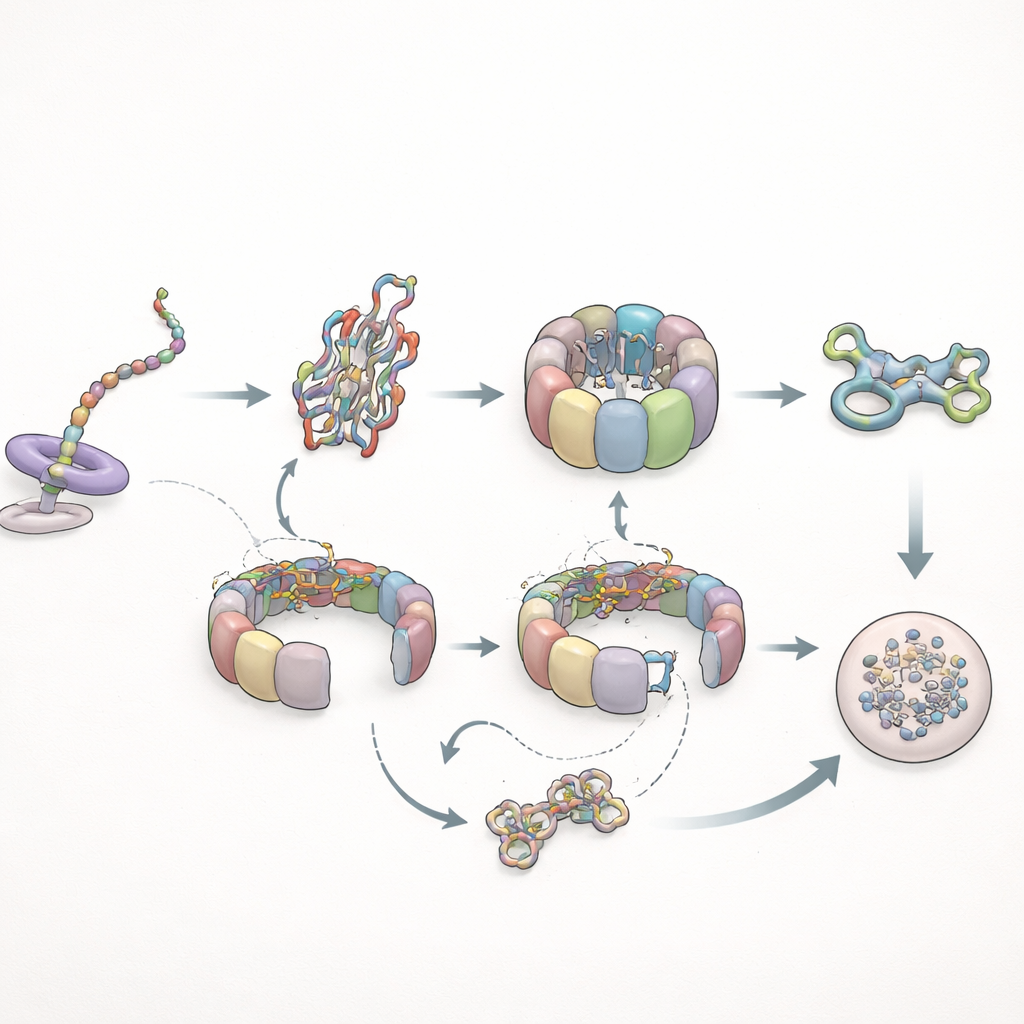
Cuando el plegamiento falla: ciclos y limpieza
Los autores probaron entonces cómo maneja este sistema a un cliente problemático: una forma mutante de actina conocida por plegarse mal. Durante la síntesis, este mutante se comportó casi con normalidad frente a TRiC, pero no desarrolló los contactos prolongados con prefoldina observados en la versión sana, lo que indica que cambios conformacionales sutiles en la cadena en crecimiento controlan cuánto tiempo la prefoldina puede retenerla. Tras la síntesis, la situación cambió drásticamente. La actina mutante permaneció en TRiC mucho más tiempo —hasta varias veces la duración normal— y recicló repetidamente a través de la chaperonina sin alcanzar un estado plegado estable. Eventualmente, en lugar de incorporarse a la red estructural de la célula, la mutante se destinó a la maquinaria de degradación celular. En paralelo, las interacciones de la prefoldina se volvieron más frecuentes pero más breves, y sus encuentros directos con TRiC disminuyeron, coherente con TRiC pasando más tiempo en un estado cerrado que encapsula al cliente mal plegado.
Una zona protectora local para el plegamiento
Una observación llamativa fue que TRiC y la prefoldina a menudo permanecían cerca de su cliente entre rondas de unión en lugar de difundirse hacia el citoplasma general. Tras liberar una proteína, TRiC típicamente permanecía confinado dentro de una pequeña región alrededor del sitio de traducción durante hasta dos segundos, y luego se volvía a unir a la misma u otra cadena vecina. Los autores también detectaron contactos transitorios entre diferentes complejos TRiC que dependían de la síntesis proteica en curso. En conjunto, estos comportamientos respaldan la idea de una “zona protegida de plegamiento”: un racimo suelto y dinámico de chaperonas y maquinaria de traducción en el que las proteínas recién hechas se mantienen cerca de sus ayudantes y protegidas de interacciones dañinas hasta que se decide su destino.
Qué implica esto para células sanas y para la enfermedad
En términos sencillos, este trabajo demuestra que TRiC y la prefoldina actúan como un dúo ágil de control de calidad: inspeccionan brevemente muchas cadenas nuevas, concentran su atención a medida que la cadena se acerca a la finalización y luego realizan ciclos rápidos de plegamiento dentro de una pequeña burbuja local alrededor del ribosoma. Las proteínas bien comportadas como la actina normal suelen alcanzar su conformación correcta tras varias pasadas rápidas por TRiC. Las variantes defectuosas, en cambio, quedan atrapadas en ciclos prolongados y acaban siendo encaminadas a la degradación, consumiendo capacidad de chaperonas en el proceso. Estas ideas a nivel de molécula única ayudan a explicar cómo las células gestionan el riesgo constante de mal plegamiento en un entorno concurrido, y por qué las mutaciones en los clientes o en las chaperonas pueden inclinar la balanza hacia la enfermedad.
Cita: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Palabras clave: plegamiento de proteínas, chaperonas moleculares, chaperonina TRiC, dinámica de la actina, proteostasis celular