Clear Sky Science · ar
ديناميكيات جزيء واحد لنظام الشابيرونين TRiC داخل الخلايا الحية
كيف تحمي الخلايا البروتينات الجديدة من المشاكل
كل ثانية، تُنتج خلاياك آلاف البروتينات الجديدة—أدوات جزيئية صغيرة يجب أن تطوى إلى الشكل الصحيح لتؤدي وظيفتها. يمكن للبروتينات المطوية بشكل خاطئ أن تسد آليات الخلية وتساهم في أمراض تتراوح من التنكس العصبي إلى اضطرابات التطور. تستعرض هذه الدراسة داخل خلايا بشرية حية على مستوى جزيء واحد لمراقبة، في الوقت الحقيقي، كيف يقوم فريق الطي الخلوي الرئيسي، الشابيرونين TRiC ومعاونه بريفولدين، بإرشاد البروتينات الجديدة إلى الشكل الصحيح وما الذي يفعلونه عندما تفشل عملية الطي.
فريق مراقبة الجودة الخلوي أثناء العمل
داخل خلايانا، توجه بروتينات مساعدة خاصة تُسمى الشابيرونات بروتينات أخرى أثناء تصنيعها وطيها. TRiC هو مركب كبير على شكل برميل يمكنه احتواء سلسلة بروتينية متمردة مؤقتًا، بينما بريفولدين هو مركب أصغر بشِبه مجسات يقوم بتسليم العملاء إلى TRiC. أظهرت دراسات سابقة، معظمها في أنابيب الاختبار، أن TRiC يستطيع طي بروتينات مهمة مثل الأكتين والتوبولين. لكن ما يحدث في الداخل المزدحم والحيوي للخلية الحقيقية—كم مرة تلتقي TRiC وبريفولدين بعملائهم، كم من الوقت يحتفظان بهم، وكيف يتعاملان مع الحالات الصعبة—ظل غامضًا. طور الباحثون تقنية متقدمة لتتبع جسيمات مفردة بالمجهر في خلايا بشرية حية لملاحظة جزيئات TRiC وبريفولدين الفردية ولقاءاتها مع البروتينات الجديدة.
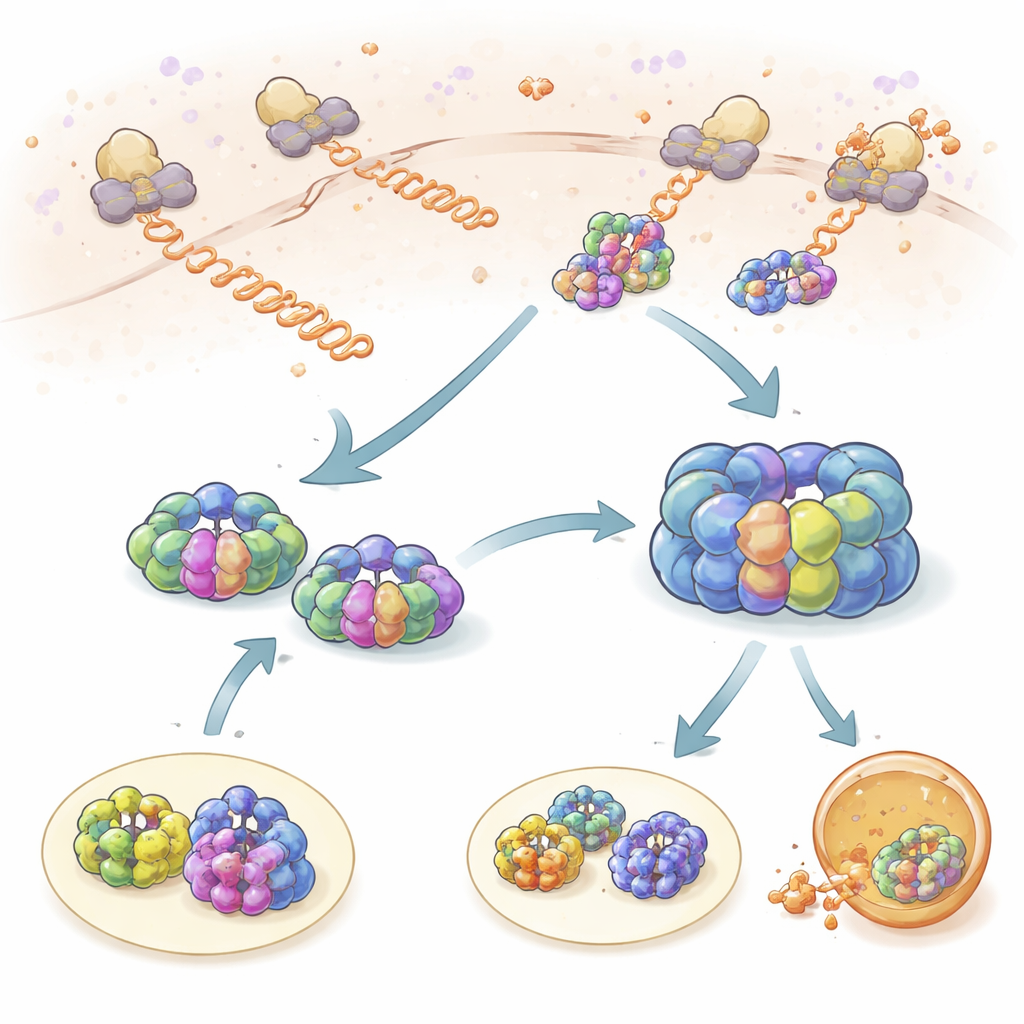
فحوصات قصيرة أثناء تصنيع البروتين
نظر الفريق أولًا في كيفية تفاعل TRiC وبريفولدين مع سلاسل البروتين المولدة حديثًا أثناء خروجها من الريبوسومات، مصانع البروتين في الخلية. من خلال وسم الريبوسومات وTRiC وبريفولدين بأصباغ فلورية مختلفة، استطاعوا مراقبة متى ترتبط تحركاتها في الزمان والمكان. لمس كل من TRiC وبريفولدين السلاسل الناشئة مرارًا في أحداث «تحقق» قصيرة استمرت حوالي ثانية واحدة. تلامس بريفولدين مع السلاسل الجديدة كان أكثر تواترًا من TRiC، وتخفيض مستويات بريفولدين خفّض بشكل كبير وصول TRiC إلى هؤلاء العملاء، ما يدل على أن بريفولدين يعمل كعامل تجنيد. باستخدام ملفات تعريف الريبوسومات، وجد الباحثون أن مئات البروتينات المختلفة تُراقب بهذه الطريقة، مع تداخل كبير بين عملاء TRiC وبريفولدين، مما يؤكد أن هذه الشراكة مركزية للحفاظ على حُسْن حالة مجموعة البروتينات في الخلية.
ارتباط ممتد قرب خط النهاية
للتركيز على عميل ملزم واحد، تتبع الباحثون الأكتين، حجر البناء الرئيسي لهيكل الخلية. بدلًا من وسم بروتين الأكتين مباشرة، وسموا الحمض النووي الريبوسي الرسول الخاص به، مما مكنهم من تتبع مواقع تصنيع الأكتين. مع نمو سلسلة الأكتين، زادت زيارات كل من بريفولدين وTRiC وتطول مدة بقائهما. قرب نهاية الترجمة، غالبًا ما كان بريفولدين يرتبط لعدة ثوانٍ، محتلًا سلاسل أكتين شبه مكتملة ويساعد في تجنيد TRiC للمرحلة التالية من الطي. عندما ربط الباحثون عمدًا جزيئات أكتين مكتملة الطول بالقرب من الريبوسوم، لاحظوا أن TRiC يتعامل معها في دورات متكررة مدتها نحو 2.5 ثانية لكل دورة، وهو ما يتوافق مع عملية طي متعددة الخطوات. كان بريفولدين حاسمًا لمشاركات TRiC الأطول والأكثر إنتاجية، مما يشير إلى أنه لا يقتصر دوره على التسليم فحسب، بل يضبط أيضًا طريقة عمل TRiC.
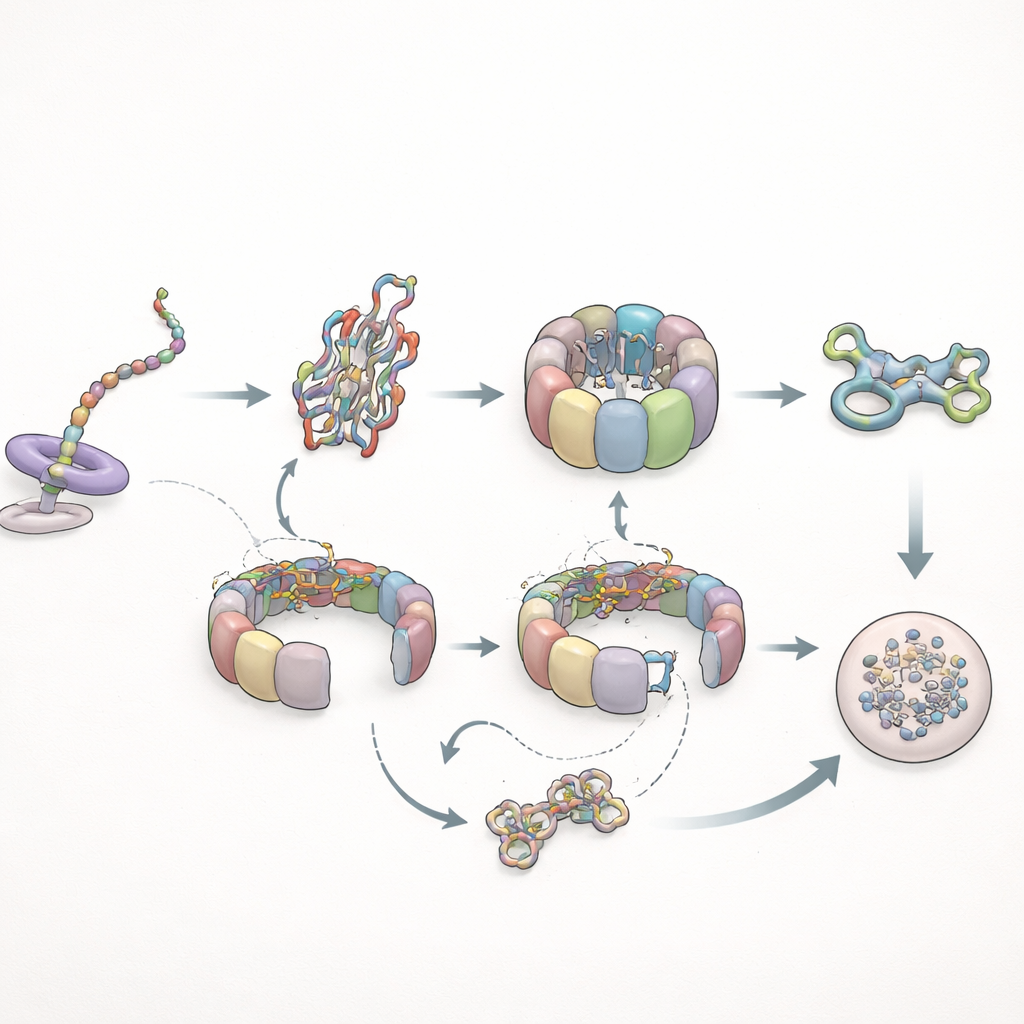
عندما يفشل الطي: دورات وتنظيف
اختبر المؤلفون بعد ذلك كيف يتعامل هذا النظام مع عميل إشكالي: شكل طافح من الأكتين معروف عنه أنه يطوى بشكل ضعيف. أثناء تخليق البروتين، تصرف هذا المتحور بشكل شبه طبيعي مع TRiC لكنه فشل في تكوين الاتصالات الطويلة الأمد مع بريفولدين التي لوحظت لدى النسخة السليمة، ما يشير إلى أن تغييرات شكلية دقيقة في السلسلة النامية تتحكم في مدة تمسك بريفولدين. بعد الانتهاء من التخليق تغيرت القصة جذريًا. بقي الأكتين المتحوِّر على TRiC لفترات أطول بكثير—حتى عدة أضعاف زمن الإقامة الطبيعي—ودورِيًّا تجول عبر الشابيرونين دون الوصول إلى حالة مطوية مستقرة. في النهاية، بدلًا من الانضمام إلى الشبكة البنائية للخلية، تم تمرير المتحور إلى آليات التحلل الخلوية. تزامنًا مع ذلك، أصبحت تفاعلات بريفولدين أكثر تكرارًا لكنها أقصر مدة، وانخفضت لقاءاته المباشرة مع TRiC، بما يتوافق مع بقاء TRiC لفترات أطول في حالة مغلقة تحيط بالعميل المطوي بشكل خاطئ.
منطقة محمية محلية للطي
ملاحظة لافتة كانت أن TRiC وبريفولدين كثيرًا ما بقيا بالقرب من عميلهما بين جولات الارتباط بدلًا من الانتشار في سائِل السيتوبلازم. بعد تحرير بروتين، عادة ما بقي TRiC محصورًا ضمن منطقة صغيرة حول موقع الترجمة لمدة تصل إلى ثانيتين، ثم أعاد الارتباط بنفس السلسلة أو بسلسلة مجاورة. كما كشف المؤلفون عن اتصالات عابرة بين مركبات TRiC مختلفة اعتمدت على استمرار تصنيع البروتين. مجتمعة، تدعم هذه السلوكيات فكرة «منطقة طي محمية»—عنقود فضفاض وديناميكي من الشابيرونات وآليات الترجمة تحافظ على قرب البروتينات الجديدة من معيلِها وتحميها من تداخلات ضارة حتى يُتخذ قرار بشأن مصيرها.
ما الذي تعنيه هذه النتائج للخلايا السليمة والمرض
بعبارة مبسطة، تُظهر هذه الدراسة أن TRiC وبريفولدين يعملا كثنائي مرن لمراقبة الجودة: يفحصان بسرعة العديد من السلاسل البروتينية الجديدة، يركزان اهتمامهما مع اقتراب السلسلة من الاكتمال، ثم يجرون دورات طي سريعة داخل فقاعة محلية صغيرة حول الريبوسوم. البروتينات السليمة مثل الأكتين الطبيعي عمومًا تصل إلى شكلها الصحيح بعد عدة مرورّات سريعة عبر TRiC. بالمقابل، تصبح الأشكال المعيبة محاصرة في دورات ممتدة وتُحوَّل في النهاية إلى التحلل، مما يستهلك طاقة وقدرة الشابيرونات في الطريق. تساهم هذه الرؤى على مستوى جزيء واحد في توضيح كيف تدير الخلايا خطر الطي الخاطئ المستمر في بيئة مزدحمة، ولماذا يمكن لأنماط الطفرات في العملاء أو الشابيرونات أن تُزحزح التوازن باتجاه المرض.
الاستشهاد: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
الكلمات المفتاحية: طي البروتين, البروتينات المرافقة الجزيئية, الشابيرونين TRiC, ديناميكيات الأكتين, توازن البروتين الخلوي