Clear Sky Science · nl
Dynamiques van enkele moleculen van het TRiC-chaperoninesysteem in vivo
Hoe cellen nieuwe eiwitten uit de problemen houden
Elke seconde maken je cellen duizenden nieuwe eiwitten aan—kleine moleculaire werktuigen die in precies de juiste vorm moeten vouwen om hun werk te doen. Verkeerd gevouwde eiwitten kunnen het cellulaire apparaat blokkeren en bijdragen aan ziekten variërend van neurodegeneratie tot ontwikkelingsstoornissen. Deze studie kijkt binnen levende menselijke cellen naar individuele moleculen om in realtime te volgen hoe een belangrijk vouwhulp-team, het TRiC-chaperonine en zijn hulpje prefoldine, nieuwe eiwitten naar de juiste vorm begeleiden en bepalen wat er gebeurt als het vouwen misgaat.
Een cellulair kwaliteitscontroleteam aan het werk
Binnen onze cellen begeleiden speciale hulp-eiwitten, chaperonnes genoemd, andere eiwitten terwijl ze worden gemaakt en gevouwen. TRiC is een groot, tonvormig complex dat tijdelijk een lastige eiwitketen kan omsluiten, terwijl prefoldine een kleiner, tentakelachtig complex is dat klanten naar TRiC brengt. Eerder werk, grotendeels in reageerbuizen, toonde aan dat TRiC belangrijke eiwitten zoals actine en tubuline kan vouwen. Maar wat gebeurt er in het drukke, chaotische binnenste van een echte cel—hoe vaak TRiC en prefoldine hun klanten tegenkomen, hoe lang ze ze vasthouden en hoe ze op moeilijke gevallen reageren—bleef onduidelijk. De auteurs ontwikkelden geavanceerde single-particle-tracking-microscopie in levende menselijke cellen om individuele TRiC- en prefoldinemoleculen en hun ontmoetingen met pas gemaakte eiwitten te volgen.
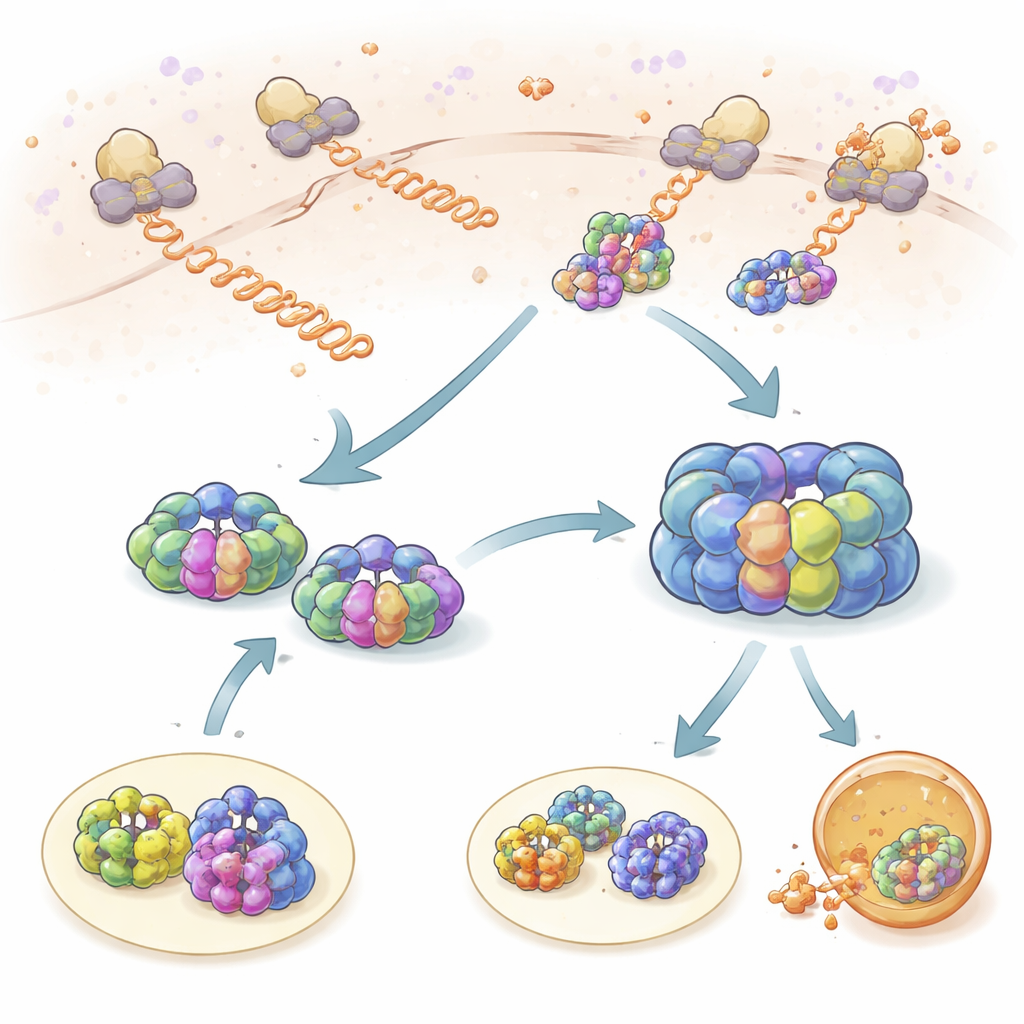
Korte controles terwijl eiwitten worden gemaakt
Het team bekeek eerst hoe TRiC en prefoldine omgaan met pas gesynthetiseerde eiwitketens zodra die uit ribosomen, de eiwitfabrieken van de cel, tevoorschijn komen. Door ribosomen, TRiC en prefoldine met verschillende fluorescerende kleurstoffen te labelen, konden ze zien wanneer hun bewegingen ruimtelijk en temporeel gekoppeld raakten. Zowel TRiC als prefoldine raakten nieuwe ketens herhaaldelijk aan in korte «proef»-events van ongeveer een seconde. Prefoldine maakte vaker contact met nieuwe ketens dan TRiC, en het verlagen van prefoldineniveaus verminderde scherp TRiC’s toegang tot deze klanten, wat toont dat prefoldine als recruiter fungeert. Met ribosoomprofilering vonden de auteurs dat honderden verschillende eiwitten op deze manier worden gecontroleerd, met een sterke overlap tussen TRiC- en prefoldineklanten, wat benadrukt dat dit partnerschap centraal staat voor het behoud van een gezonde eiwitpopulatie.
Langduriger betrokkenheid dicht bij de finish
Om in te zoomen op één verplichte klant volgden de onderzoekers actine, een belangrijk bouwblok van het cellulair skelet. In plaats van actine-eiwit direct te labelen, merkten ze het messenger-RNA ervan, zodat ze de locaties konden volgen waar actine werd gesynthetiseerd. Naarmate de actineketen langer werd, bezochten zowel prefoldine als TRiC vaker en bleven ze langer hangen. Tegen het einde van de translatie bond prefoldine vaak enkele seconden, waarbij het bijna volledige actineketens vasthield en hielp TRiC te rekruteren voor de volgende fase van het vouwen. Toen de onderzoekers volledig gevouwen actine kunstmatig dicht bij het ribosoom vastmaakten, zagen ze TRiC het in herhaalde cycli van ongeveer 2,5 seconde per cyclus betrekken, consistent met een meerstaps vouwproces. Prefoldine was cruciaal voor de langere, productievere TRiC-engagements, wat suggereert dat het niet alleen klanten aflevert maar ook afstelt hoe TRiC werkt.
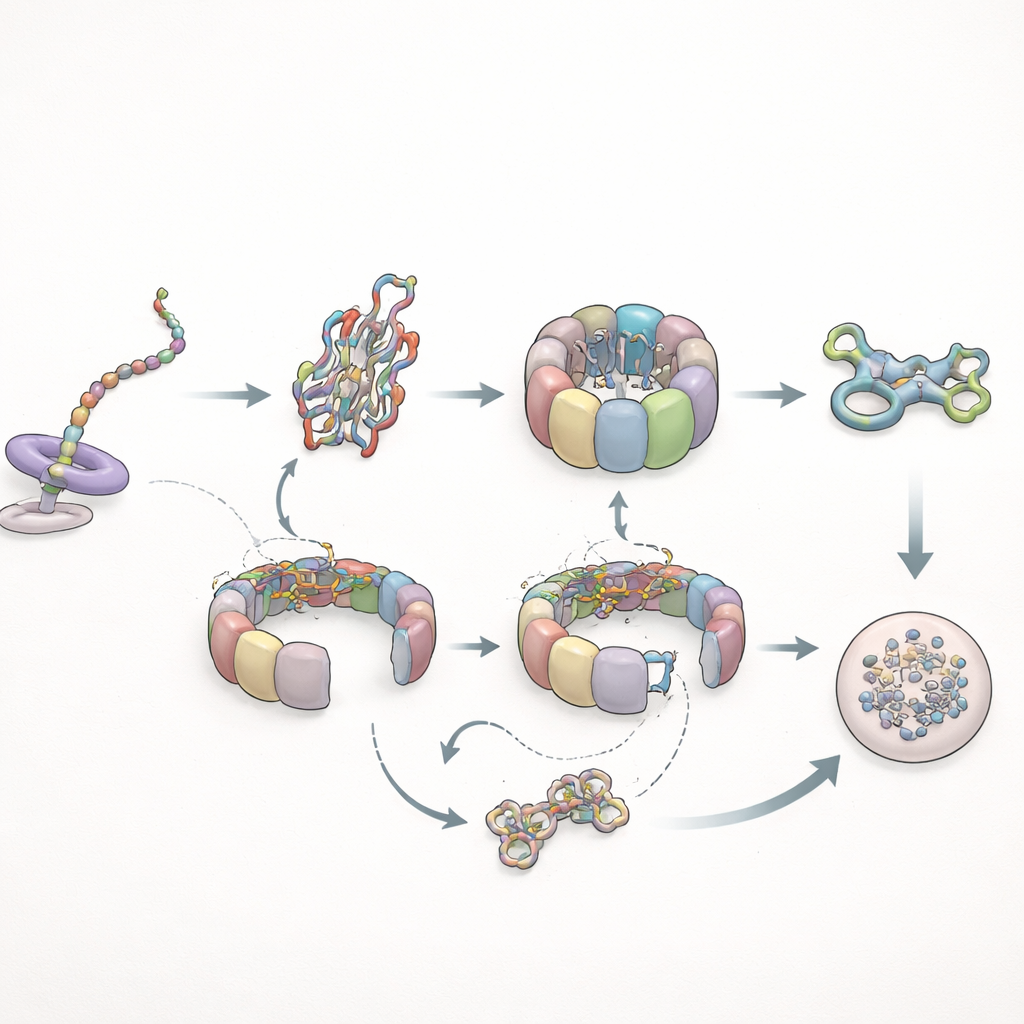
Wanneer vouwen faalt: cycli en opruiming
De auteurs testten vervolgens hoe dit systeem omgaat met een problematische klant: een mutante vorm van actine die bekendstaat om slecht te vouwen. Tijdens eiwitsynthese gedroeg deze mutant zich vrijwel normaal ten opzichte van TRiC maar slaagde er niet in de verlengde prefoldinecontacten te ontwikkelen die bij de gezonde versie werden gezien, wat aangeeft dat subtiele conformationele veranderingen in de groeiende keten bepalen hoe lang prefoldine kan vasthouden. Na synthese veranderde het beeld dramatisch. De mutante actine verbleef veel langer op TRiC—tot enkele keren de normale verblijftijd—en cycliseerde herhaaldelijk door het chaperonine zonder een stabiele gevouwen toestand te bereiken. Uiteindelijk, in plaats van zich bij het cellulaire structurele netwerk aan te sluiten, werd de mutant doorgegeven aan het degradatiemechanisme van de cel. Gelijktijdig werden de interacties van prefoldine frequenter maar korter, en verminderden zijn directe ontmoetingen met TRiC, wat consistent is met TRiC dat meer tijd in een gesloten, omsluitende staat rond de verkeerd gevouwen klant doorbrengt.
Een lokale beschermde zone voor vouwen
Een opvallende observatie was dat TRiC en prefoldine vaak in de buurt van hun klant bleven tussen bindingsrondes in, in plaats van weg te diffunderen in het cytoplasma. Na het loslaten van een eiwit bleef TRiC doorgaans beperkt tot een klein gebied rond de translatieplaats gedurende tot twee seconden, om vervolgens opnieuw te binden aan dezelfde of een naburige keten. De auteurs detecteerden ook kortstondige contacten tussen verschillende TRiC-complexen die afhankelijk waren van voortdurende eiwitsynthese. Samen ondersteunen deze gedragingen het idee van een «beschermde vouwzone»—een losse, dynamische cluster van chaperonnes en translatiemechanismen waarin pas gemaakte eiwitten dicht bij hun helpers worden gehouden en beschermd tegen schadelijke interacties totdat hun lot is bepaald.
Wat dit betekent voor gezonde cellen en ziekte
Simpel gezegd laat dit werk zien dat TRiC en prefoldine functioneren als een wendbaar kwaliteitscontroleduo: ze inspecteren kort vele nieuwe eiwitketens, concentreren hun aandacht naarmate de keten bijna klaar is en voeren snelle vouwcycli uit binnen een kleine lokale bubbel rond het ribosoom. Goed functionerende eiwitten, zoals normaal actine, bereiken over het algemeen hun juiste vorm na meerdere snelle passages door TRiC. Defecte varianten daarentegen raken verstrikt in verlengde cycli en worden uiteindelijk naar afbraak geleid, waarbij ze onderweg chaperonnecapaciteit binden. Deze single-molecuulinzichten helpen verklaren hoe cellen het constante risico van verkeerde vouwing in een drukke omgeving beheersen, en waarom mutaties in zowel klanten als chaperonnes het evenwicht richting ziekte kunnen doen kantelen.
Bronvermelding: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Trefwoorden: eiwitvouwing, moleculaire chaperonnes, TRiC-chaperonine, actinedynamiek, cellulaire proteostase