Clear Sky Science · fr
Dynamiques moléculaires uniques du système chaperonin TRiC in vivo
Comment les cellules empêchent les nouvelles protéines d’avoir des ennuis
Chaque seconde, vos cellules fabriquent des milliers de nouvelles protéines — de petits outils moléculaires qui doivent se plier dans la bonne conformation pour fonctionner. Les protéines mal repliées peuvent encrasser la machinerie cellulaire et contribuer à des maladies allant des troubles neurodégénératifs aux anomalies du développement. Cette étude observe, à l’échelle d’une seule molécule et en temps réel, des cellules humaines vivantes pour voir comment une importante équipe cellulaire de repliement, le chaperonin TRiC et son assistant prefoldin, guide les nouvelles protéines vers la bonne conformation et décide quoi faire lorsque le repliement se passe mal.
Une équipe de contrôle qualité cellulaire en action
À l’intérieur de nos cellules, des protéines d’assistance appelées chaperonnes guident d’autres protéines pendant leur synthèse et leur repliement. TRiC est un grand complexe en forme de baril qui peut enfermer temporairement une chaîne protéique récalcitrante, tandis que prefoldin est un plus petit complexe en forme de tentacules qui livre les clients à TRiC. Des travaux antérieurs, principalement in vitro, ont montré que TRiC peut replier des protéines importantes telles que l’actine et la tubuline. Mais que se passe-t-il dans l’intérieur encombré et animé d’une vraie cellule — à quelle fréquence TRiC et prefoldin rencontrent leurs clients, combien de temps ils les retiennent, et comment ils réagissent aux cas difficiles — est resté peu clair. Les auteurs ont développé une microscopie avancée de suivi de particules uniques dans des cellules humaines vivantes pour suivre des molécules individuelles de TRiC et de prefoldin et leurs rencontres avec des protéines nouvellement synthétisées.
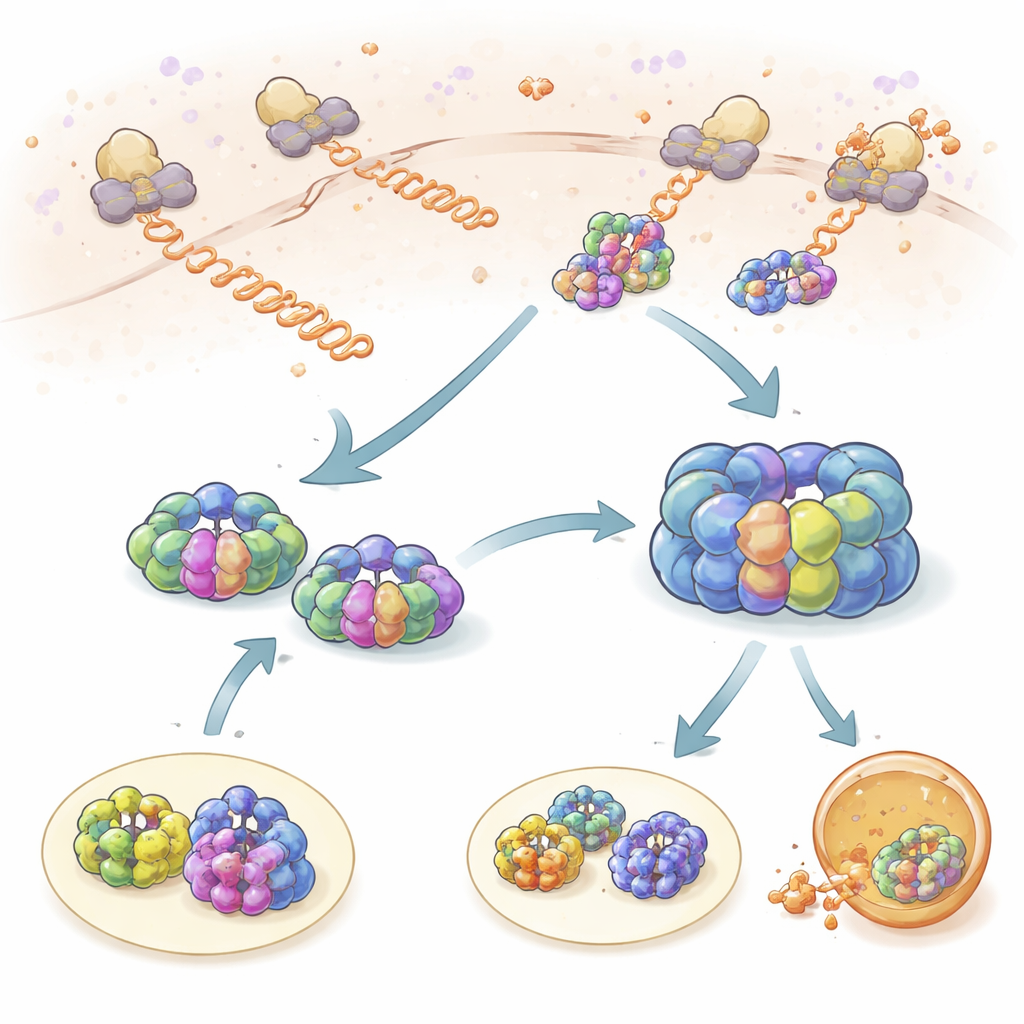
Courtes vérifications pendant la synthèse des protéines
L’équipe a d’abord examiné comment TRiC et prefoldin interagissent avec les chaînes protéiques fraîchement synthétisées qui émergent des ribosomes, les usines à protéines de la cellule. En marquant les ribosomes, TRiC et prefoldin avec des colorants fluorescents différents, ils ont pu observer quand leurs mouvements devenaient liés dans l’espace et le temps. TRiC et prefoldin effleuraient à plusieurs reprises les chaînes naissantes lors d’événements de « sondage » brefs d’environ une seconde. Prefoldin contactait les nouvelles chaînes plus souvent que TRiC, et réduire le niveau de prefoldin diminuait fortement l’accès de TRiC à ces clients, montrant que prefoldin agit comme un recruteur. Grâce au ribosome profiling, les auteurs ont constaté que des centaines de protéines différentes sont surveillées de cette manière, avec un fort chevauchement entre les clients de TRiC et ceux de prefoldin, ce qui souligne que ce partenariat est central pour maintenir une population protéique saine.
Un engagement qui persiste près de la ligne d’arrivée
Pour se concentrer sur un client obligatoire unique, les chercheurs ont suivi l’actine, un élément clé du cytosquelette. Plutôt que de marquer la protéine actine elle-même, ils ont étiqueté son ARN messager, ce qui leur a permis de suivre les sites de synthèse de l’actine. À mesure que la chaîne d’actine s’allongeait, prefoldin et TRiC visitaient plus fréquemment et restaient plus longtemps. Vers la fin de la traduction, prefoldin se liait souvent pendant plusieurs secondes, maintenant des chaînes d’actine presque complètes et aidant à recruter TRiC pour la phase suivante du repliement. Lorsque les chercheurs ont artificiellement ancré de l’actine pleine longueur près du ribosome, ils ont pu observer TRiC l’engager en cycles répétés d’environ 2,5 secondes chacun, en accord avec un processus de repliement en plusieurs étapes. Prefoldin était crucial pour les engagements TRiC plus longs et plus productifs, ce qui suggère qu’il ne se contente pas de livrer les clients mais module également le fonctionnement de TRiC.
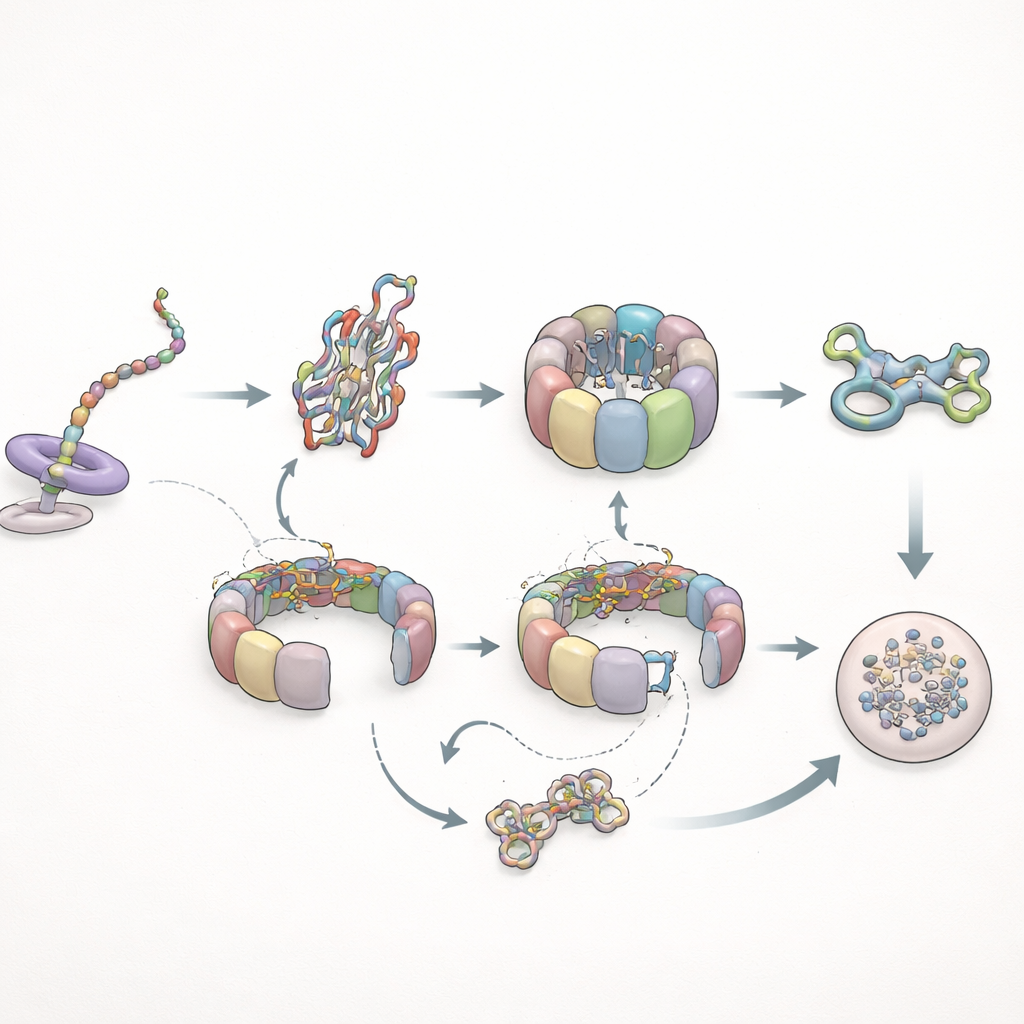
Quand le repliement échoue : cycles et élimination
Les auteurs ont ensuite testé comment ce système gère un client problématique : une forme mutante de l’actine connue pour mal se replier. Pendant la synthèse, cette variante se comportait presque normalement vis-à-vis de TRiC mais n’établissait pas les contacts prolongés avec prefoldin observés pour la version saine, indiquant que des changements conformationnels subtils dans la chaîne en croissance contrôlent la durée pendant laquelle prefoldin peut la maintenir. Après la synthèse, l’histoire a changé de façon spectaculaire. L’actine mutante est restée sur TRiC beaucoup plus longtemps — jusqu’à plusieurs fois la durée normale de résidence — et a cyclé à plusieurs reprises via le chaperonin sans atteindre un état replié stable. Finalement, au lieu d’intégrer le réseau structural de la cellule, la variante mutante a été transférée à la machinerie de dégradation cellulaire. Parallèlement, les interactions de prefoldin sont devenues plus fréquentes mais plus courtes, et ses rencontres directes avec TRiC ont diminué, cohérent avec le fait que TRiC passait plus de temps dans un état fermé, encapsulant le client mal replié.
Une zone protectrice locale pour le repliement
Une observation frappante est que TRiC et prefoldin restaient souvent à proximité de leur client entre les cycles de liaison au lieu de diffuser dans le cytosol. Après avoir relâché une protéine, TRiC demeurait généralement confiné dans une petite région autour du site de traduction pendant jusqu’à deux secondes, puis se liait de nouveau à la même chaîne ou à une chaîne voisine. Les auteurs ont également détecté des contacts transitoires entre différents complexes TRiC dépendant de la synthèse protéique en cours. Ensemble, ces comportements soutiennent l’idée d’une « zone de repliement protégée » — un agrégat lâche et dynamique de chaperonnes et de machinerie de traduction dans lequel les protéines nouvellement synthétisées sont maintenues proches de leurs assistants et protégées des interactions nocives jusqu’à ce que leur sort soit décidé.
Ce que cela signifie pour la santé cellulaire et la maladie
En termes simples, ce travail montre que TRiC et prefoldin forment un duo de contrôle qualité agile : ils inspectent brièvement de nombreuses nouvelles chaînes protéiques, concentrent leur attention à l’approche de l’achèvement de la chaîne, puis effectuent des cycles de repliement rapides au sein d’une petite bulle locale autour du ribosome. Les protéines bien comportées, comme l’actine normale, atteignent généralement leur conformation correcte après plusieurs passages rapides par TRiC. Les variantes défectueuses, en revanche, se retrouvent piégées dans des cycles prolongés et sont finalement orientées vers la dégradation, mobilisant au passage la capacité des chaperonnes. Ces aperçus au niveau de la molécule unique aident à expliquer comment les cellules gèrent le risque permanent de mauvais repliement dans un environnement encombré, et pourquoi des mutations chez les clients ou les chaperonnes peuvent faire basculer l’équilibre vers la maladie.
Citation: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Mots-clés: repliement des protéines, chaperonnes moléculaires, chaperonin TRiC, dynamique de l’actine, protéostasie cellulaire