Clear Sky Science · pt
Dinâmica de molécula única do sistema chaperonina TRiC in vivo
Como as Células Mantêm Novas Proteínas Fora de Problemas
A cada segundo, suas células produzem milhares de novas proteínas — pequenas ferramentas moleculares que precisam dobrar-se na forma exata para funcionar. Proteínas mal dobradas podem entupir a maquinaria celular e contribuir para doenças que vão da neurodegeneração a distúrbios do desenvolvimento. Este estudo observa, dentro de células humanas vivas e ao nível de molécula única, como uma importante equipe de dobra celular — a chaperonina TRiC e sua ajudante prefoldina — guia novas proteínas para a forma correta e decide o que fazer quando a dobra dá errado.
Uma Equipe de Controle de Qualidade Celular em Ação
No interior das células, proteínas auxiliares chamadas chaperonas orientam outras proteínas enquanto são sintetizadas e dobradas. A TRiC é um grande complexo em forma de barril que pode enclausurar temporariamente uma cadeia proteica indisciplinada, enquanto a prefoldina é um complexo menor, com aspecto tentacular, que entrega clientes à TRiC. Trabalhos anteriores, em grande parte em tubos de ensaio, mostraram que a TRiC pode dobrar proteínas importantes, como actina e tubulina. Mas o que ocorre no interior lotado e agitado de uma célula real — com que frequência TRiC e prefoldina encontram seus clientes, quanto tempo os mantêm e como respondem a casos difíceis — permanecia incerto. Os autores desenvolveram microscopia avançada de rastreio de partículas únicas em células humanas vivas para seguir moléculas individuais de TRiC e prefoldina e seus encontros com proteínas recém-sintetizadas.
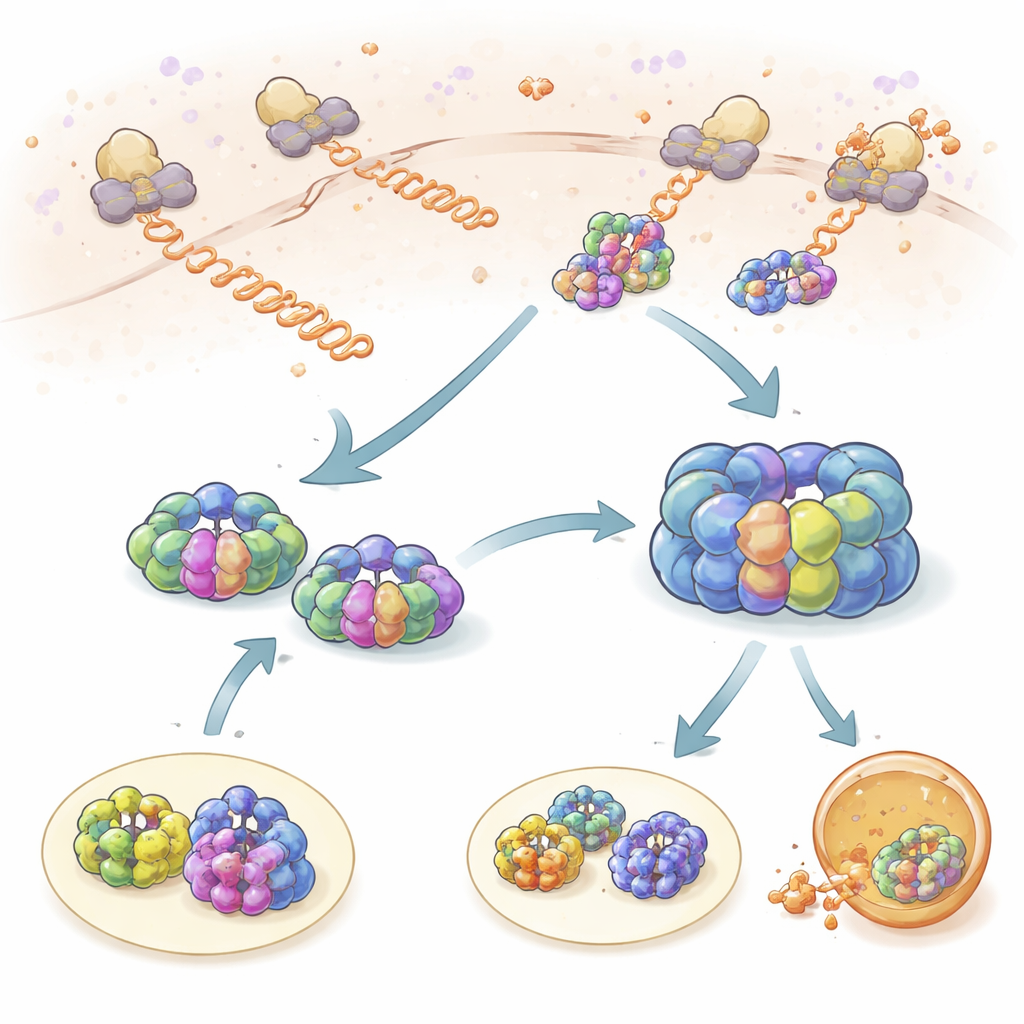
Checagens Breves Enquanto as Proteínas São Produzidas
A equipe primeiro examinou como TRiC e prefoldina interagem com cadeias proteicas recém-sintetizadas à medida que emergem dos ribossomos, as fábricas de proteínas da célula. Ao marcar ribossomos, TRiC e prefoldina com diferentes corantes fluorescentes, eles puderam observar quando seus movimentos se tornavam vinculados no espaço e no tempo. Tanto TRiC quanto prefoldina tocaram repetidamente as cadeias nascente em eventos curtos de “sondagem” durando cerca de um segundo. A prefoldina contactou novas cadeias com mais frequência que a TRiC, e reduzir os níveis de prefoldina diminuiu fortemente o acesso da TRiC a esses clientes, mostrando que a prefoldina atua como recrutadora. Usando perfilagem de ribossomos, os autores descobriram que centenas de proteínas diferentes são monitoradas dessa forma, com grande sobreposição entre os clientes de TRiC e prefoldina, enfatizando que essa parceria é central para manter uma população proteica saudável.
Engajamento Prolongado Perto da Linha de Chegada
Para detalhar um cliente obrigatório, os pesquisadores rastrearam a actina, um bloco construtor-chave do esqueleto celular. Em vez de marcar a proteína actina diretamente, eles rotularam seu RNA mensageiro, permitindo acompanhar os locais onde a actina estava sendo sintetizada. À medida que a cadeia de actina crescia, tanto a prefoldina quanto a TRiC visitavam com mais frequência e permaneciam por mais tempo. Perto do fim da tradução, a prefoldina frequentemente se ligava por vários segundos, segurando cadeias de actina quase completas e ajudando a recrutar a TRiC para a fase seguinte da dobra. Quando os pesquisadores artificialmente ancoraram actina de comprimento total próximo ao ribossomo, puderam observar a TRiC envolvê-la em ciclos repetidos de cerca de 2,5 segundos cada, consistente com um processo de dobra em múltiplas etapas. A prefoldina foi crucial para os engajamentos mais longos e produtivos da TRiC, sugerindo que ela não apenas entrega clientes, mas também ajusta o modo de atuação da TRiC.
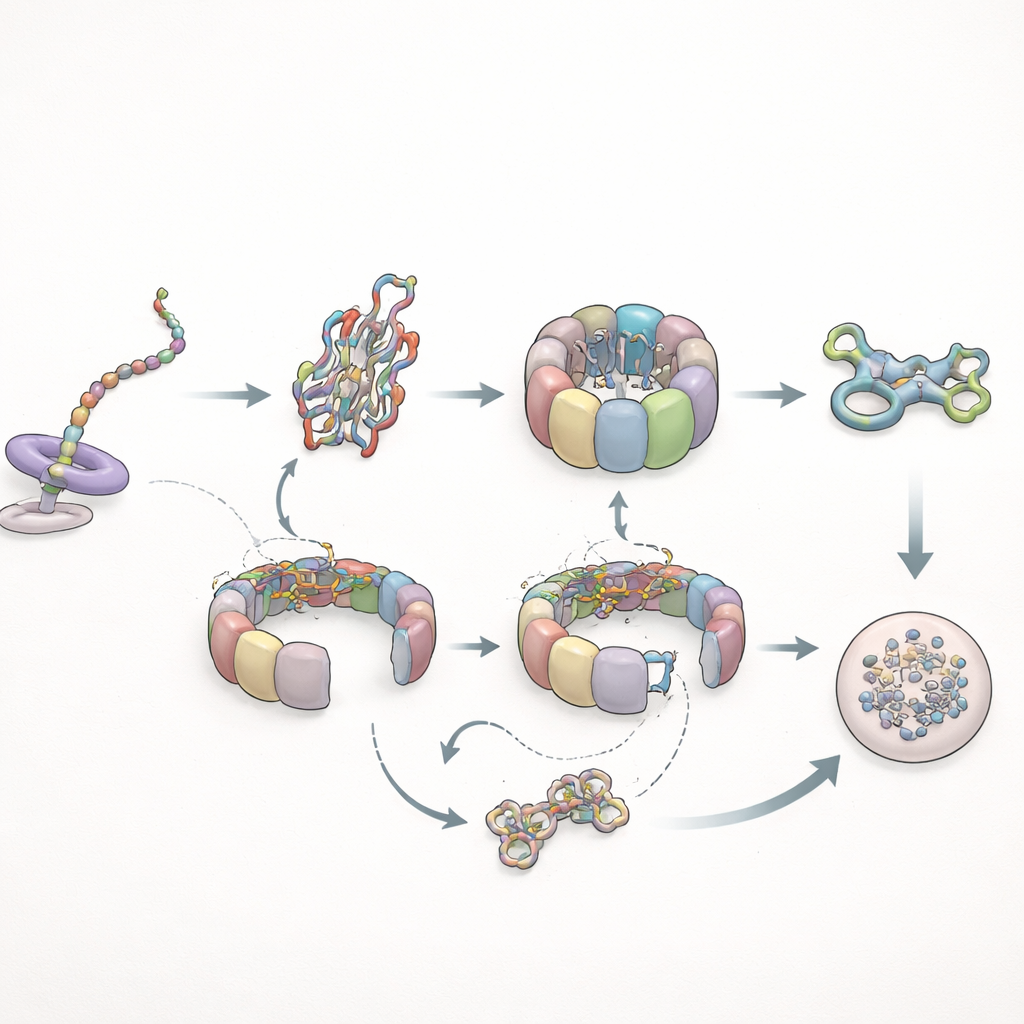
Quando a Dobra Falha, Ciclagem e Limpeza
Os autores então testaram como esse sistema lida com um cliente problemático: uma forma mutante da actina conhecida por se dobrar mal. Durante a síntese proteica, esse mutante comportou-se quase normalmente com a TRiC, mas deixou de desenvolver os contatos prolongados com a prefoldina observados na versão saudável, indicando que mudanças conformacionais sutis na cadeia em crescimento controlam por quanto tempo a prefoldina consegue sustentá-la. Após a síntese, a história mudou dramaticamente. A actina mutante permaneceu na TRiC muito mais tempo — até várias vezes o tempo de residência normal — e ciclou repetidamente pela chaperonina sem atingir um estado dobrado estável. Eventualmente, em vez de integrar a rede estrutural da célula, o mutante foi encaminhado para a maquinaria de degradação celular. Em paralelo, as interações da prefoldina tornaram-se mais frequentes, porém mais curtas, e seus encontros diretos com a TRiC diminuíram, consistente com a TRiC passando mais tempo em um estado fechado, encapsulando o cliente mal dobrado.
Uma Zona Protetora Local para a Dobra
Uma observação marcante foi que TRiC e prefoldina frequentemente permaneciam perto de seu cliente entre rodadas de ligação, em vez de difundir-se para o citoplasma em massa. Após liberar uma proteína, a TRiC tipicamente permanecia confinada dentro de uma pequena região ao redor do sítio de tradução por até dois segundos, e então se ligava novamente à mesma cadeia ou a uma vizinha. Os autores também detectaram contatos transitórios entre diferentes complexos TRiC que dependiam da síntese proteica em curso. Em conjunto, esses comportamentos sustentam a ideia de uma “zona de dobra protegida” — um aglomerado frouxo e dinâmico de chaperonas e maquinaria de tradução no qual proteínas recém-sintetizadas são mantidas próximas a seus ajudantes e protegidas de interações prejudiciais até que seu destino seja decidido.
O Que Isso Significa para Células Saudáveis e Doença
Em termos simples, este trabalho mostra que TRiC e prefoldina atuam como uma dupla ágil de controle de qualidade: inspecionam brevemente muitas cadeias proteicas novas, concentram sua atenção à medida que a cadeia se aproxima da conclusão e então executam ciclos rápidos de dobra dentro de uma pequena bolha local ao redor do ribossomo. Proteínas bem comportadas, como a actina normal, geralmente atingem sua forma correta após múltiplas passagens rápidas pela TRiC. Variantes defeituosas, por outro lado, ficam presas em ciclos prolongados e são, em última instância, direcionadas à degradação, prendendo a capacidade das chaperonas no processo. Essas percepções em nível de molécula única ajudam a explicar como as células gerenciam o risco constante de má dobra em um ambiente lotado e por que mutações em clientes ou chaperonas podem deslocar o equilíbrio em direção à doença.
Citação: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Palavras-chave: dobra de proteínas, chaperonas moleculares, chaperonina TRiC, dinâmica da actina, proteostase celular