Clear Sky Science · it
Dinâmica a singola molecola del sistema chaperoninico TRiC in vivo
Come le cellule proteggono le nuove proteine dai problemi
Ogni secondo, le tue cellule producono migliaia di nuove proteine—piccoli strumenti molecolari che devono ripiegarsi nella forma corretta per funzionare. Le proteine mal ripiegate possono intasare la macchina cellulare e contribuire a malattie che vanno dalla neurodegenerazione a disturbi dello sviluppo. Questo studio osserva all’interno di cellule umane vive a livello di singola molecola per vedere, in tempo reale, come un importante sistema cellulare di ripiegamento, il chaperonin TRiC e il suo aiutante prefoldina, accompagnino le nuove proteine verso la forma corretta e cosa succeda quando il ripiegamento fallisce.
Una squadra di controllo qualità cellulare al lavoro
All’interno delle nostre cellule, proteine helper speciali chiamate chaperoni guidano altre proteine mentre vengono sintetizzate e ripiegate. TRiC è un grande complesso a forma di barile che può inglobare temporaneamente una catena proteica ribelle, mentre la prefoldina è un complesso più piccolo, a tentacoli, che consegna i clienti a TRiC. Studi precedenti, per lo più in provetta, avevano mostrato che TRiC può ripiegare proteine importanti come actina e tubulina. Ma cosa accade nell’ambiente affollato e dinamico di una vera cellula—con quale frequenza TRiC e prefoldina incontrano i loro clienti, quanto a lungo li trattengono e come rispondono ai casi difficili—era rimasto poco chiaro. Gli autori hanno sviluppato una microscopia avanzata di tracciamento a singole particelle in cellule umane vive per seguire molecole individuali di TRiC e prefoldina e i loro incontri con proteine appena sintetizzate.
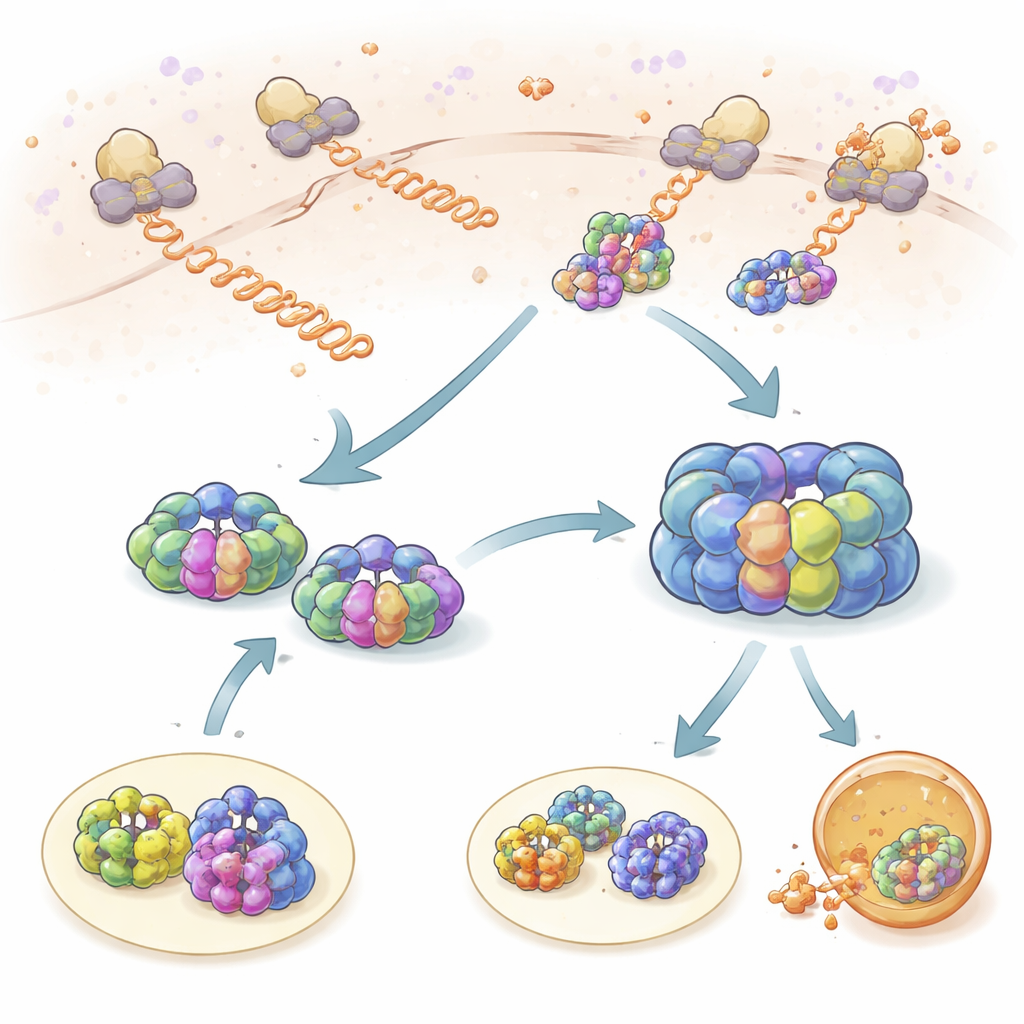
Controlli brevi mentre le proteine vengono sintetizzate
Il team ha prima esaminato come TRiC e prefoldina interagiscono con catene proteiche appena sintetizzate man mano che emergono dai ribosomi, le fabbriche proteiche della cellula. Marcando ribosomi, TRiC e prefoldina con diversi coloranti fluorescenti, hanno potuto osservare quando i loro movimenti diventavano collegati nello spazio e nel tempo. Sia TRiC sia la prefoldina toccavano ripetutamente le catene nascenti in brevi eventi di “sondaggio” della durata di circa un secondo. La prefoldina contattava le nuove catene più spesso di TRiC, e la riduzione dei livelli di prefoldina ha diminuito nettamente l’accesso di TRiC a questi clienti, dimostrando che la prefoldina funge da reclutatore. Usando il ribosome profiling, gli autori hanno trovato che centinaia di proteine diverse sono monitorate in questo modo, con una forte sovrapposizione tra i clienti di TRiC e quelli della prefoldina, sottolineando che questa collaborazione è centrale per mantenere una popolazione proteica sana.
Coinvolgimenti prolungati vicino alla linea d’arrivo
Per concentrarsi su un singolo cliente obbligato, i ricercatori hanno tracciato l’actina, un mattone chiave dello scheletro cellulare. Invece di marcare direttamente la proteina actina, hanno etichettato il suo RNA messaggero, permettendo di seguire i siti dove l’actina veniva sintetizzata. Man mano che la catena di actina si allungava, sia la prefoldina sia TRiC la visitavano più frequentemente e rimanevano più a lungo. Verso la fine della traduzione, la prefoldina spesso si legava per diversi secondi, trattenendo catene di actina quasi complete e contribuendo a reclutare TRiC per la fase successiva del ripiegamento. Quando i ricercatori hanno artificialmente ancorato actina a lunghezza completa vicino al ribosoma, hanno potuto osservare TRiC impegnarsi in cicli ripetuti di circa 2,5 secondi ciascuno, coerenti con un processo di ripiegamento multistep. La prefoldina è risultata cruciale per gli impegni TRiC più lunghi e più produttivi, suggerendo che non solo consegna i clienti ma regola anche il funzionamento di TRiC.
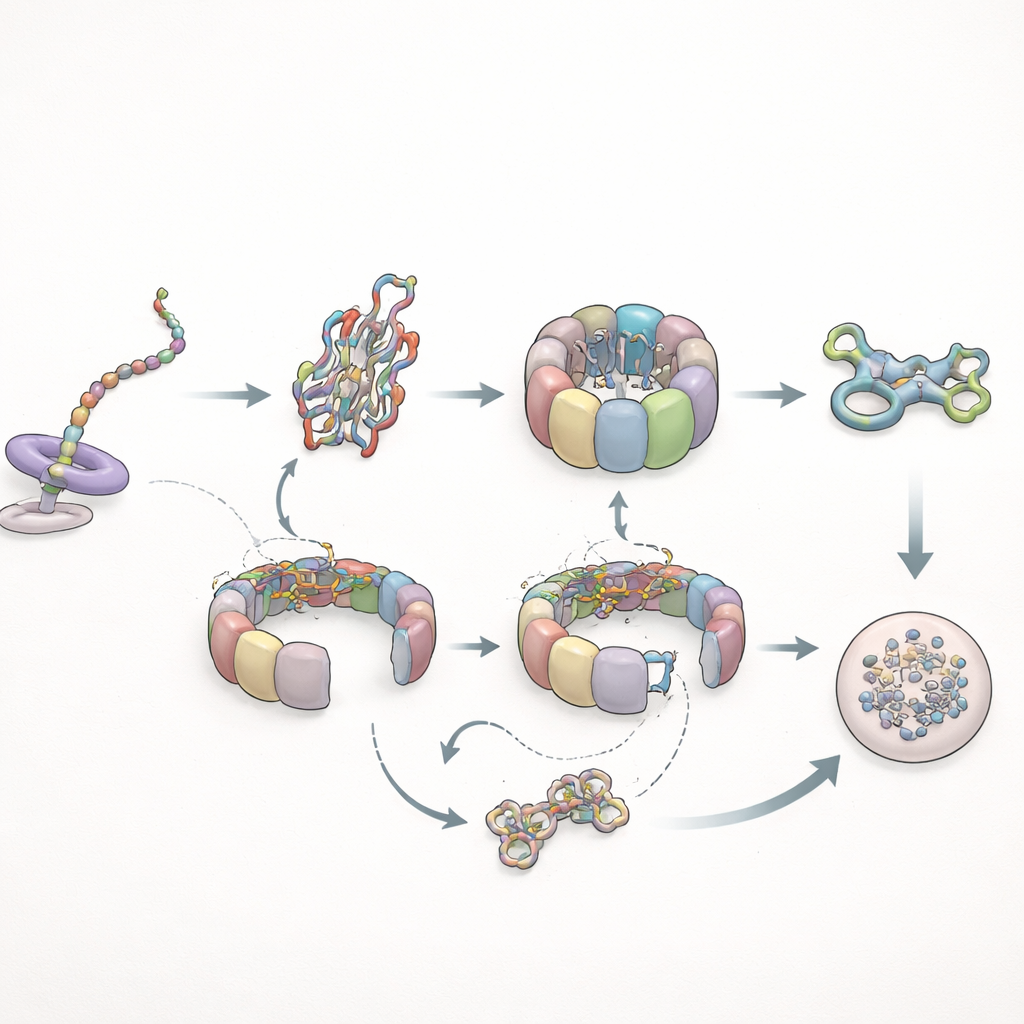
Quando il ripiegamento fallisce: cicli e smaltimento
Gli autori hanno poi testato come questo sistema gestisce un cliente problematico: una forma mutante dell’actina nota per ripiegarsi male. Durante la sintesi proteica, questo mutante si comportava quasi normalmente con TRiC ma non sviluppava i contatti prolungati con la prefoldina osservati nella versione sana, indicando che sottili cambiamenti conformazionali nella catena in crescita controllano per quanto tempo la prefoldina può trattenere. Dopo la sintesi, la situazione cambiava radicalmente. L’actina mutante rimaneva su TRiC molto più a lungo—fino a diverse volte il tempo di permanenza normale—e ciclicamente passava ripetutamente attraverso il chaperonin senza raggiungere uno stato ripiegato stabile. Alla fine, invece di unirsi alla rete strutturale della cellula, il mutante veniva indirizzato alla macchina di degradazione cellulare. Parallelamente, le interazioni della prefoldina diventavano più frequenti ma più brevi, e i suoi incontri diretti con TRiC diminuivano, coerentemente con TRiC che trascorreva più tempo in uno stato chiuso e inglobante attorno al cliente mal ripiegato.
Una zona protetta locale per il ripiegamento
Un’osservazione notevole è stata che TRiC e prefoldina spesso rimanevano nelle vicinanze del loro cliente tra un legame e l’altro invece di diffondersi nel citoplasma. Dopo aver rilasciato una proteina, TRiC tipicamente restava confinato in una piccola regione attorno al sito di traduzione per fino a due secondi, per poi rilegare la stessa o una catena vicina. Gli autori hanno anche rilevato contatti transitori tra diversi complessi TRiC che dipendevano dalla sintesi proteica in corso. Questi comportamenti sostengono l’idea di una “zona protetta di ripiegamento”—un ammasso sciolto e dinamico di chaperoni e macchinari di traduzione in cui le proteine appena fatte sono tenute vicine ai loro aiutanti e schermate da interazioni dannose fino a quando il loro destino non è deciso.
Implicazioni per cellule sane e malattie
In termini semplici, questo lavoro mostra che TRiC e prefoldina agiscono come un duo di controllo qualità agile: ispezionano brevemente molte nuove catene proteiche, concentrano la loro attenzione man mano che la catena si avvicina al completamento e poi eseguono rapidi cicli di ripiegamento all’interno di una piccola bolla locale intorno al ribosoma. Proteine ben comportate, come l’actina normale, generalmente raggiungono la forma corretta dopo molteplici passaggi rapidi attraverso TRiC. Le varianti difettose, al contrario, rimangono intrappolate in cicli prolungati e sono infine indirizzate alla degradazione, impegnando nel frattempo la capacità dei chaperoni. Queste intuizioni a singola molecola aiutano a spiegare come le cellule gestiscano il rischio costante di malripiegamento in un ambiente affollato e perché mutazioni nei clienti o nei chaperoni possano spostare l’equilibrio verso la malattia.
Citazione: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Parole chiave: ripiegamento delle proteine, chaperoni molecolari, chaperonin TRiC, dinamiche dell'actina, proteostasi cellulare