Clear Sky Science · ja
生体内におけるTRiCシャペロニン系の単一分子ダイナミクス
細胞が新しいタンパク質のトラブルを回避する仕組み
あなたの細胞は毎秒何千もの新しいタンパク質を生産しており、それらは機能するために正確な立体構造に折りたたまれる必要があります。誤って折りたたまれたタンパク質は細胞内の機構を詰まらせ、神経変性疾患から発達障害に至るまでさまざまな病態に寄与します。本研究は生きたヒト細胞内で単一分子レベルを直接観察し、主要な折りたたみチームであるTRiCシャペロニンとその補助因子プレフォルジンが、新たに合成されたタンパク質をどのように正しい形へ導き、折りたたみが失敗したときにどのように対応するかをリアルタイムで追います。
働く細胞の品質管理チーム
細胞内ではシャペロンと呼ばれる特殊な補助タンパク質が、翻訳と折りたたみの過程で他のタンパク質を導きます。TRiCは大きな樽状の複合体で、手に負えないポリペプチド鎖を一時的に内部に包み込むことができます。一方プレフォルジンは触手状の小さな複合体で、クライアントをTRiCへ届けます。これまでの主に試験管内での研究は、TRiCがアクチンやチューブリンのような重要なタンパク質を折りたたむことを示してきました。しかし、混雑し活発な実際の細胞内部では、TRiCとプレフォルジンがクライアントにどれほど頻繁に出会い、どれくらいの時間保持し、困難なケースにどう反応するかは不明瞭でした。著者らは生きたヒト細胞での高度な単一粒子追跡顕微鏡法を開発し、個々のTRiCおよびプレフォルジン分子と新生タンパク質との出会いを追跡しました。
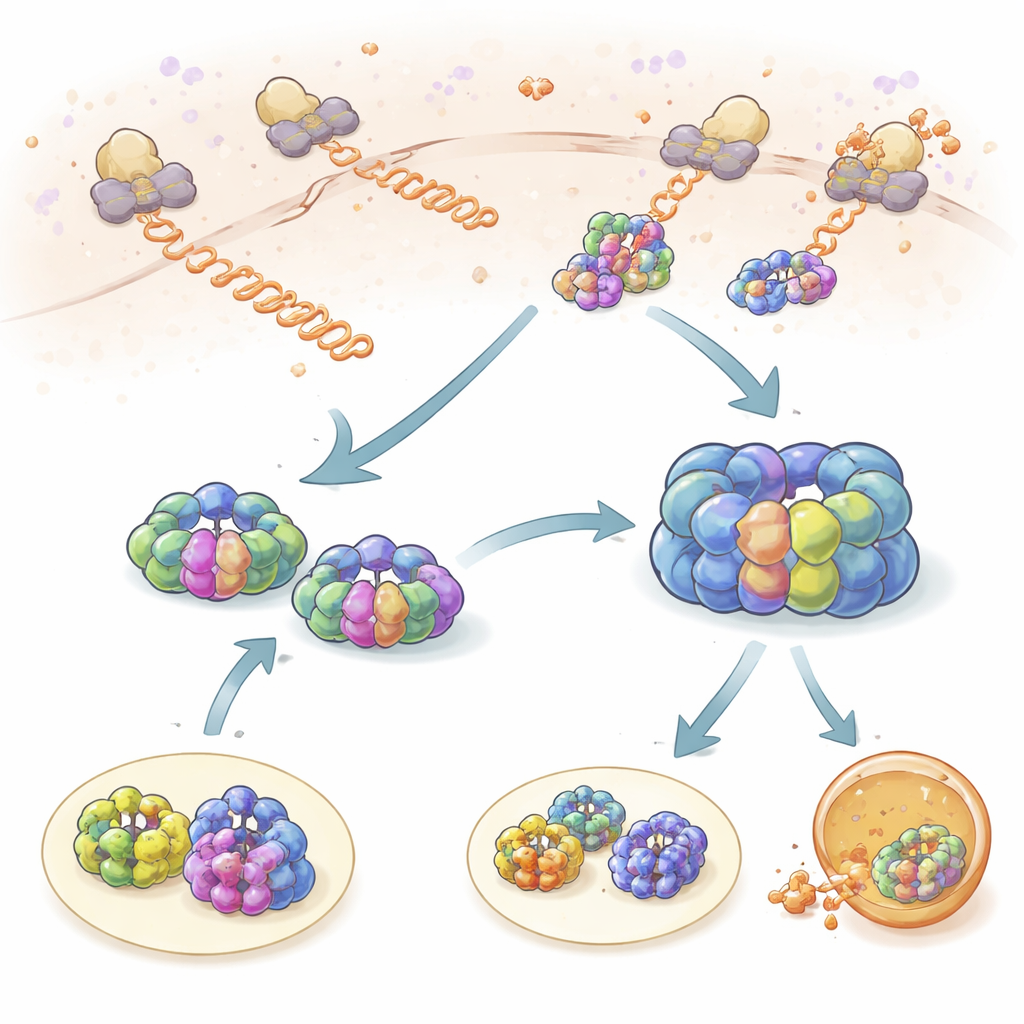
合成中のタンパク質への短いチェック
まず研究チームは、TRiCとプレフォルジンがリボソームから出てくる新生ポリペプチド鎖とどのように相互作用するかを調べました。リボソーム、TRiC、プレフォルジンをそれぞれ異なる蛍光色素で標識することで、それらの動きが空間的・時間的に連動する瞬間を観察できました。TRiCとプレフォルジンはどちらも、新生鎖に対して約1秒程度の短い「プロービング」イベントを繰り返し行っていました。プレフォルジンはTRiCよりも新生鎖と接触する頻度が高く、プレフォルジンの量を減らすとTRiCのクライアントアクセスが著しく低下したため、プレフォルジンはリクルーターとして働くことが示されました。リボソームプロファイリングにより、何百種類ものタンパク質がこのように監視されており、TRiCとプレフォルジンのクライアントに強い重なりがあることが分かり、この協働が健全なタンパク質プールを維持するうえで中心的であることが強調されます。
仕上げ間際での長時間の関与
単一の必須クライアントに焦点を絞るため、研究者らは細胞骨格の主要な構成要素であるアクチンを追跡しました。アクチンタンパク質自体にタグを付ける代わりに、そのメッセンジャーRNAを標識することで、アクチンが合成されている場を追うことができました。ポリペプチド鎖が伸びるにつれて、プレフォルジンとTRiCの訪問頻度は増し、滞在時間も長くなりました。翻訳の終盤近くでは、プレフォルジンが数秒間結合してほぼ完成したアクチン鎖を保持し、次の折りたたみ段階にTRiCをリクルートすることが多く見られました。研究者らが人工的にリボソーム近傍に全長アクチンを固定すると、TRiCが約2.5秒ごとの反復サイクルで関与する様子が観察され、これは多段階の折りたたみ過程と整合します。プレフォルジンはこうしたより長く生産的なTRiCの関与に不可欠であり、単にクライアントを届けるだけでなくTRiCの働き方を調整していることを示唆しています。
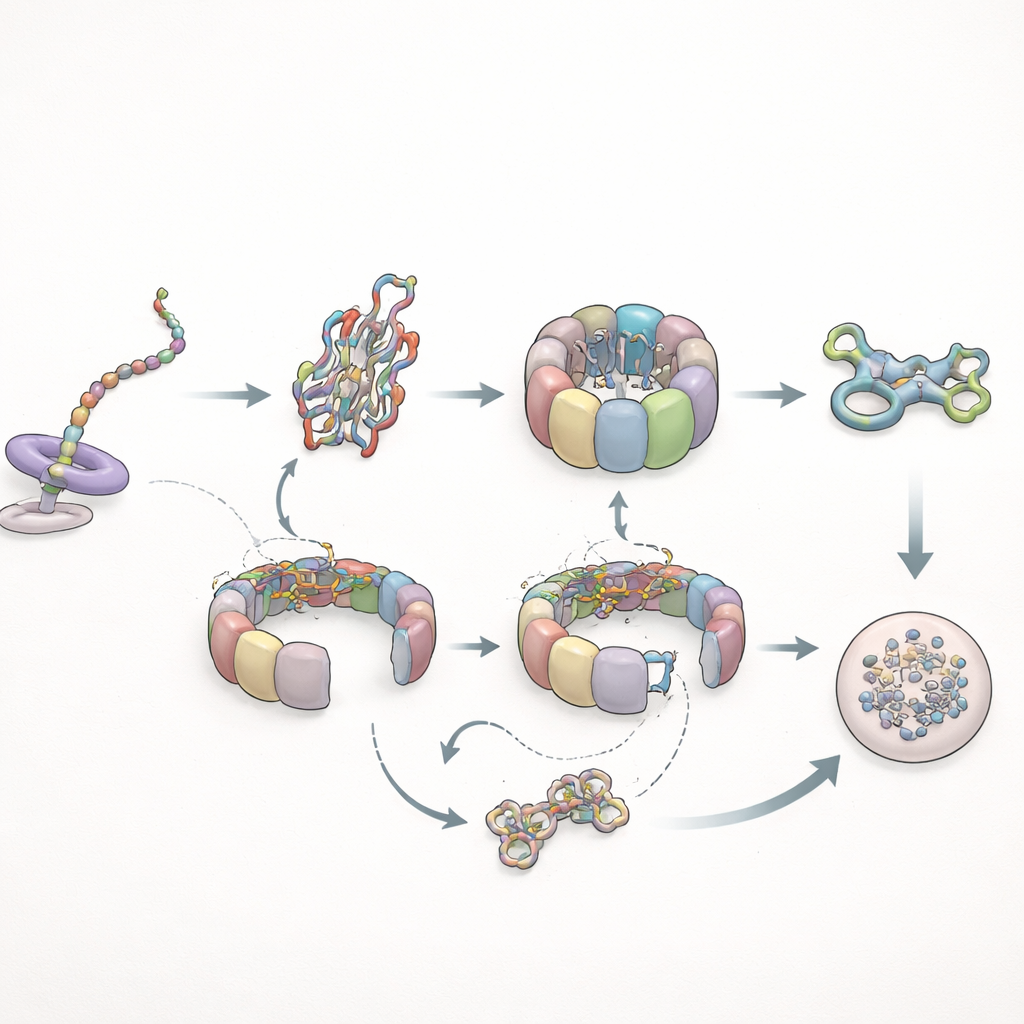
折りたたみが失敗したときのサイクリングと処理
次に著者らは、このシステムが問題のあるクライアント—折りたたみが苦手であることが知られている変異型アクチン—をどのように扱うかを調べました。合成中、この変異体はTRiCとの挙動はほぼ正常に見えましたが、正常なアクチンで見られるような長時間のプレフォルジン接触を発展させませんでした。これは、成長中の鎖の微妙な構造変化がプレフォルジンの保持時間を制御していることを示唆します。しかし合成後の状況は劇的に変わりました。変異型アクチンはTRiC上に通常よりずっと長く留まり—通常の滞在時間の数倍に達することもあり—安定した折りたたみ状態に到達せずにシャペロニン内を繰り返しサイクルしました。最終的に、細胞の構造ネットワークに組み込まれる代わりに、その変異体は分解機構へと渡されました。並行して、プレフォルジンの相互作用はより頻繁になる一方で短くなり、TRiCとの直接的な遭遇は減少しました。これは、TRiCが誤折りたたみクライアントの周囲でより閉鎖的・包摂的な状態にある時間が長くなることと整合します。
折りたたみのための局所的な保護ゾーン
興味深い観察の一つは、TRiCとプレフォルジンが結合サイクルの間に拡散して細胞質へ離れていくのではなく、クライアントの近くにとどまることが多い点でした。タンパク質を放した後もTRiCは通常、翻訳部位の周囲の小さな領域に最大2秒ほど留まり、その後同じ鎖か隣接する鎖に再結合しました。著者らはまた、進行中のタンパク質合成に依存する一時的な異なるTRiC複合体間の接触も検出しました。これらの振る舞いは一緒になって「保護された折りたたみゾーン」という概念を支持します――新生タンパク質が補助因子に近く、望ましくない相互作用から守られ、その運命が決まるまで局所的に保持されるゆるやかで動的なクラスタです。
健康な細胞と疾患への示唆
簡潔に言えば、本研究はTRiCとプレフォルジンが機敏な品質管理の二重奏として働くことを示しています。彼らは多くの新生ポリペプチド鎖を短時間で点検し、鎖が完成に近づくと注意を集中させ、リボソーム周辺の小さな局所バブル内で迅速な折りたたみサイクルを行います。正常なアクチンのように問題なく振る舞うタンパク質は、複数回の短いTRiC通過を経て正しい形に到達します。一方で欠陥のある変異体は長期のサイクルに捕らわれ、最終的に分解へ回されるため、その過程でシャペロンのキャパシティを消費します。これら単一分子レベルの知見は、混雑した環境下で細胞が誤折りたたみの恒常的なリスクをどのように管理しているか、そしてクライアントやシャペロンの変異がなぜ疾患への傾きを生むのかを説明する助けになります。
引用: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
キーワード: タンパク質の折りたたみ, 分子シャペロン, TRiCシャペロニン, アクチン動態, 細胞のプロテオスタシス