Clear Sky Science · tr
TRiC şaperonin sisteminin canlıda tek molekül dinamikleri
Hücreler Yeni Proteinleri Sorundan Nasıl Koruyor
Hücreleriniz her saniye binlerce yeni protein üretiyor—çalışmak için tam olarak doğru biçime katlanmaları gereken küçük moleküler araçlar. Yanlış katlanmış proteinler hücrenin makinelerini tıkayabilir ve nörodejenerasyondan gelişim bozukluklarına kadar çeşitli hastalıklara katkıda bulunabilir. Bu çalışma, canlı insan hücreleri içinde tek molekül düzeyinde gerçek zamanlı olarak bakarak, büyük bir hücresel katlama ekibi olan TRiC şaperonin ile yardımcıları prefoldin’in yeni proteinleri doğru şekle nasıl yönlendirdiğini ve katlanma yanlış gittiğinde ne yaptığını izliyor.
Çalışan Bir Hücresel Kalite Kontrol Ekibi
Hücrelerimizde, şaperon adı verilen özel yardımcı proteinler diğer proteinlerin üretilip katlanması sırasında rehberlik eder. TRiC, dürtüye kaçan bir polipeptid zincirini geçici olarak içine alabilen büyük fıçı biçimli bir kompleks iken, prefoldin müşterileri TRiC’e taşıyan daha küçük, dokunsu bir komplekstir. Önceki çalışmaların çoğu deney tüplerinde TRiC’in aktin ve tubulin gibi önemli proteinleri katlayabildiğini göstermişti. Ancak gerçek hücrenin kalabalık, hareketli iç ortamında—TRiC ve prefoldin’in müşterileriyle ne sıklıkta karşılaştığı, onları ne kadar süre tuttukları ve zor vakalara nasıl tepki verdikleri—belirsizliğini korumuştu. Yazarlar, tekil TRiC ve prefoldin moleküllerini ve bunların yeni sentezlenen proteinlerle karşılaşmalarını takip etmek için gelişmiş tek-parçacık izleme mikroskopisini canlı insan hücrelerinde geliştirdiler.
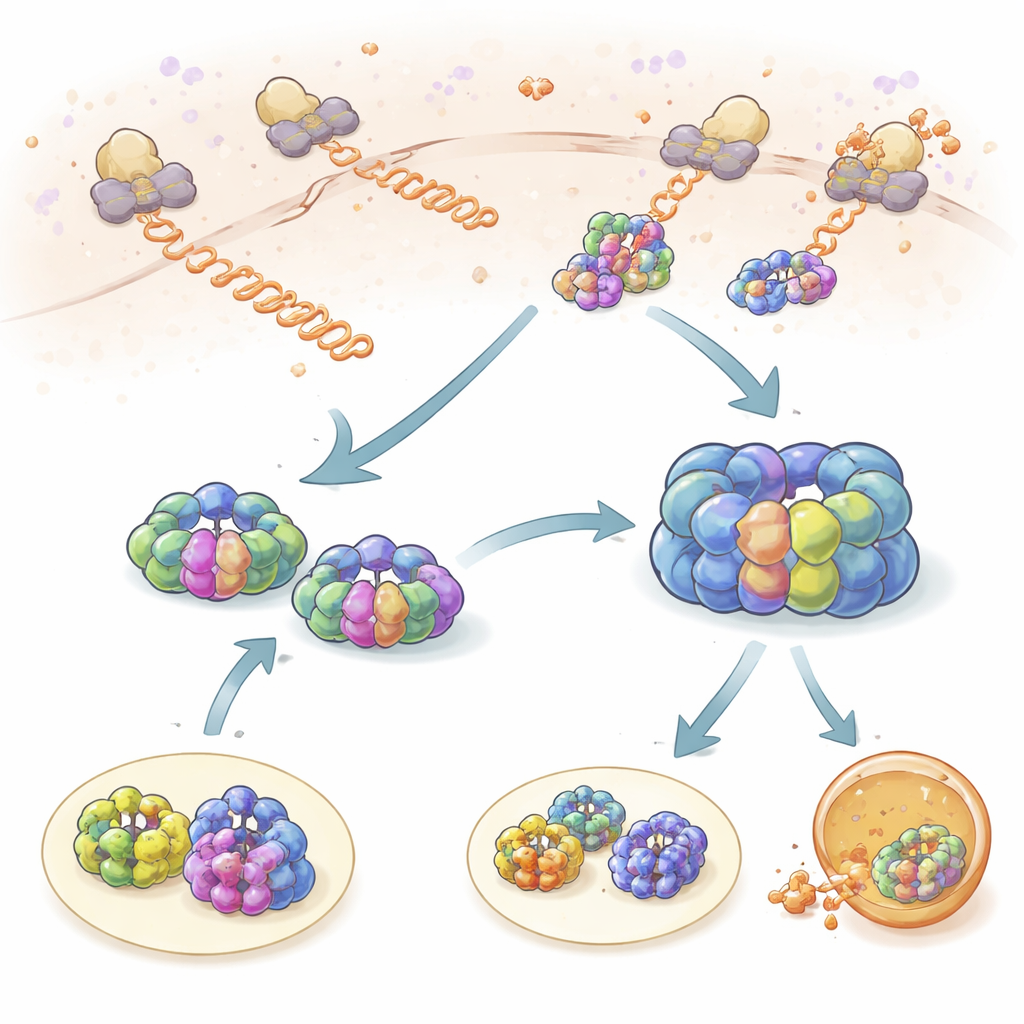
Proteinler Yapılırken Kısa Kontroller
Ekip önce TRiC ve prefoldin’in ribozomlardan, yani hücrenin protein fabrikalarından çıkan taze sentezlenmiş polipeptid zincirleriyle nasıl etkileştiğine baktı. Ribozomları, TRiC’i ve prefoldin’i farklı floresan boyalarla etiketleyerek hareketlerinin ne zaman uzay ve zamanda bağlantılı hale geldiğini izleyebildiler. Hem TRiC hem de prefoldin, yaklaşık bir saniye süren kısa “probing” olaylarıyla yeni zincirlere tekrar tekrar temas etti. Prefoldin yeni zincirlere TRiC’den daha sık temas etti ve prefoldin seviyeleri düşürüldüğünde TRiC’in bu müşterilere erişimi keskin şekilde azaldı; bu da prefoldin’in bir toplayıcı (recruiter) olarak davrandığını gösteriyor. Ribozom profilleme kullanılarak, yüzlerce farklı proteinin bu şekilde izlendiği ve TRiC ile prefoldin müşterileri arasında güçlü bir örtüşme olduğu bulundu; bu ortak çalışmanın sağlıklı bir protein popülasyonunu korumada merkezi olduğunu vurguluyor.
Bitime Yakın Süreklilik Gösteren Bağlanma
Tek bir zorunlu müşteriye daha yakından bakmak için araştırmacılar hücre iskeletinin temel yapı taşı olan aktini izlediler. Aktin proteinini doğrudan etiketlemek yerine, onun haberci RNA’sını (mRNA) işaretleyerek aktinin sentezlendiği yerleri takip ettiler. Aktin zinciri uzadıkça, hem prefoldin hem de TRiC daha sık ziyaret etti ve daha uzun süre kaldı. Çeviri sonuna yaklaşıldığında prefoldin sıklıkla birkaç saniye bağlı kalarak neredeyse tamamlanmış aktin zincirlerini tutuyor ve bir sonraki katlanma aşaması için TRiC’i işe alıyordu. Araştırmacılar tam uzunlukta aktini yapay olarak ribozoma yakın bağladıklarında, TRiC’in onu her biri yaklaşık 2,5 saniye süren tekrar eden döngülerle işlediğini gördüler; bu, çok aşamalı bir katlanma süreciyle uyumlu. Prefoldin daha uzun ve daha verimli TRiC etkileşimleri için kritikti; bu da onun sadece müşterileri teslim etmekle kalmayıp TRiC’in işleyişini de ayarladığını düşündürüyor.
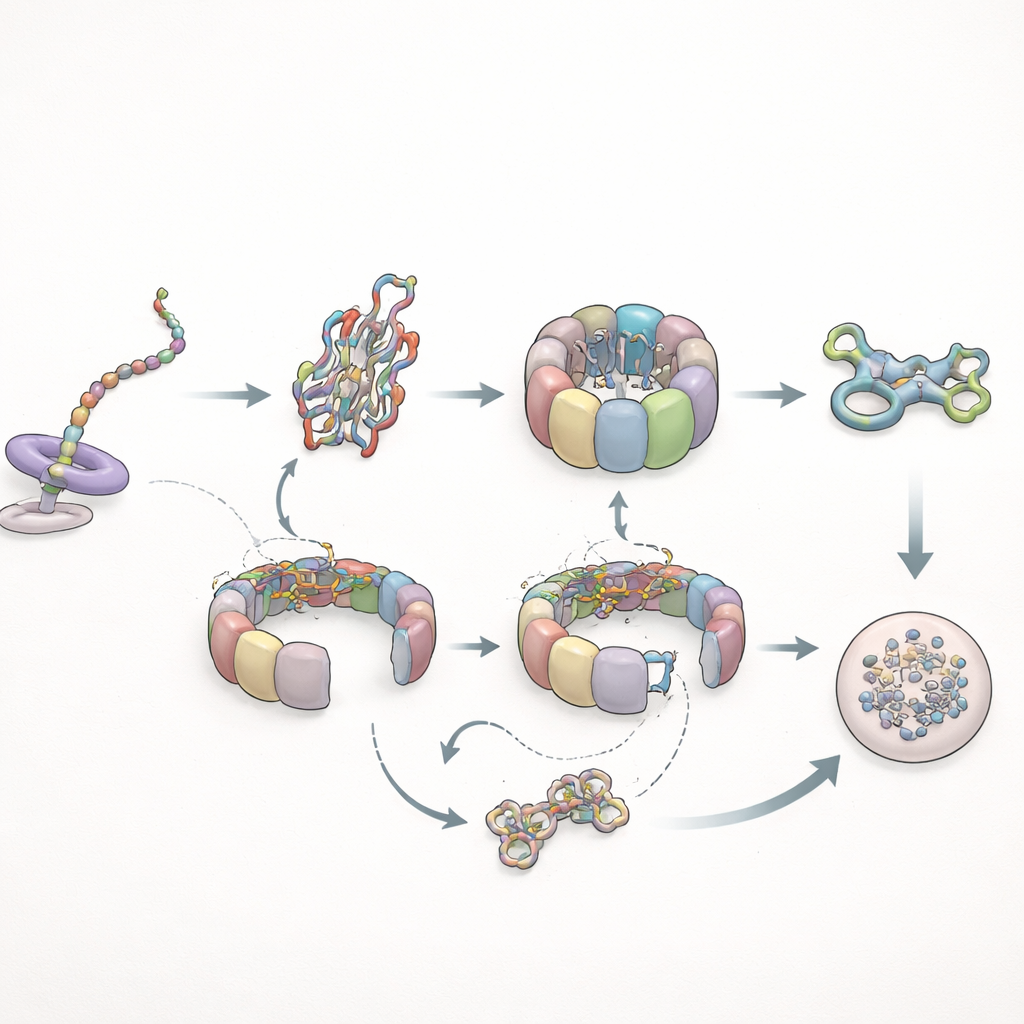
Katlanma Başarısız Olunca: Döngüler ve Temizlik
Yazarlar sonra bu sistemin problemli bir müşteriyle nasıl başa çıktığını test ettiler: kötü katlanan bir aktin mutantı. Protein sentezi sırasında bu mutant TRiC ile neredeyse normal davranıyordu ama sağlıklı versiyonda görülen uzun prefoldin temasları gelişmedi; bu, uzayan zincirdeki ince konformasyonel farklılıkların prefoldin’in tutma süresini kontrol ettiğini gösteriyor. Sentez sonrası hikâye dramatik biçimde değişti. Mutant aktin TRiC üzerinde çok daha uzun kaldı—normal konaklama süresinin birkaç katına kadar—ve katlanmış kararlı bir duruma ulaşamadan şaperon içinde tekrarlayan döngülerden geçti. Sonunda, hücrenin yapısal ağına katılmak yerine mutant, hücrenin parçalama (degradasyon) makinelerine teslim edildi. Paralel olarak, prefoldin’in etkileşimleri daha sık fakat daha kısa oldu ve TRiC ile doğrudan karşılaşmaları azaldı; bu da TRiC’in yanlış katlanmış müşterinin etrafında daha uzun süre kapalı, kapsayıcı bir durumda kaldığını destekliyor.
Katlanma İçin Yerel Bir Koruyucu Bölge
Çarpıcı bir gözlem, TRiC ve prefoldin’in bağlanma turlarının arasında kütle sitoplazmaya doğru yayılmak yerine müşterilerinin yakınında beklemeyi sık sık tercih etmesiydi. Bir proteini serbest bıraktıktan sonra TRiC tipik olarak çeviri bölgesi etrafında küçük bir bölgede iki saniyeye kadar sınırlı kaldı ve ardından aynı veya komşu zincire yeniden bağlandı. Yazarlar ayrıca devam eden protein sentezine bağlı olan farklı TRiC kompleksleri arasında geçici temaslar tespit ettiler. Birlikte, bu davranışlar “korunmuş katlanma bölgesi” fikrini destekliyor—yeni üretilen proteinlerin yardımcılarına yakın tutulduğu ve kaderi belirlenene kadar zararlı etkileşimlerden korunmuş olduğu gevşek, dinamik bir şaperon ve çeviri makine kümesi.
Sağlıklı Hücreler ve Hastalık İçin Anlamı
Basitçe söylemek gerekirse, bu çalışma TRiC ve prefoldin’in çevik bir kalite kontrol ikilisi olarak davrandığını gösteriyor: birçok yeni protein zincirini kısa süreliğine inceliyorlar, zincir tamamlanmaya yakın dikkatlerini yoğunlaştırıyorlar ve sonra ribozom çevresindeki küçük lokal balon içinde hızlı katlanma döngüleri çalıştırıyorlar. Normal davranan proteinler, örneğin sağlıklı aktin, genellikle TRiC’ten geçen birkaç hızlı geçişten sonra doğru şekline ulaşır. Buna karşılık hatalı varyantlar uzun döngülere takılıp kalır ve nihayetinde degradasyona yönlendirilir; bu süreç şaperon kapasitesini meşgul eder. Bu tek-molekül içgörüleri, hücrelerin kalabalık bir ortamda yanlış katlanma riskini nasıl yönettiğini ve müşteri veya şaperonlardaki mutasyonların dengeyi hastalığa nasıl kaydırabileceğini anlamaya yardımcı oluyor.
Atıf: Li, R., Dalheimer, N., Müller, M.B.D. et al. Single-molecule dynamics of the TRiC chaperonin system in vivo. Nature 652, 481–489 (2026). https://doi.org/10.1038/s41586-025-10073-3
Anahtar kelimeler: protein katlanması, moleküler şaperonlar, TRiC şaperonin, aktin dinamikleri, hücresel proteostaz