Clear Sky Science · zh
ZFTA–RELA 融合型室管膜瘤通过产生它康酸来表观遗传学性地驱动融合基因表达
为何这一脑癌研究重要
室管膜瘤是罕见但侵袭性的脑肿瘤,常见于儿童和年轻成人。对许多患者而言,手术和放疗可以在一段时间内控制病情,但很少能治愈。本研究揭示了这一常见亚型肿瘤的一个意想不到弱点:它们依赖一种鲜为人知的分子——它康酸,来维持主要致癌基因的持续开启。研究者通过追踪肿瘤如何合成并利用这种分子,揭示了未来药物可能切断这些肿瘤生存途径的若干新方法。
脑内的危险融合基因
在脑上部出现的室管膜瘤中,超过一半携带一种称为 ZFTA–RELA 的基因融合。单独看时,这两个原始基因并无害处,但融合后产生一个强效的致癌驱动因子,会进入细胞核并重塑 DNA 的读取方式。迄今为止,大多数关于 ZFTA–RELA 的研究集中在其基因调控功能上。本研究提出了一个不同的问题:该融合是否也会以可用于治疗的方式重编程肿瘤的代谢网络——即为能量和构建块提供原料的化学反应网络?
被劫持的巨噬细胞分子
研究团队使用携带该融合的工程化小鼠脑干细胞、来源于病人的肿瘤细胞及小鼠模型,对数百种代谢物进行了谱分析。其中一种代谢物明显突出:它康酸,这是一种在感染时由称为巨噬细胞的免疫细胞产生的分子。肿瘤细胞通过一种名为 ACOD1 的酶大量生成它康酸,而 ACOD1 的水平与 ZFTA–RELA 同步波动。下调 ACOD1 或用小分子抑制它对融合阳性细胞具有毒性并能在小鼠体内缩小肿瘤,而外加它康酸则可以恢复肿瘤生长。这些结果表明,癌细胞已经挪用了一个免疫细胞通路以维持自身生存。 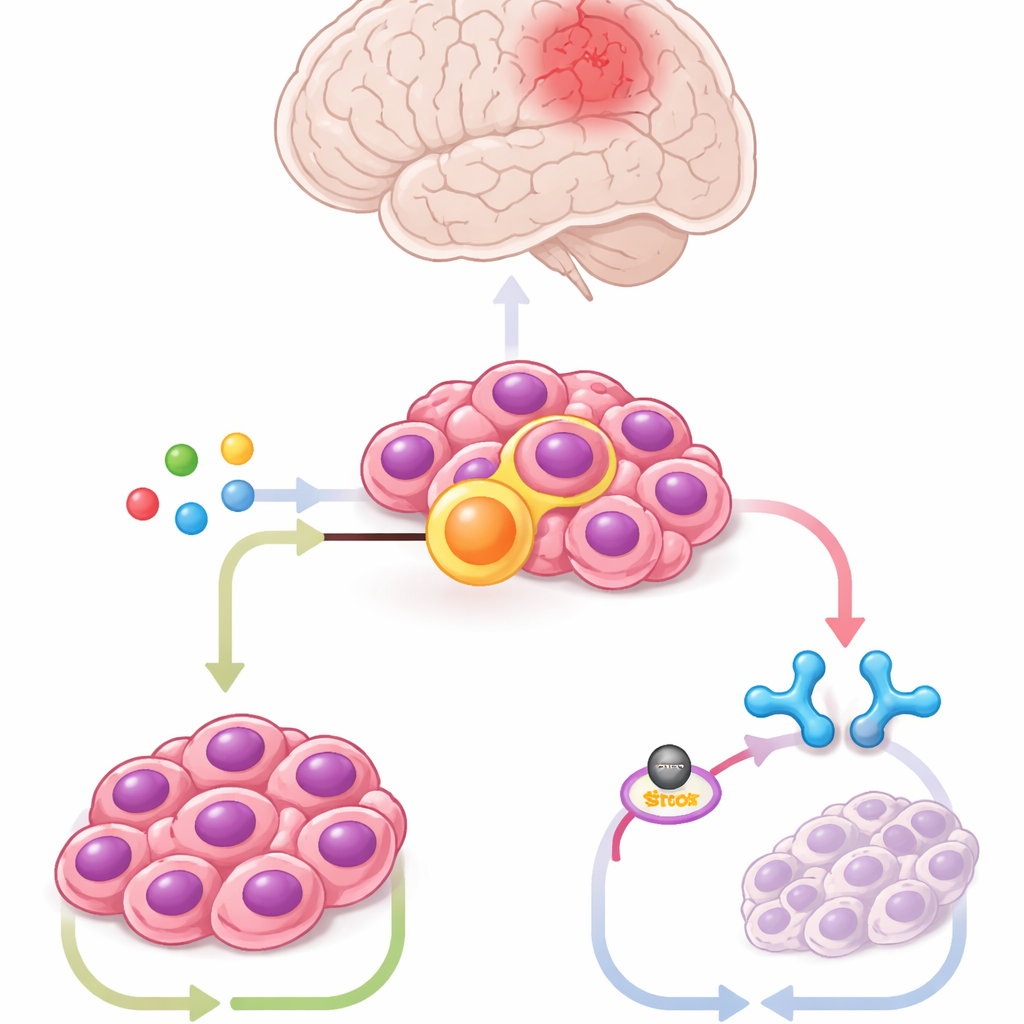
肿瘤基因调控中的自我强化回路
为什么它康酸如此重要?答案在于表观遗传学——存在于包裹 DNA 的蛋白上的化学标记,这些标记决定了哪些基因处于活跃状态。作者发现它康酸抑制了一类去甲基化酶(KDM5),这类酶通常去除组蛋白上的一种激活性标记 H3K4me3。当 KDM5 被抑制时,H3K4me3 在组蛋白上积累,特别是在 ZFTA 基因的关键调控区域(这些区域构成 ZFTA–RELA 融合的一部分)上。这种标记的增加提升了融合基因的转录,形成一个前馈放大回路:ZFTA–RELA 激活 ACOD1,ACOD1 产生它康酸,而它康酸又增强 ZFTA–RELA 的表达。破坏 ACOD1 或模拟 KDM5 活性可以打破这一回路,降低融合蛋白水平,并在多个模型中减缓肿瘤生长。
驱动融合的燃料是谷氨酰胺
研究进一步追踪肿瘤从何处获取合成它康酸的原料。通过向细胞提供用重碳标记的谷氨酰胺和葡萄糖,研究者显示大部分它康酸的碳骨架来自谷氨酰胺。ZFTA–RELA 肿瘤过度表达谷氨酰胺转运蛋白和谷氨酰胺酶,并表现出激活的 PI3K–AKT–mTOR 信号通路——这一通路已知能驱动谷氨酰胺利用。与此同时,融合通过表观遗传学方式沉默了 PTEN,这一关键抑癌基因通常对该信号通路起制衡作用。结果是代谢被重接线,增强谷氨酰胺摄取,将其引入细胞能量代谢循环,并将部分流向它康酸的合成,全部目的都是维持高水平的融合驱动因子。 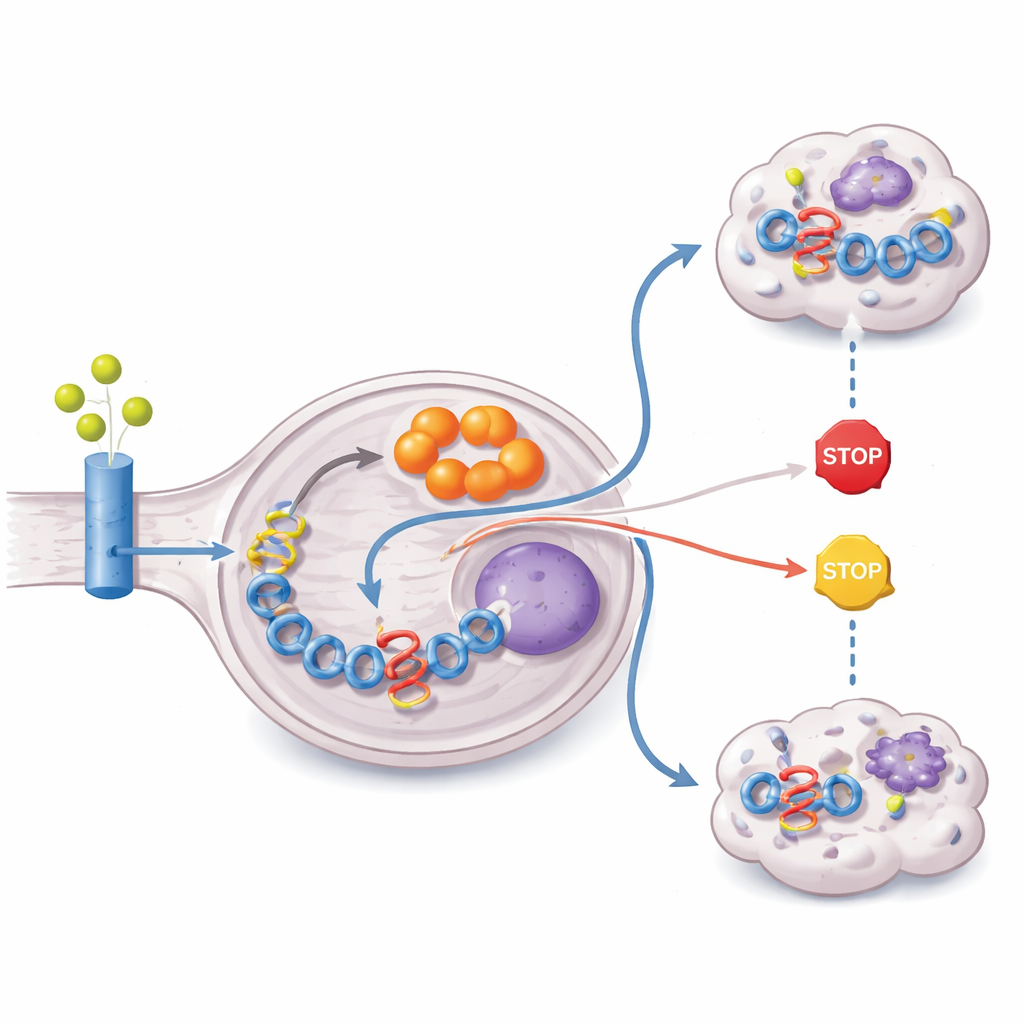
打击肿瘤的进食来源
由于这一回路包含若干独立步骤,因此提供了多个药物靶点。作者测试了阻断谷氨酰胺摄入、抑制谷氨酰胺酶、抑制 ACOD1 或抑制 PI3K–mTOR 通路的化合物,以及一种能穿透大脑的谷氨酰胺拮抗剂 JHU‑083。与其他室管膜瘤亚型相比,融合阳性细胞对这些药物更加敏感,且经治疗的小鼠寿命更长、肿瘤更小。尤其显著的是,抑制 ACOD1 或将谷氨酰胺拮抗与 PI3K–mTOR 抑制联合使用,不仅减少了原发性脑肿瘤,还在小鼠模型中预防或消除了难以治疗的脊髓转移灶。
对患者和家庭的意义
对非专业读者来说,关键信息是这些室管膜瘤对一种由自身形成的特定代谢回路上瘾。它们劫持了一种免疫细胞代谢物——它康酸——以及一种常见营养物质谷氨酰胺,以维持其主要致癌基因处于开启状态。通过从头到尾描绘这一回路,研究指出了若干已有或新兴的药物类别——针对谷氨酰胺利用、ACOD1 或 PI3K–mTOR 信号——这些药物可能被组合使用以选择性削弱 ZFTA–RELA 肿瘤,同时尽量保护正常脑组织。尽管这些结果仍处于临床前阶段,尚未准备好常规应用,但它们为一种目前缺乏有效治疗方案的儿童脑肿瘤指明了清晰的靶向治疗路径。
引用: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
关键词: 室管膜瘤, 脑肿瘤代谢, 它康酸, 谷氨酰胺依赖, 表观遗传学治疗