Clear Sky Science · nl
ZFTA–RELA-ependymomen maken itaconaat om fusie-expressie epigenetisch aan te sturen
Waarom dit hersenkankerverhaal ertoe doet
Ependymomen zijn zeldzame maar agressieve hersentumoren die vaak kinderen en jongvolwassenen treffen. Bij veel patiënten kunnen chirurgie en bestraling de ziekte enige tijd onder controle houden, maar ze genezen zelden. Deze studie onthult een verrassende zwakte in één veelvoorkomend subtype van deze tumoren: ze zijn afhankelijk van een weinig bekend molecuul, itaconaat, om hun belangrijkste kankerverwekkende gen aan te houden. Door na te gaan hoe de tumor dit molecuul maakt en gebruikt, tonen de onderzoekers verschillende nieuwe manieren waarop toekomstige geneesmiddelen deze kankers mogelijk kunnen uitschakelen.
Een gevaarlijke fusie in de hersenen
Meer dan de helft van de ependymomen die in het bovenste deel van de hersenen ontstaan, draagt een genetische samensmelting genaamd ZFTA–RELA. Op zichzelf zijn de twee oorspronkelijk genen onschuldig, maar wanneer ze samensmelten vormen ze een krachtige kankeraanjager die naar de celkern verhuist en herprogrammeren van DNA‑aflezing veroorzaakt. Tot nu toe richtte het meeste werk rond ZFTA–RELA zich op zijn rol in genregulatie. De nieuwe studie stelde een andere vraag: herschikt deze fusie ook het metabolisme van de tumor — het netwerk van chemische reacties dat energie en bouwstenen levert — op manieren die therapie mogelijk maken?
Een macrofaagmolecuul dat naar de duistere kant gaat
Met behulp van muis hersenstamcellen die zo waren aangepast dat ze de fusie dragen, patiëntafgeleide tumorcellen en muismodellen profilen de onderzoekers honderden metabolieten. Eén metaboliet sprong er scherp uit: itaconaat, een molecuul dat normaal door immuuncellen genaamd macrofagen wordt geproduceerd tijdens infectie. De tumorcellen maakten grote hoeveelheden itaconaat via een enzym genaamd ACOD1, waarvan de niveaus meeklonken met die van ZFTA–RELA. Het onderdrukken van ACOD1 of het blokkeren ervan met kleine moleculen was toxisch voor fusie‑positieve cellen en deed tumoren bij muizen krimpen, terwijl het toevoegen van extra itaconaat de tumorengroei redde. Deze resultaten tonen aan dat de kanker een immuuncelroute heeft gekaapt voor zijn eigen overleving. 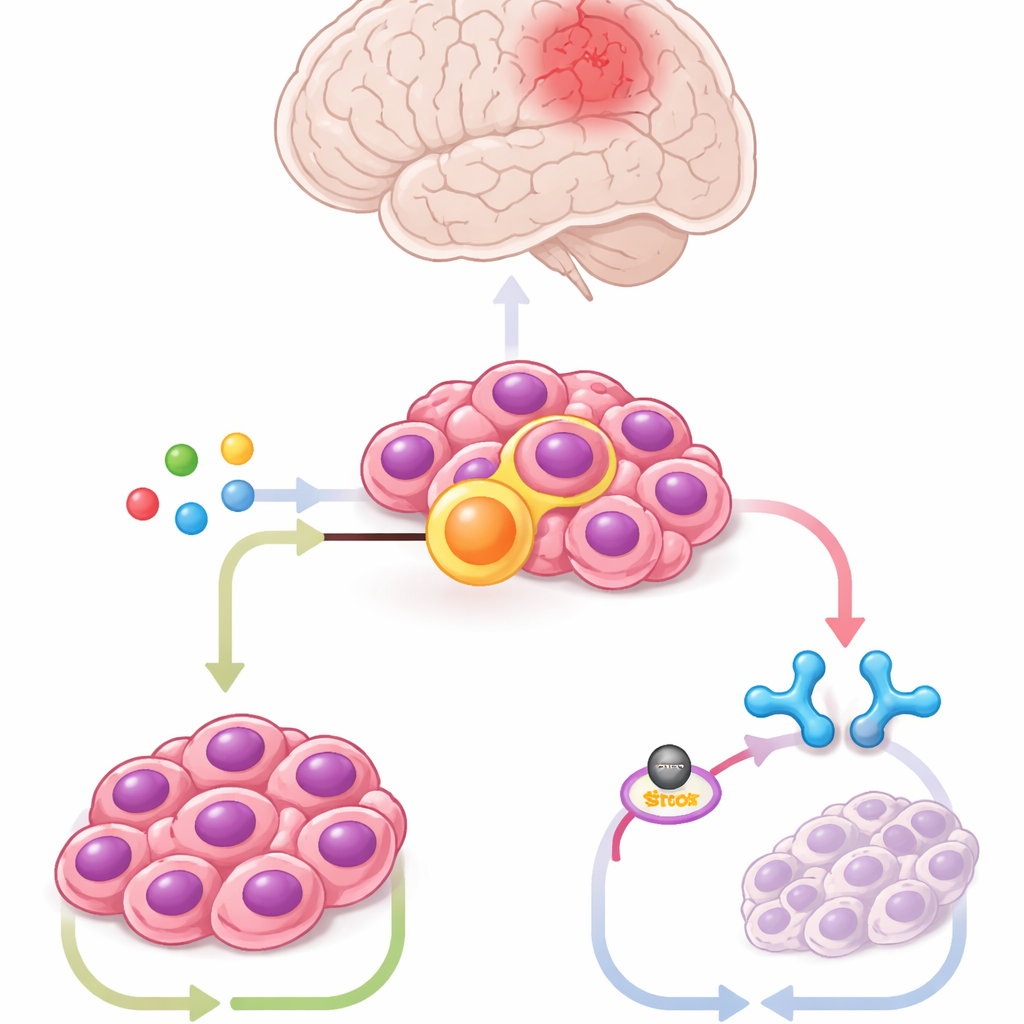
Een zelfversterkende lus in de DNA‑controle van de tumor
Waarom zou itaconaat zo belangrijk zijn? Het antwoord ligt in epigenetica — chemische markeringen op DNA‑verpakkende eiwitten die bepalen welke genen actief zijn. De auteurs ontdekten dat itaconaat een familie enzymen (KDM5) remt die normaal een activerende markering genaamd H3K4me3 van histonen verwijderen. Wanneer KDM5 wordt geblokkeerd, stapelt H3K4me3 zich op, vooral bij sleutelregio’s van het ZFTA-gen die deel uitmaken van de ZFTA–RELA-fusie. Deze toegenomen markering versterkt de transcriptie van de fusie zelf en creëert een feed‑forward‑lus: ZFTA–RELA schakelt ACOD1 aan, ACOD1 maakt itaconaat, en itaconaat verhoogt op zijn beurt de expressie van ZFTA–RELA. Het verstoren van ACOD1 of het nabootsen van KDM5‑activiteit doorbrak deze lus, verlaagde het fusie-eiwit en vertraagde tumorgroei in meerdere modellen.
Glutamine: de brandstof achter de fusie
De studie volgde daarna waar de tumor de grondstof vandaan haalt om itaconaat te maken. Door cellen vormen van glutamine en glucose met zwaar koolstof gelabeld te voeden, toonden de onderzoekers aan dat het grootste deel van het koolstofskelet van itaconaat van glutamine komt. ZFTA–RELA‑tumoren overexpresseren glutaminetransporters en het enzym glutaminase, en vertonen geactiveerde PI3K–AKT–mTOR‑signalisatie, een route die bekend staat om glutaminegebruik aan te sturen. Tegelijkertijd dempt de fusie epigenetisch PTEN, een kritisch tumorremsend eiwit dat deze signaalweg normaal begrenst. Het gevolg is een herbedraad metabolisme dat glutamine aantrekt, het door de energieketen van de cel leidt en afzweigt naar itaconaatproductie, alles om hoge niveaus van de fusie‑aanjager te onderhouden. 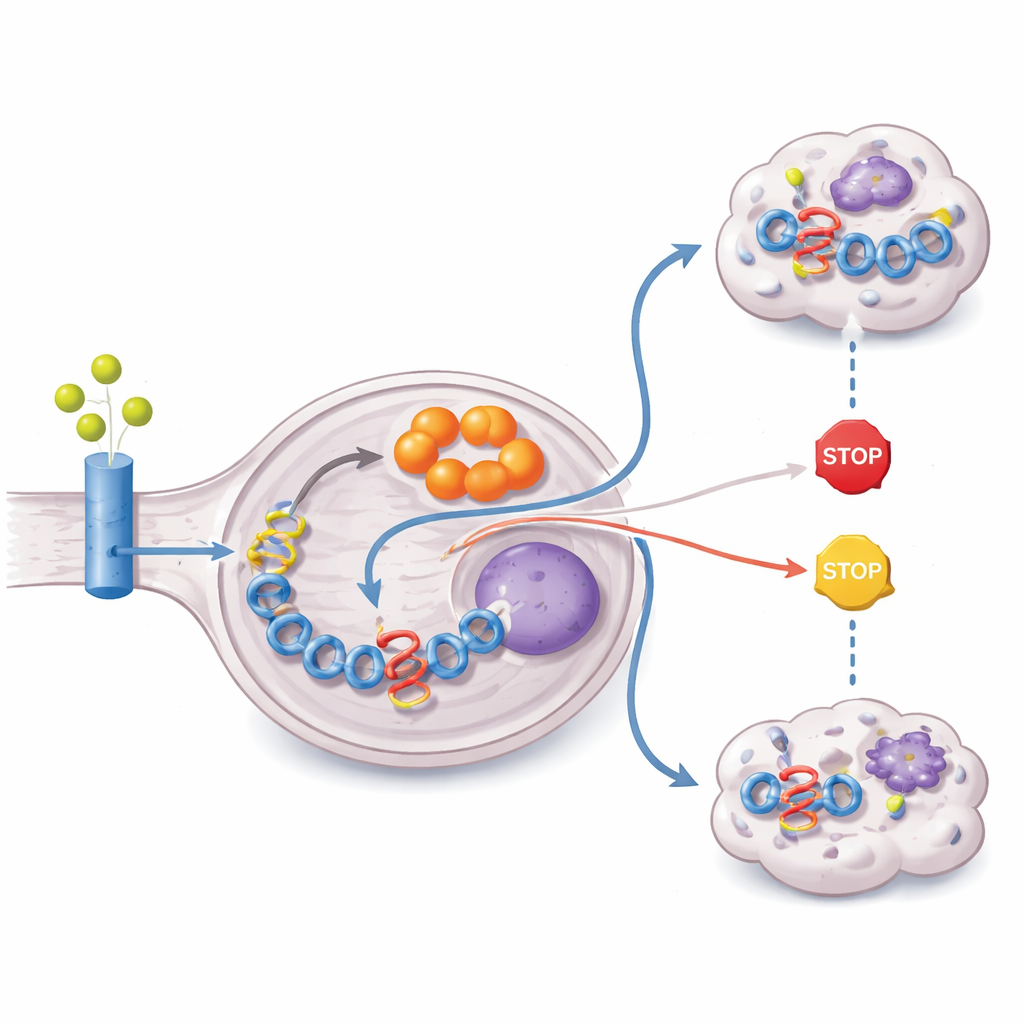
De tumor treffen waar hij zich voedt
Aangezien deze schakels uit meerdere afzonderlijke stappen bestaan, bieden ze meerdere geneesmiddelstargets. De auteurs testten verbindingen die de glutamine‑invoer, glutaminase, ACOD1 of de PI3K–mTOR‑route blokkeren, evenals een in de hersenen doordringende glutamineantagonist genaamd JHU‑083. Fusie‑positieve cellen waren veel gevoeliger voor deze middelen dan andere ependymoomsubtypes, en behandelde muizen leefden langer met kleinere tumoren. Bijzonder opvallend was dat het blokkeren van ACOD1 of het combineren van glutamineantagonisme met PI3K–mTOR‑remming niet alleen primaire hersentumoren verminderde, maar ook ruggenmergmetastasen in muismodellen voorkwam of uitrolde — laesies die bij patiënten bijzonder moeilijk te behandelen zijn.
Wat dit betekent voor patiënten en families
Voor niet‑specialisten is de kernboodschap dat deze ependymomen verslaafd zijn aan een specifiek metabolisch lusje dat ze zelf opzetten. Ze kapen een immuuncelmetaboliet, itaconaat, en een veelvoorkomende voedingsstof, glutamine, om hun belangrijkste kankergen aan te houden. Door deze lus van begin tot eind in kaart te brengen, identificeert de studie verschillende bestaande of opkomende soorten geneesmiddelen — die glutaminegebruik, ACOD1 of PI3K–mTOR‑signalisatie targeten — die gecombineerd zouden kunnen worden om ZFTA–RELA‑tumoren selectief te verzwakken en normaal hersenweefsel te sparen. Hoewel deze resultaten preklinisch zijn en nog niet klaar voor routinematige behandeling, wijzen ze een duidelijke weg naar gerichte therapieën voor een kinderkanker van de hersenen waarvoor momenteel weinig effectieve opties bestaan.
Bronvermelding: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Trefwoorden: ependymoom, hersenstumormetabolisme, itaconaat, glutamine‑verslaving, epigenetische therapie