Clear Sky Science · pt
ZFTA–RELA ependimomas produzem itaconato para ativar epigeneticamente a expressão da fusão
Por que esta história sobre câncer cerebral importa
Os ependimomas são tumores cerebrais raros, porém agressivos, que frequentemente atingem crianças e jovens adultos. Para muitos pacientes, cirurgia e radioterapia conseguem controlar o câncer por algum tempo, mas raramente o curam. Este estudo revela uma vulnerabilidade inesperada em um subtipo comum desses tumores: eles dependem de uma molécula pouco conhecida, o itaconato, para manter seu gene principal causador de câncer ativado. Ao rastrear como o tumor produz e usa essa molécula, os pesquisadores identificam várias novas maneiras pelas quais futuros medicamentos poderiam bloquear esses cânceres.
Uma fusão perigosa no cérebro
Mais da metade dos ependimomas que surgem na parte superior do cérebro carregam uma fusão genética chamada ZFTA–RELA. Sozinhos, os dois genes originais são inofensivos, mas quando fundidos criam um potente indutor de câncer que se desloca para o núcleo celular e reprograma como o DNA é lido. Até agora, a maior parte do trabalho sobre ZFTA–RELA focava seu papel no controle gênico. O novo estudo fez uma pergunta diferente: essa fusão também reprograma o metabolismo do tumor — a rede de reações químicas que fornece energia e blocos de construção — de maneiras que possam ser exploradas terapeuticamente?
Uma molécula de macrófago virada para o lado maligno
Usando células do tronco cerebral de camundongo modificadas para carregar a fusão, células tumorais derivadas de pacientes e modelos murinos, a equipe analisou centenas de metabólitos. Um se destacou nitidamente: o itaconato, uma molécula normalmente produzida por células imunes chamadas macrófagos durante infecções. As células tumorais produziam grandes quantidades de itaconato por meio de uma enzima chamada ACOD1, cujos níveis subiam e desciam em sincronia com ZFTA–RELA. Reduzir ACOD1 ou bloqueá‑la com pequenas moléculas foi tóxico para células positivas para a fusão e encolheu tumores em camundongos, enquanto a adição de itaconato suplementar resgatou o crescimento tumoral. Esses resultados mostram que o câncer cooptou uma via de células imunes para sua própria sobrevivência. 
Um circuito autorreforçador no controle do DNA do tumor
Por que o itaconato seria tão importante? A resposta está na epigenética — marcas químicas nas proteínas que empacotam o DNA que determinam quais genes estão ativos. Os autores descobriram que o itaconato inibe uma família de enzimas (KDM5) que normalmente removem uma marca ativadora chamada H3K4me3 dos histonas. Quando KDM5 é bloqueada, H3K4me3 se acumula, especialmente em regiões de controle-chave do gene ZFTA que fazem parte da fusão ZFTA–RELA. Esse aumento de marcação reforça a transcrição da própria fusão, criando um loop de alimentação positiva: ZFTA–RELA liga ACOD1, ACOD1 produz itaconato, e o itaconato por sua vez aumenta a expressão de ZFTA–RELA. Disromper ACOD1 ou mimetizar a atividade de KDM5 quebrou esse circuito, reduziu a proteína de fusão e desacelerou o crescimento tumoral em múltiplos modelos.
Glutamina: o combustível por trás da fusão
O estudo então rastreou de onde o tumor obtém a matéria‑prima para fabricar itaconato. Ao fornecer às células formas de glutamina e glicose rotuladas com carbono pesado, os pesquisadores mostraram que a maior parte do esqueleto de carbono do itaconato vem da glutamina. Tumores ZFTA–RELA superexpressam transportadores de glutamina e a enzima glutaminase, e apresentam sinalização ativada PI3K–AKT–mTOR, uma via conhecida por estimular o uso de glutamina. Ao mesmo tempo, a fusão silencia epigeneticamente PTEN, um supressor tumoral crítico que normalmente modera essa via. O resultado é um metabolismo reconfigurado que capta glutamina, a canaliza pelo ciclo energético da célula e a desvia para a produção de itaconato, tudo para sustentar altos níveis do indutor de fusão.
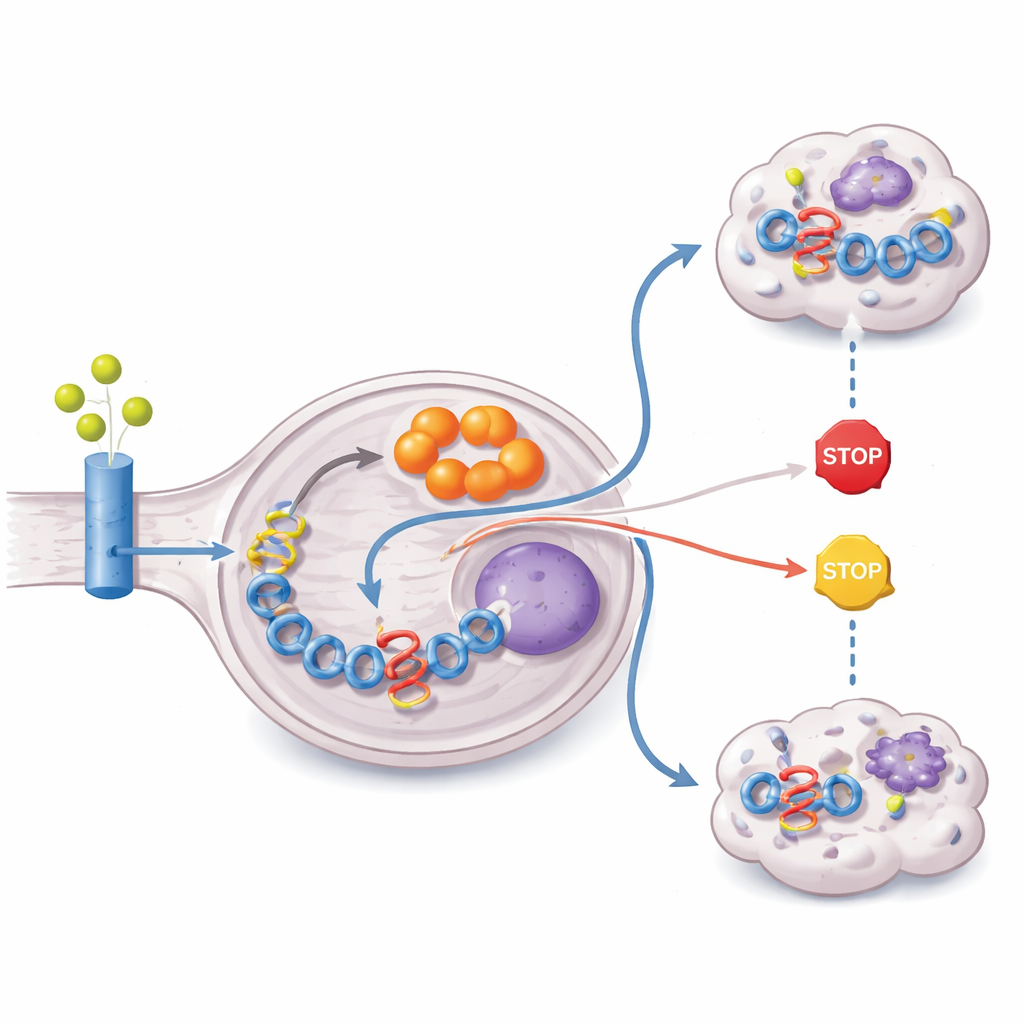
Atacando o tumor onde ele se alimenta
Como esse circuito tem várias etapas distintas, ele oferece múltiplos alvos farmacológicos. Os autores testaram compostos que bloqueiam a entrada de glutamina, a glutaminase, a ACOD1 ou a via PI3K–mTOR, bem como um antagonista de glutamina capaz de penetrar no cérebro chamado JHU‑083. Células positivas para a fusão foram muito mais sensíveis a esses agentes do que outros subtipos de ependimoma, e camundongos tratados viveram mais tempo com tumores menores. De forma particularmente marcante, bloquear ACOD1 ou combinar antagonismo da glutamina com inibição de PI3K–mTOR não apenas reduziu tumores cerebrais primários, como também preveniu ou eliminou metástases na medula espinhal em modelos de camundongo — lesões especialmente difíceis de tratar em pacientes.
O que isso significa para pacientes e famílias
Para um público não especializado, a mensagem chave é que esses ependimomas são viciados em um circuito metabólico específico de sua própria fabricação. Eles sequestram um metabólito de células imunes, o itaconato, e um nutriente comum, a glutamina, para manter seu principal gene cancerígeno ativado. Ao mapear esse circuito do início ao fim, o estudo identifica vários tipos de drogas existentes ou em desenvolvimento — que visam o uso de glutamina, a ACOD1 ou a sinalização PI3K–mTOR — que poderiam ser combinados para enfraquecer seletivamente tumores ZFTA–RELA ao mesmo tempo em que poupam o cérebro normal. Embora esses resultados sejam pré‑clínicos e ainda não estejam prontos para uso rotineiro em tratamentos, eles traçam um caminho claro rumo a terapias direcionadas para um câncer cerebral infantil que atualmente carece de opções efetivas.
Citação: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Palavras-chave: ependimoma, metabolismo de tumor cerebral, itaconato, dependência de glutamina, terapia epigenética