Clear Sky Science · tr
ZFTA–RELA ependimomları, füzyon ifadesini epigenetik olarak sürdürmek için itakonat üretiyor
Bu beyin kanseri öyküsünün önemi
Ependimomlar nadir ancak agresif beyin tümörleridir ve sıklıkla çocukları ve genç erişkinleri etkiler. Birçok hasta için cerrahi ve radyasyon kanseri bir süre kontrol altında tutabilir ama nadiren tamamen iyileştirir. Bu çalışma, bu tümörlerin yaygın bir alt türünde şaşırtıcı bir zayıflığı ortaya koyuyor: esas kanser yapıcı genlerini açık tutmak için az bilinen bir molekül olan itakonata bağımlılar. Tümörün bu molekülü nasıl ürettiğini ve kullandığını izleyerek, araştırmacılar gelecekteki ilaçların bu kanserleri kapatmak için kullanabileceği birkaç yeni yolu ortaya koyuyor.
Beyindeki tehlikeli bir füzyon
Beynin üst kısmında ortaya çıkan ependimomların yarısından fazlasında ZFTA–RELA adlı genetik bir karışım bulunur. Orijinal iki gen tek başına zararsızken, füze olduklarında hücre çekirdeğine giren ve DNA okunmasını yeniden düzenleyen güçlü bir kanser sürücüsü oluştururlar. Bugüne dek ZFTA–RELA üzerindeki çalışmaların çoğu gen kontrolündeki rolüne odaklandı. Yeni çalışma ise farklı bir soruyu sordu: bu füzyon tümörün enerji ve yapı taşlarını sağlayan kimyasal reaksiyon ağı olan metabolizmasını, terapötik açıdan sömürülebilecek şekilde yeniden programlıyor mu?
Makrofaj molekülü karanlık tarafa geçti
Füzyonu taşımak üzere düzenlenmiş fare beyin kök hücreleri, hastadan türetilmiş tümör hücreleri ve fare modelleri kullanılarak ekip yüzlerce metaboliti profilledi. Biri belirgin şekilde öne çıktı: itakonat, normalde enfeksiyon sırasında makrofaj adı verilen bağışıklık hücreleri tarafından üretilen bir molekül. Tümör hücreleri ACOD1 adlı bir enzim yoluyla büyük miktarda itakonat üretti; bu enzimin seviyeleri ZFTA–RELA ile paralel olarak yükselip düştü. ACOD1‘i azaltmak veya küçük moleküllerle engellemek füzyon‑pozitif hücrelere toksikti ve farelerde tümörleri küçülttü; ek itakonat ise tümör büyümesini kurtardı. Bu sonuçlar, kanserin bir bağışıklık hücresi yolunu kendi hayatta kalması için ele geçirdiğini gösteriyor. 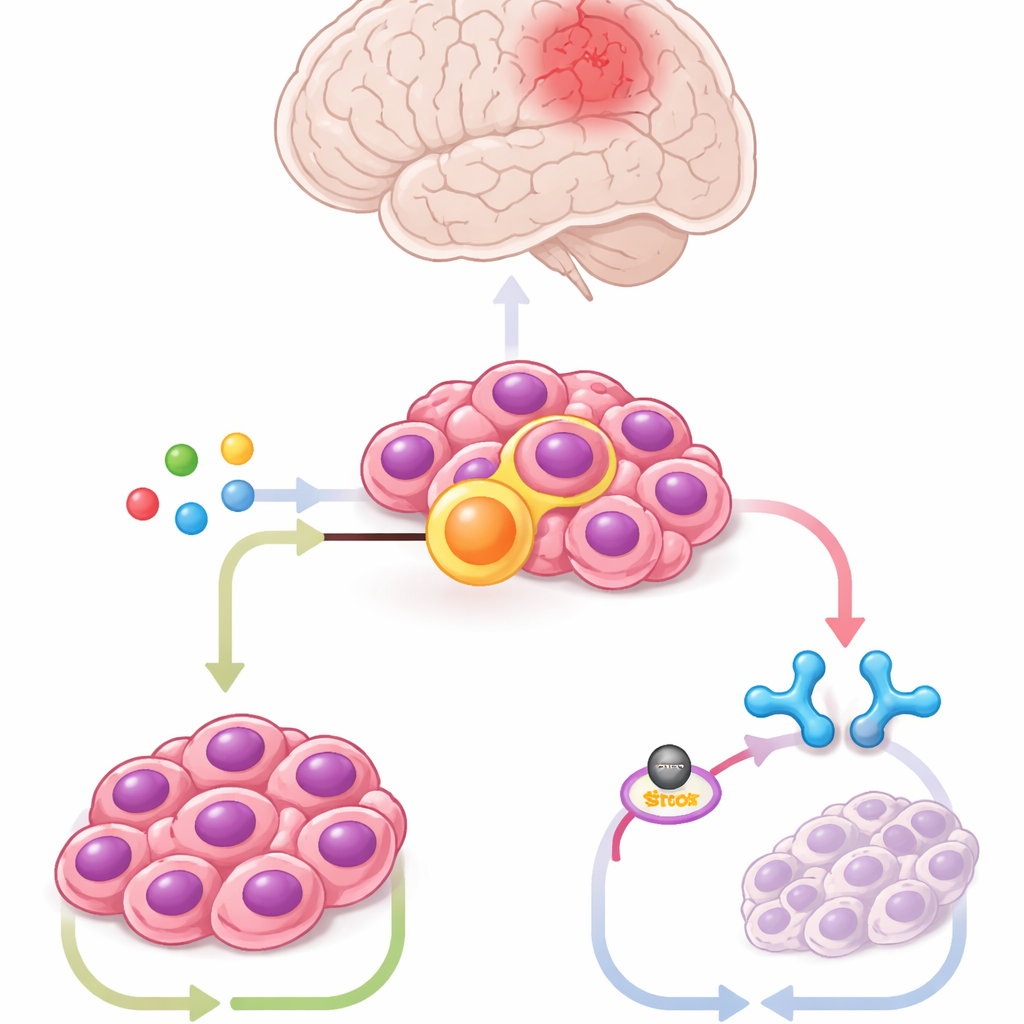
Tümörün DNA kontrolünde kendini güçlendiren bir döngü
Itakonat neden bu kadar önemli olur? Cevap epigenetikte—hangi genlerin aktif olduğunu belirleyen DNA paketleme proteinleri üzerindeki kimyasal işaretlerde yatıyor. Yazarlar, itakonatın normalde histonlardan etkinleştirici bir işaret olan H3K4me3'ü kaldıran KDM5 ailesi enzimlerini inhibe ettiğini keşfettiler. KDM5 engellendiğinde H3K4me3 birikiyor, özellikle ZFTA geninin ZFTA–RELA füzyonunun parçalarını içeren ana kontrol bölgelerinde. Bu artan işaretleme füzyonun kendisinin transkripsiyonunu artırıyor ve besleyen bir döngü oluşturuyor: ZFTA–RELA ACOD1‘i açıyor, ACOD1 itakonat üretiyor ve itakonat da ZFTA–RELA ifadesini güçlendiriyor. ACOD1'i bozmak veya KDM5 aktivitesini taklit etmek bu döngüyü kırdı, füzyon proteinini azalttı ve birden çok modelde tümör büyümesini yavaşlattı.
Füzyonun arkasındaki yakıt: glutamin
Çalışma ardından tümörün itakonat yapmak için hangi hammaddeyi kullandığını izledi. Hücrelere ağır karbon etiketli glutamin ve glukoz formları vererek araştırmacılar itakonatın karbon iskeletinin çoğunun glutaminden geldiğini gösterdiler. ZFTA–RELA tümörleri glutamin taşıyıcılarını ve glutaminaz enziminin aşırı ifadesini gösteriyor ve glutamin kullanımını yönlendiren PI3K–AKT–mTOR sinyal yolunun etkinleşmiş olduğunu sergiliyor. Aynı zamanda füzyon epigenetik olarak bu sinyali normalde sınırlayan kritik tümör baskılayıcı PTEN'i susturuyor. Sonuç, glutamini içeri çeken, onu hücrenin enerji döngüsünden kanallayan ve itakonat üretimine yönlendiren yeniden kablolanmış bir metabolizma; bunların hepsi füzyon sürücüsünün yüksek düzeylerini sürdürmek için hizmet ediyor. 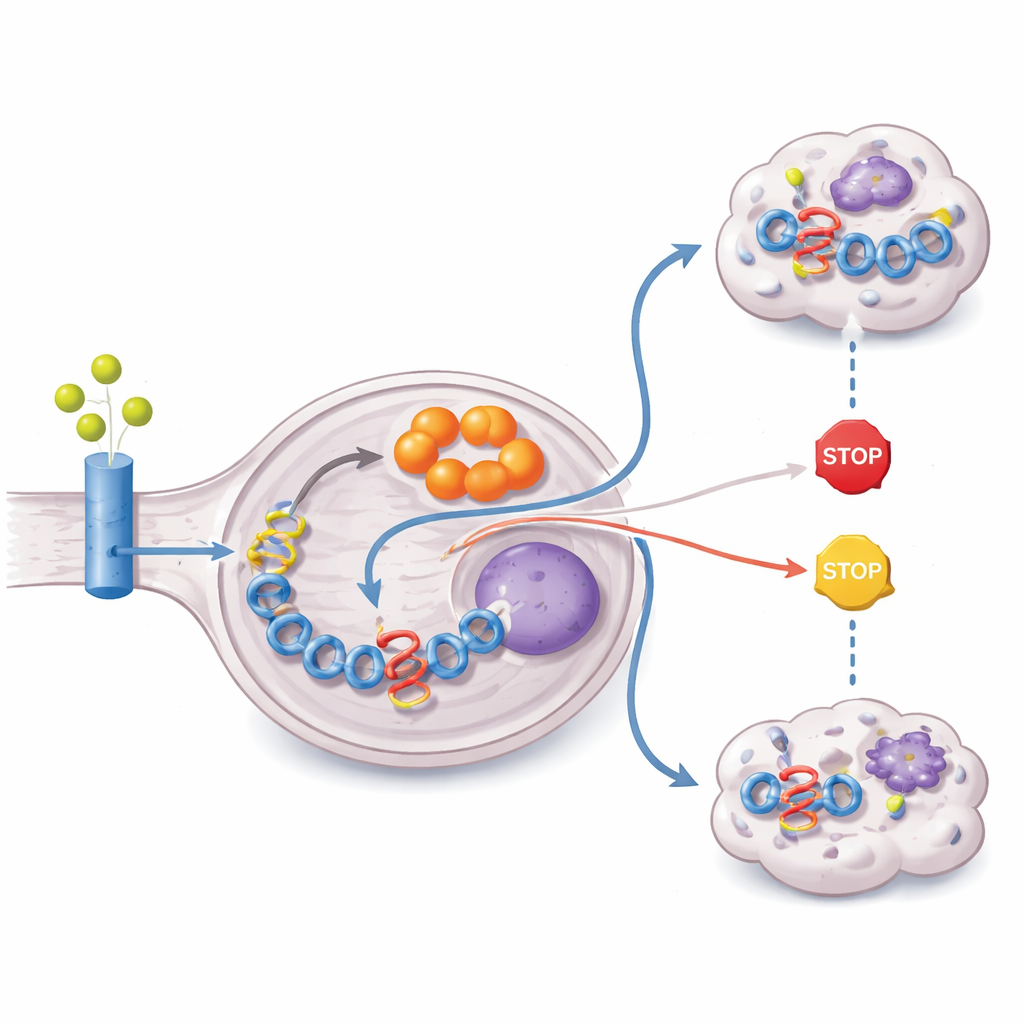
Tümörün beslendiği yere darbe
Bu devre birkaç ayrı adıma sahip olduğu için birden fazla ilaç hedefi sunuyor. Yazarlar glutamin alımını, glutaminazı, ACOD1‘i veya PI3K–mTOR yolunu bloke eden bileşikleri ve beyne geçen bir glutamin antagonisti olan JHU‑083’ü test ettiler. Füzyon‑pozitif hücreler bu ajanlara diğer ependimom alt türlerinden çok daha duyarlıydı ve tedavi edilen fareler daha küçük tümörlerle daha uzun yaşadı. Özellikle çarpıcı olan, ACOD1’i engellemenin veya glutamin antagonizmini PI3K–mTOR inhibisyonuyla birleştirmenin yalnızca primer beyin tümörlerini azaltmakla kalmayıp fare modellerinde omurilik metastazlarını da önlemesi veya ortadan kaldırmasıydı—hastalarda özellikle tedavisi zor lezyonlar.
Hastalar ve aileleri için anlamı
Uzman olmayan biri için temel mesaj şudur: bu ependimomlar kendi yarattıkları belirli bir metabolik döngüye bağımlı. Bir bağışıklık hücresi metabolitini, itakonatı, ve ortak bir besin maddesini, glutamini, kaçırarak başlıca kanser genlerini açık tutuyorlar. Bu döngüyü baştan sona haritalayarak çalışma, glutamin kullanımı, ACOD1 veya PI3K–mTOR sinyalini hedefleyen mevcut veya ortaya çıkan birkaç ilaç türünü tanımlıyor; bunlar birleştirilerek ZFTA–RELA tümörlerini seçici olarak zayıflatıp normal beyni koruyabilir. Bu sonuçlar preklinik olup henüz rutin tedaviye hazır olmasa da, etkili seçeneği sınırlı bir çocukluk beyin kanseri için hedefe yönelik tedavilere doğru açık bir yol çiziyor.
Atıf: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Anahtar kelimeler: ependimom, beyin tümörü metabolizması, itakonat, glutamin bağımlılığı, epigenetik tedavi