Clear Sky Science · es
Los ependimomas ZFTA–RELA producen itaconato para impulsar epigenéticamente la expresión de la fusión
Por qué importa esta historia sobre cáncer cerebral
Los ependimomas son tumores cerebrales raros pero agresivos que suelen afectar a niños y adultos jóvenes. Para muchos pacientes, la cirugía y la radioterapia pueden contener el cáncer durante un tiempo, pero rara vez lo curan. Este estudio descubre una debilidad sorprendente en un subtipo frecuente de estos tumores: dependen de una molécula poco conocida, el itaconato, para mantener activado su gen cancerígeno principal. Al seguir cómo el tumor produce y utiliza esta molécula, los investigadores revelan varias vías nuevas que podrían aprovecharse con fármacos futuros para detener estos cánceres.
Una fusión peligrosa en el cerebro
Más de la mitad de los ependimomas que se originan en la parte superior del cerebro llevan una hibridación genética llamada ZFTA–RELA. Por separado, los dos genes originales son inofensivos, pero cuando se fusionan crean un potente impulsor tumoral que se traslada al núcleo celular y reprograma la lectura del ADN. Hasta ahora, la mayor parte del trabajo sobre ZFTA–RELA se centró en su papel en el control génico. El nuevo estudio planteó una pregunta distinta: ¿esta fusión también reprograma el metabolismo del tumor, la red de reacciones químicas que proporciona energía y bloques de construcción, de formas que podrían explotarse terapéuticamente?
Una molécula de macrófago convertida al lado oscuro
Utilizando células madre del tronco encefálico de ratón diseñadas para portar la fusión, células tumorales derivadas de pacientes y modelos murinos, el equipo perfiló cientos de metabolitos. Uno destacó claramente: el itaconato, una molécula que normalmente producen células inmunitarias llamadas macrófagos durante la infección. Las células tumorales fabricaron grandes cantidades de itaconato mediante una enzima llamada ACOD1, cuyos niveles subían y bajaban en sincronía con ZFTA–RELA. Reducir ACOD1 o bloquearla con pequeñas moléculas resultó tóxico para las células positivas para la fusión y redujo el tamaño de los tumores en ratones, mientras que añadir itaconato adicional rescató el crecimiento tumoral. Estos resultados muestran que el cáncer ha cooptado una vía propia de las células inmunitarias para su supervivencia. 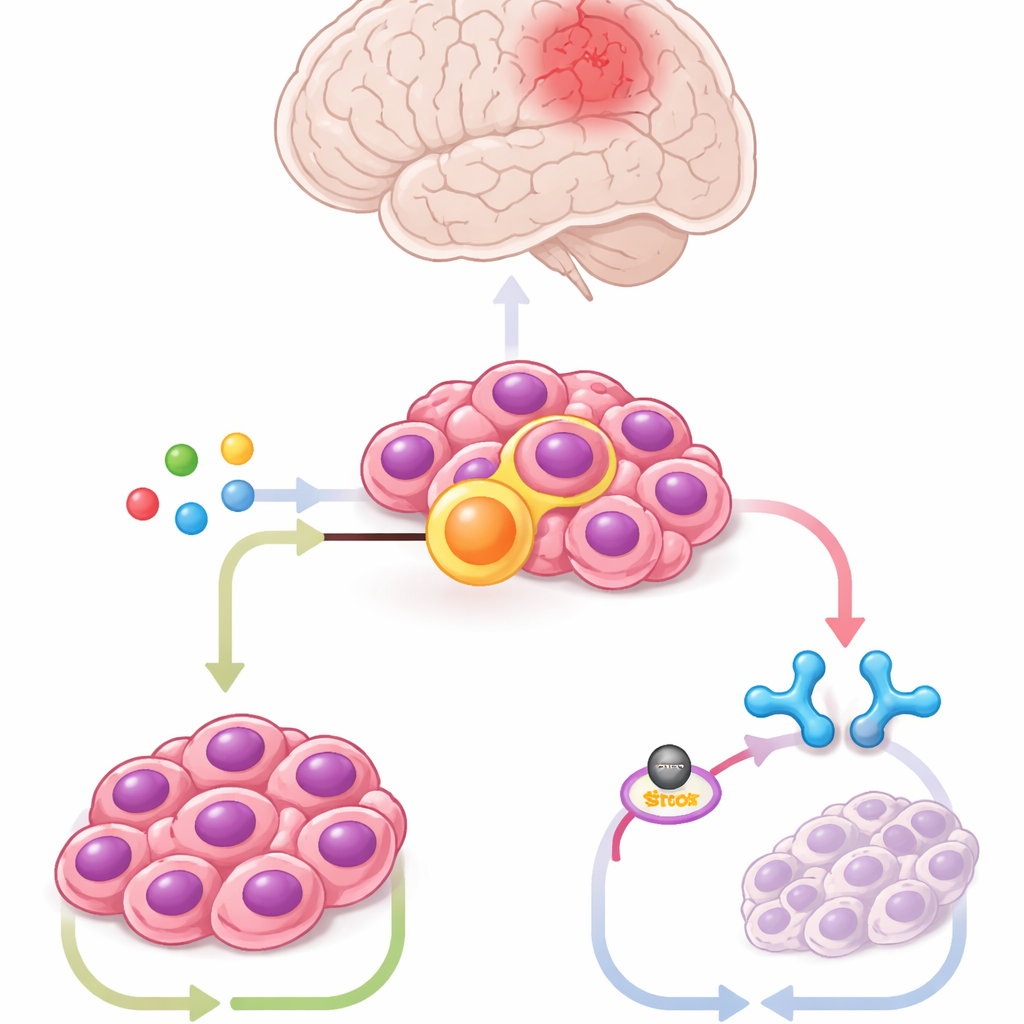
Un circuito autorreforzante en el control del ADN del tumor
¿Por qué sería tan importante el itaconato? La respuesta está en la epigenética: marcas químicas en las proteínas que empaquetan el ADN que determinan qué genes están activos. Los autores descubrieron que el itaconato inhibe una familia de enzimas (KDM5) que normalmente eliminan una marca activadora llamada H3K4me3 de las histonas. Cuando KDM5 queda bloqueada, H3K4me3 se acumula, especialmente en regiones clave de control del gen ZFTA que forman parte de la fusión ZFTA–RELA. Este aumento de marcas potencia la transcripción de la propia fusión, creando un bucle de retroalimentación: ZFTA–RELA activa ACOD1, ACOD1 produce itaconato, y el itaconato a su vez mejora la expresión de ZFTA–RELA. Interrumpir ACOD1 o imitar la actividad de KDM5 rompió este bucle, redujo la proteína de fusión y ralentizó el crecimiento tumoral en múltiples modelos.
Glutamina: el combustible detrás de la fusión
El estudio siguió luego de dónde obtiene el tumor la materia prima para fabricar itaconato. Alimentando células con formas de glutamina y glucosa marcadas con carbono pesado, los investigadores mostraron que la mayor parte del esqueleto carbonado del itaconato procede de la glutamina. Los tumores ZFTA–RELA sobreexpresan transportadores de glutamina y la enzima glutaminasa, y muestran activación de la señalización PI3K–AKT–mTOR, una vía conocida por impulsar el uso de glutamina. Al mismo tiempo, la fusión silencia epigenéticamente PTEN, un supresor tumoral crítico que normalmente limita esta señalización. El resultado es un metabolismo reprogramado que incorpora glutamina, la canaliza a través del ciclo energético celular y la desvía hacia la producción de itaconato, todo ello para sostener niveles altos del impulsor de la fusión. 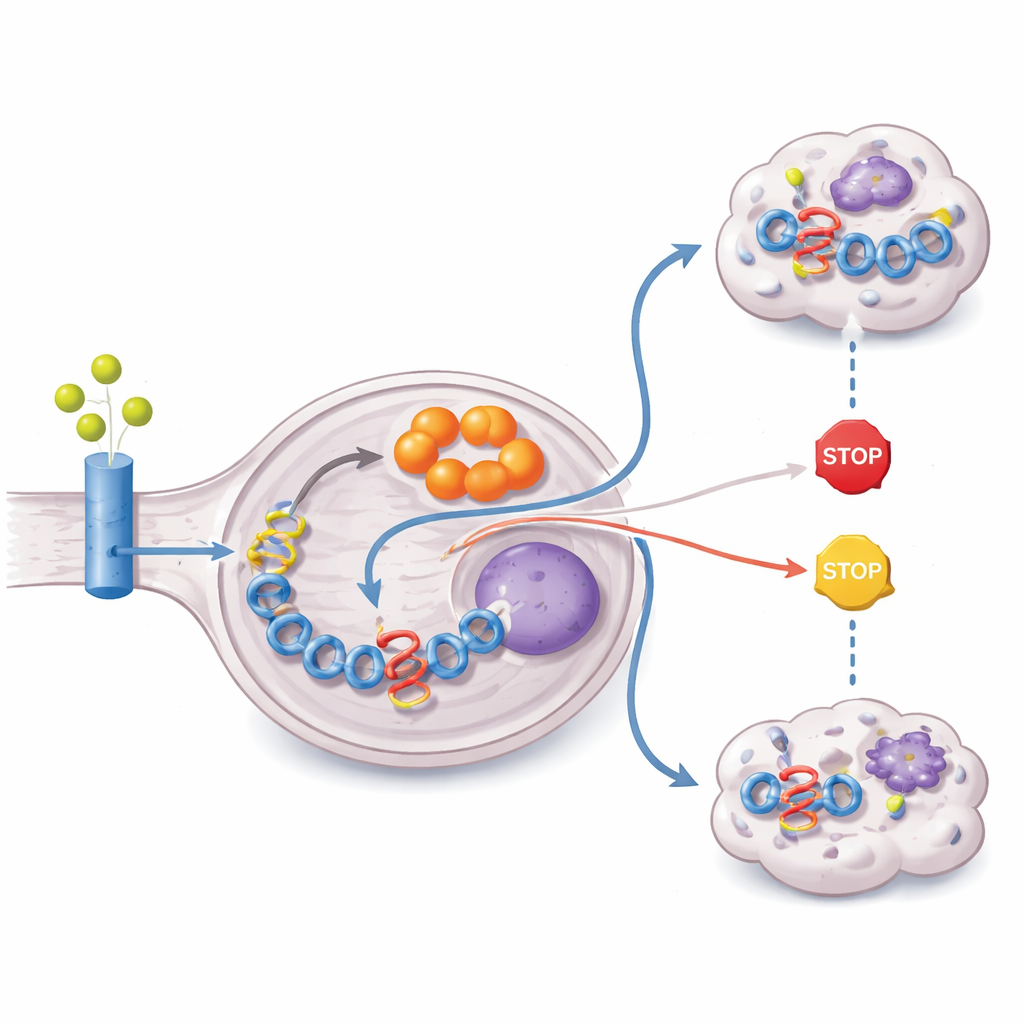
Atacar el tumor donde se alimenta
Porque este circuito tiene varios pasos distintos, ofrece múltiples dianas farmacológicas. Los autores probaron compuestos que bloquean la importación de glutamina, la glutaminasa, ACOD1 o la vía PI3K–mTOR, así como un antagonista de la glutamina con capacidad para penetrar el cerebro llamado JHU‑083. Las células positivas para la fusión fueron mucho más sensibles a estos agentes que otros subtipos de ependimoma, y los ratones tratados vivieron más tiempo con tumores más pequeños. De manera especialmente llamativa, bloquear ACOD1 o combinar el antagonismo de la glutamina con la inhibición de PI3K–mTOR no solo redujo los tumores cerebrales primarios sino que también previno o eliminó metástasis en la médula espinal en modelos murinos, lesiones que son especialmente difíciles de tratar en pacientes.
Qué significa esto para pacientes y familias
Para un público no especialista, el mensaje clave es que estos ependimomas son adictos a un bucle metabólico específico que ellos mismos han generado. Secuestran un metabolito de las células inmunitarias, el itaconato, y un nutriente común, la glutamina, para mantener activado su gen cancerígeno principal. Al cartografiar este bucle de principio a fin, el estudio identifica varios tipos de fármacos existentes o emergentes —que atacan el uso de glutamina, ACOD1 o la señalización PI3K–mTOR— que podrían combinarse para debilitar selectivamente los tumores ZFTA–RELA mientras se preserva el tejido cerebral normal. Aunque estos resultados son preclínicos y todavía no están listos para uso clínico rutinario, trazan un camino claro hacia terapias dirigidas para un cáncer cerebral infantil que actualmente carece de opciones eficaces.
Cita: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Palabras clave: ependimoma, metabolismo de tumores cerebrales, itaconato, adicción a la glutamina, terapia epigenética