Clear Sky Science · he
אפנדימומות ZFTA–RELA מייצרות איטקונאט כדי להפעיל אפיגנטית את ביטוי המיזוג
מדוע הסיפור הזה על סרטן המוח חשוב
אפנדימומות הן גידולים מוחיים נדירים אך אגרסיביים שפוגעים לעתים קרובות בילדים ובצעירים. עבור רבים מהחולים, ניתוח וקרינה עשויים לשלוט במחלה לפרק זמן, אך נדיר שירפאו אותה. המחקר הזה חושף חולשה מפתיעה בתת‑סוג שכיח של גידולים אלה: הם תלויים במולקולה מעט ידועה, איטקונאט, כדי להמשיך להפעיל את הגן המרכזי הגורם לסרטן. באמצעות מעקב אחר אופן ייצור ושימוש הגידול במולקולה זו, החוקרים מצביעים על מספר דרכים חדשות שבהן תרופות עתידיות עשויות לשתק את הגידולים הללו.
מיזוג מסוכן במוח
יותר ממחצית מהאפנדימומות שמופיעות בחלק העליון של המוח נושאות מיזוג גנטי שנקרא ZFTA–RELA. כל אחד מהגנים המקוריים לבדו אינו מזיק, אך כשהם מחוברים הם יוצרים מדַלֵּג סרטן חזק שנכנס לגרעין התא ומשנה את אופן קריאת ה‑DNA. עד כה רוב המחקר על ZFTA–RELA התרכז בתפקידו בבקרת גנים. המחקר החדש שאל שאלה שונה: האם המיזוג גם מתכנת מחדש את המטבוליזם של הגידול — רשת התגובות הכימיות שמספקת אנרגיה וחומרי בניין — באופן שניתן לנצל לטיפול?
מולקולה של מאקרופאג שנטתה לצידה האפל
בעזרת תאי גזע מוחיים של עכבר שעברו הנדסה לשאת את המיזוג, תאים ממקור חולים ומודלים עכבריים, הצוות פרופיל מאות מטבוליטים. אחד בלט במובהק: איטקונאט, מולקולה שמיוצרת בדרך כלל על ידי תאים חיסוניים הנקראים מאקרופאגים בזמן זיהום. תאי הגידול ייצרו כמויות גדולות של איטקונאט בעזרת אנזים בשם ACOD1, שרמותיו עלו וירדו בקורלציה עם ZFTA–RELA. השבתת ACOD1 או חסימתו בעזרת מולקולות קטנות היתה רעילה לתאים בעלי המיזוג וצימחה את גודל הגידולים בעכברים, בעוד תוספת איטקונאט החזירה את הצמיחה של הגידול. תוצאות אלה מראות שהסרטן השתלט על מסלול של תאי חיסון לטובת הישרדותו. 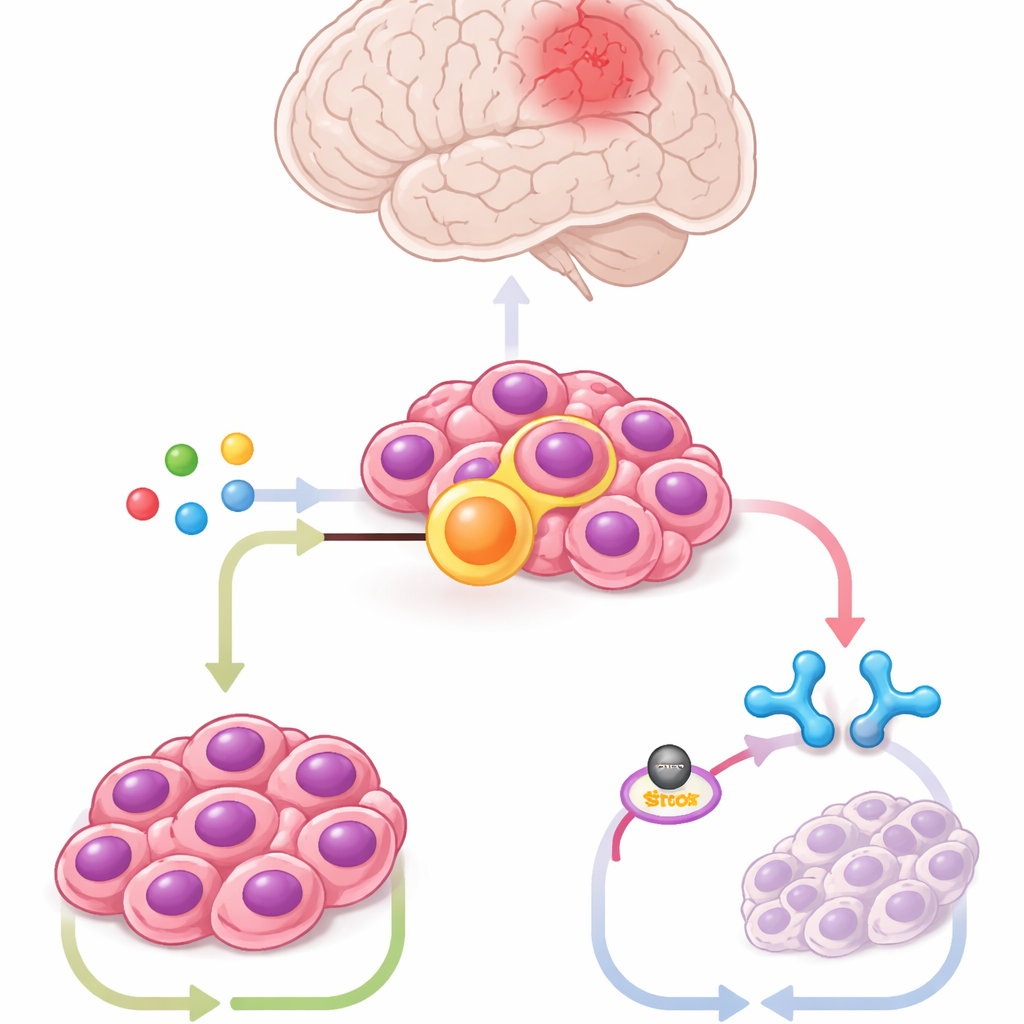
לולאה מחזקת‑עצמית בבקרת ה‑DNA של הגידול
מדוע איטקונאט חשוב כל כך? התשובה טמונה באפיגנטיקה — סימנים כימיים על חלבוני אריזת ה‑DNA שקובעים אילו גנים פעילים. המחברים גילו שאיטקונאט מעכב משפחה של אנזימים (KDM5) שמסירים בדרך כלל סימן מפעיל בשם H3K4me3 מהיסטונים. כאשר KDM5 נחסם, H3K4me3 מצטבר, במיוחד באזורים בקרה מרכזיים של גן ZFTA שמשתתפים במיזוג ZFTA–RELA. הצטברות סימון זו מגדילה את שיעתוק המיזוג עצמו, ובכך נוצר מעגל חיזוק: ZFTA–RELA מפעיל את ACOD1, ACOD1 מייצר איטקונאט, ואיטקונאט בתורו מגביר את הביטוי של ZFTA–RELA. שיבוש ACOD1 או חיקוי פעילות KDM5 שברו את המעגל הזה, הורידו את חלבון המיזוג והאטו את גדילת הגידול במודלים מרובים.
גלוטמין: הדלק שמאחורי המיזוג
המחקר עקב גם אחר מקורות החומר הגולמי לייצור איטקונאט בגידול. על ידי האכלת תאים בגלוטמין ובגלוקוז מסומנים בפחמן כבד, החוקרים הראו שרוב שלד הפחמן של איטקונאט מגיע מגלוטמין. גידולי ZFTA–RELA מבטאים יתר של נשאי גלוטמין והאנזים גלוטמינאז, ומציגים איתות פעיל של PI3K–AKT–mTOR — מסלול הידוע בדחיפת השימוש בגלוטמין. בו‑זמנית, המיזוג משתיק אפיגנטית את PTEN, מעכב גידול קריטי שמצמצם בדרך כלל את האיתות הזה. התוצאה היא מטבוליזם משוכתב שלוקח גלוטמין, מכוון אותו דרך מחזור האנרגיה של התא ומסיט אותו לייצור איטקונאט, הכל כדי לשמור על רמות גבוהות של מניע המיזוג. 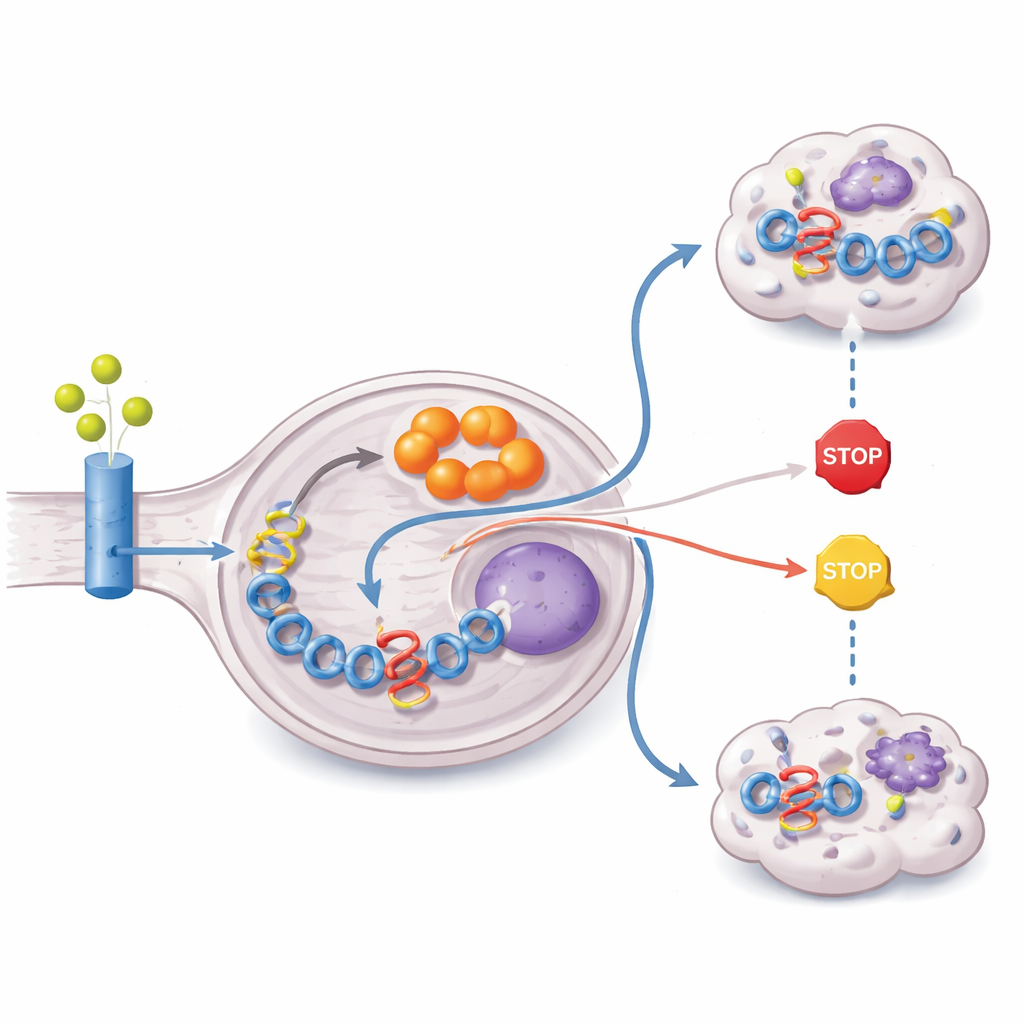
לתקוף את הגידול במקום שבו הוא אוכל
כיוון שלמעגל זה יש מספר שלבים מובחנים, הוא מציע מטרות תרופתיות מרובות. המחברים בחנו תרכובות שמחסמות ייבוא גלוטמין, גלוטמינאז, ACOD1 או את מסלול PI3K–mTOR, וכן אנטגוניסט לגלוטמין שיכול לחדור למוח בשם JHU‑083. תאי המיזוג היו רגישים בהרבה לסוכנים אלה בהשוואה לתת‑סוגים אחרים של אפנדימומה, ובעכברים מטופלים החיות האריכו וניתנו גידולים קטנים יותר. באופן בולט, חסימת ACOD1 או שילוב של אנטגוניזם לגלוטמין עם עיכוב PI3K–mTOR לא רק הקטינו גידולים ראשוניים במוח אלא גם מנעו או הסירו גרורות בחוט השדרה במודלים עכבריים — נגעים שקשה במיוחד לטפל בהם בחולים.
מה זה אומר לחולים ולמשפחותיהם
ללא ידע מומחה, המסר המרכזי הוא שאותן אפנדימומות מכורות ללולאה מטבולית ספציפית שיצרו לעצמן. הן חוטפות מטבוליט של תא חיסון, איטקונאט, וחומר מזון נפוץ, גלוטמין, כדי לשמור על הגן המוביל שלהן דולק. על ידי מיפוי הלולאה הזו מתחילתה ועד סופה, המחקר מזהה כמה סוגי תרופות קיימות או מתפתחות — שמטרתן שימוש בגלוטמין, ACOD1 או איתות PI3K–mTOR — שאותן ניתן לשלב כדי להחליש באופן סלקטיבי גידולים של ZFTA–RELA ולשמור על מוח תקין. אמנם התוצאות הן פרה‑קליניות ועדיין לא מוכנות לטיפול שגרתי, אך הן משרטטות דרך ברורה לעבר טיפולים ממוקדים עבור סרטן מוח בילדים שלרוב חסרים לו אופציות יעילות כיום.
ציטוט: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
מילות מפתח: אפנדימומה, מטבוליזם של גידול מוחי, איטקונאט, תלות בגלוטמין, טיפול אפיגנטי