Clear Sky Science · pl
ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression
Dlaczego ta opowieść o raku mózgu ma znaczenie
Ependymomy to rzadkie, ale agresywne nowotwory mózgu, które często dotykają dzieci i młodych dorosłych. U wielu pacjentów operacja i radioterapia mogą przez pewien czas powstrzymać chorobę, lecz rzadko prowadzą do wyleczenia. To badanie ujawnia zaskakującą słabość jednego z powszechnych podtypów tych guzów: polegają one na mało znanym związku, itakonianie, by utrzymywać aktywność głównego onkogenu. Śledząc, jak guz wytwarza i wykorzystuje tę cząsteczkę, naukowcy wskazują kilka nowych sposobów, w jakie przyszłe leki mogłyby je wyłączyć.
Niebezpieczne złączenie w mózgu
Więcej niż połowa ependymomów powstających w górnej części mózgu nosi genetyczne zlanie zwane ZFTA–RELA. Same dwa oryginalne geny są nieszkodliwe, ale po złączeniu tworzą silny czynnik onkogenny, który wnika do jądra komórkowego i przeprogramowuje sposób odczytu DNA. Do tej pory większość badań nad ZFTA–RELA koncentrowała się na jego roli w kontroli genów. Nowe badanie postawiło inne pytanie: czy to złączenie także przestawia metabolizm guza — sieć reakcji chemicznych dostarczających energii i budulca — w sposób możliwy do wykorzystania terapeutycznie?
Cząsteczka makrofagów zwrócona przeciwko
Pracując na zmodyfikowanych komórkach pnia mózgu myszy niosących złączenie, komórkach nowotworu pochodzących od pacjentów oraz modelach mysich, zespół przeanalizował setki metabolitów. Jeden związek wyróżniał się wyraźnie: itakonian, cząsteczka zwykle produkowana przez komórki odpornościowe zwane makrofagami podczas infekcji. Komórki guza wytwarzały duże ilości itakonianu za pośrednictwem enzymu ACOD1, którego poziomy rosły i malały równolegle z ZFTA–RELA. Zahamowanie ACOD1 lub blokada małymi cząsteczkami była toksyczna dla komórek z fuzją i zmniejszała guzy u myszy, natomiast podanie dodatkowego itakonianu przywracało wzrost guza. Wyniki te pokazują, że rak zawłaszczył ścieżkę typową dla komórek odpornościowych, by zapewnić sobie przetrwanie. 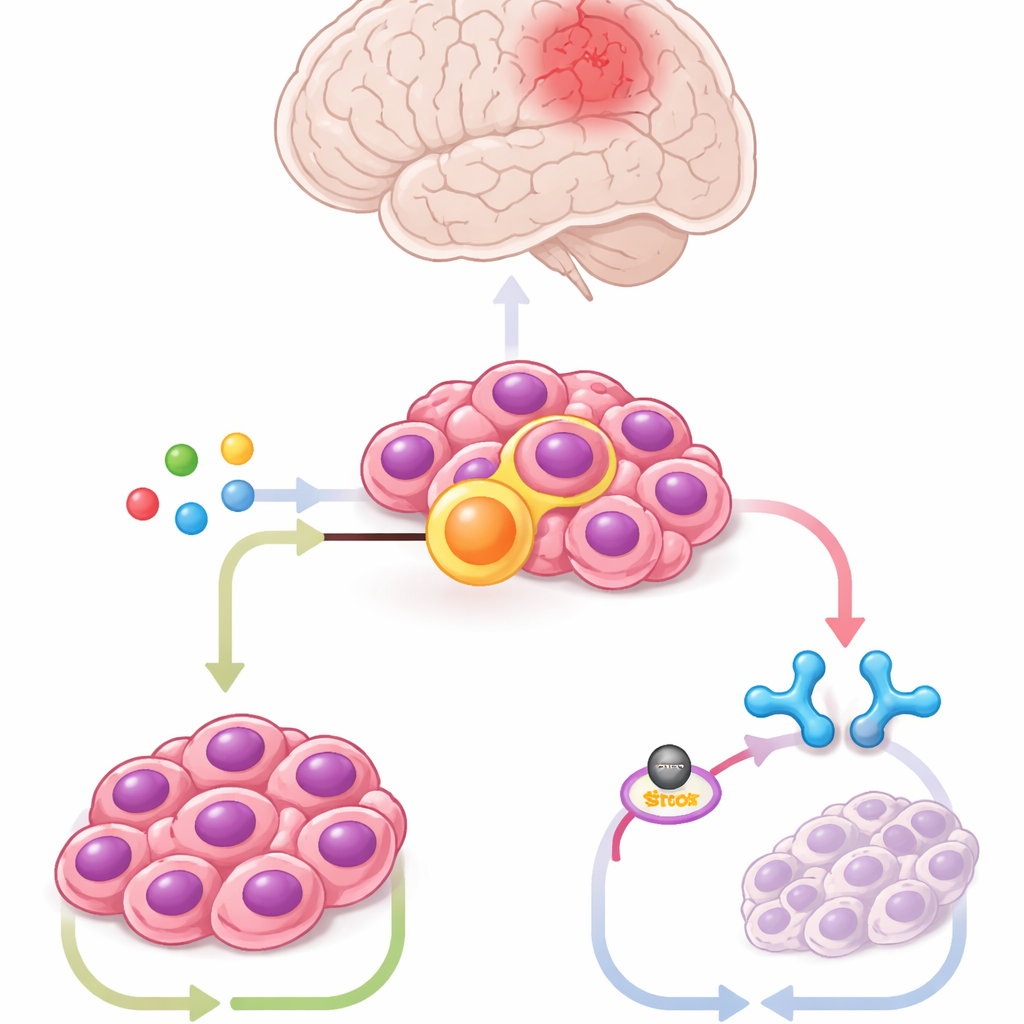
Samo-wzmacniająca się pętla w kontroli DNA guza
Dlaczego itakonian jest tak ważny? Odpowiedź leży w epigenetyce — chemicznych znakach na białkach opakowujących DNA, które decydują, które geny są aktywne. Autorzy odkryli, że itakonian hamuje rodzinę enzymów (KDM5), które normalnie usuwają aktywujący znak H3K4me3 z histonów. Gdy KDM5 są zahamowane, H3K4me3 się kumuluje, szczególnie w kluczowych regionach kontrolnych genu ZFTA, które wchodzą w skład fuzji ZFTA–RELA. To nasilenie znakowania zwiększa transkrypcję samej fuzji, tworząc pętlę wzmacniającą: ZFTA–RELA włącza ACOD1, ACOD1 produkuje itakonian, a itakonian z kolei zwiększa ekspresję ZFTA–RELA. Przerwanie ACOD1 lub udawanie aktywności KDM5 łamało tę pętlę, obniżało poziom białka fuzyjnego i spowalniało wzrost guza w wielu modelach.
Glutamina: paliwo stojące za fuzją
Następnie badanie śledziło, skąd guz czerpie surowiec do produkcji itakonianu. Karmiąc komórki formami glutaminy i glukozy znakowanymi ciężkim węglem, badacze wykazali, że większość szkieletu węglowego itakonianu pochodzi z glutaminy. Guzy ZFTA–RELA nadmiernie ekspresjonują transportery glutaminy i enzym glutaminazę oraz wykazują aktywację szlaku PI3K–AKT–mTOR, znanego z napędzania wykorzystania glutaminy. Jednocześnie złączenie epigenetycznie wycisza PTEN, krytyczny supresor guza, który normalnie hamuje ten szlak. W efekcie metabolizm zostaje przeprogramowany tak, by pobierać glutaminę, kierować ją przez cykl energetyczny komórki i przekierowywać na produkcję itakonianu — wszystko po to, by utrzymać wysokie poziomy onkogenu fuzyjnego. 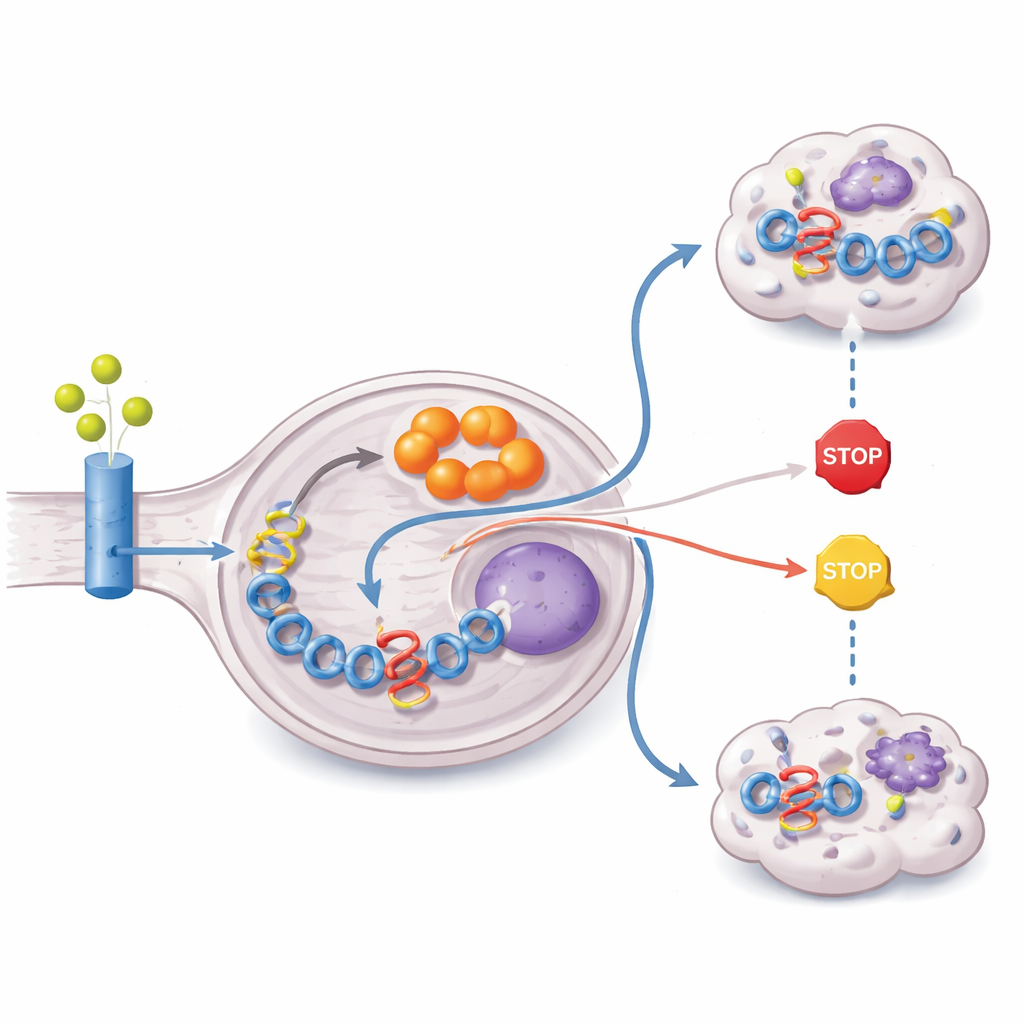
Uderzanie w guz tam, gdzie się odżywia
Ponieważ obwód ten ma kilka odrębnych etapów, oferuje wiele celów dla leków. Autorzy przetestowali związki blokujące import glutaminy, glutaminazę, ACOD1 oraz szlak PI3K–mTOR, a także przepuszczalny dla mózgu antagonista glutaminy zwany JHU‑083. Komórki z fuzją były znacznie bardziej wrażliwe na te środki niż inne podtypy ependymom, a leczeni myszy żyły dłużej i miały mniejsze guzy. Szczególnie uderzające były efekty blokady ACOD1 lub połączenia antagonizmu glutaminy z hamowaniem PI3K–mTOR — nie tylko zmniejszały guzy pierwotne w mózgu, ale także zapobiegały lub usuwały przerzuty do rdzenia kręgowego w modelach mysich — zmiany, które u pacjentów są szczególnie trudne do leczenia.
Co to oznacza dla pacjentów i rodzin
Dla czytelnika niezwiązanego z tematem kluczowe przesłanie jest takie: te ependymomy są uzależnione od konkretnej metabolicznej pętli, którą same wytworzyły. Przywłaszczają sobie metabolit komórek odpornościowych — itakonian — oraz powszechny składnik odżywczy, glutaminę, aby utrzymywać włączony główny gen nowotworowy. Mapując tę pętlę od początku do końca, badanie identyfikuje kilka istniejących lub pojawiających się typów leków — celujących w użycie glutaminy, ACOD1 lub sygnalizację PI3K–mTOR — które mogłyby być łączone, by selektywnie osłabić guzy ZFTA–RELA przy jednoczesnym oszczędzeniu normalnej tkanki mózgowej. Chociaż wyniki są przedkliniczne i jeszcze nie nadają się do rutynowego leczenia, wskazują jasną drogę ku terapiom ukierunkowanym dla dziecięcego nowotworu mózgu, dla którego obecnie brakuje skutecznych opcji.
Cytowanie: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Słowa kluczowe: ependymoma, brain tumor metabolism, itaconate, glutamine addiction, epigenetic therapy