Clear Sky Science · ru
Эпендимомы с фузией ZFTA–RELA синтезируют итаконат, который эпигенетически поддерживает экспрессию фузии
Почему эта история о раке мозга важна
Эпендимомы — редкие, но агрессивные опухоли мозга, которые часто поражают детей и молодых взрослых. Для многих пациентов хирургия и радиотерапия способны временно сдерживать болезнь, но редко приводят к излечению. В этом исследовании выявлена неожиданная уязвимость одного из распространённых подтипов: эти опухоли зависят от малоизвестной молекулы — итаконата — чтобы поддерживать включённым свой главный онкоген. Проследив, как опухоль синтезирует и использует эту молекулу, авторы раскрывают несколько новых направлений, которыми можно воспользоваться при разработке будущих лекарств.
Опасная фузия в мозге
Более половины эпендимом верхних отделов мозга несут генетическую перестановку, называемую ZFTA–RELA. По отдельности исходные гены безобидны, но при слиянии они образуют мощный онкоген, который попадает в ядро клетки и перенастраивает считывание ДНК. До сих пор большая часть работ над ZFTA–RELA сосредотачивалась на её роли в регуляции генов. Новое исследование поставило иной вопрос: перенастраивает ли эта фузия также метаболизм опухоли — сеть химических реакций, обеспечивающих энергию и строительные блоки — таким образом, чтобы это можно было использовать для терапии?
Молекула макрофагов, обратившаяся во зло
Используя стволовые клетки мозга мыши, генетически модифицированные для несения фузии, клетки опухоли, полученные от пациентов, и мышиные модели, исследователи профилировали сотни метаболитов. Один из них резко выделялся: итаконат — молекула, обычно вырабатываемая иммунными клетками, макрофагами, во время инфекции. Клетки опухоли продуцировали большие количества итаконата через фермент ACOD1, уровни которого менялись синхронно с ZFTA–RELA. Понижение экспрессии ACOD1 или блокада его небольшими молекулами оказывала токсичное действие на клетки с фузией и уменьшала опухоли у мышей, тогда как добавление внешнего итаконата восстанавливало рост опухоли. Эти результаты показывают, что рак присвоил путь, свойственный иммунным клеткам, для собственного выживания. 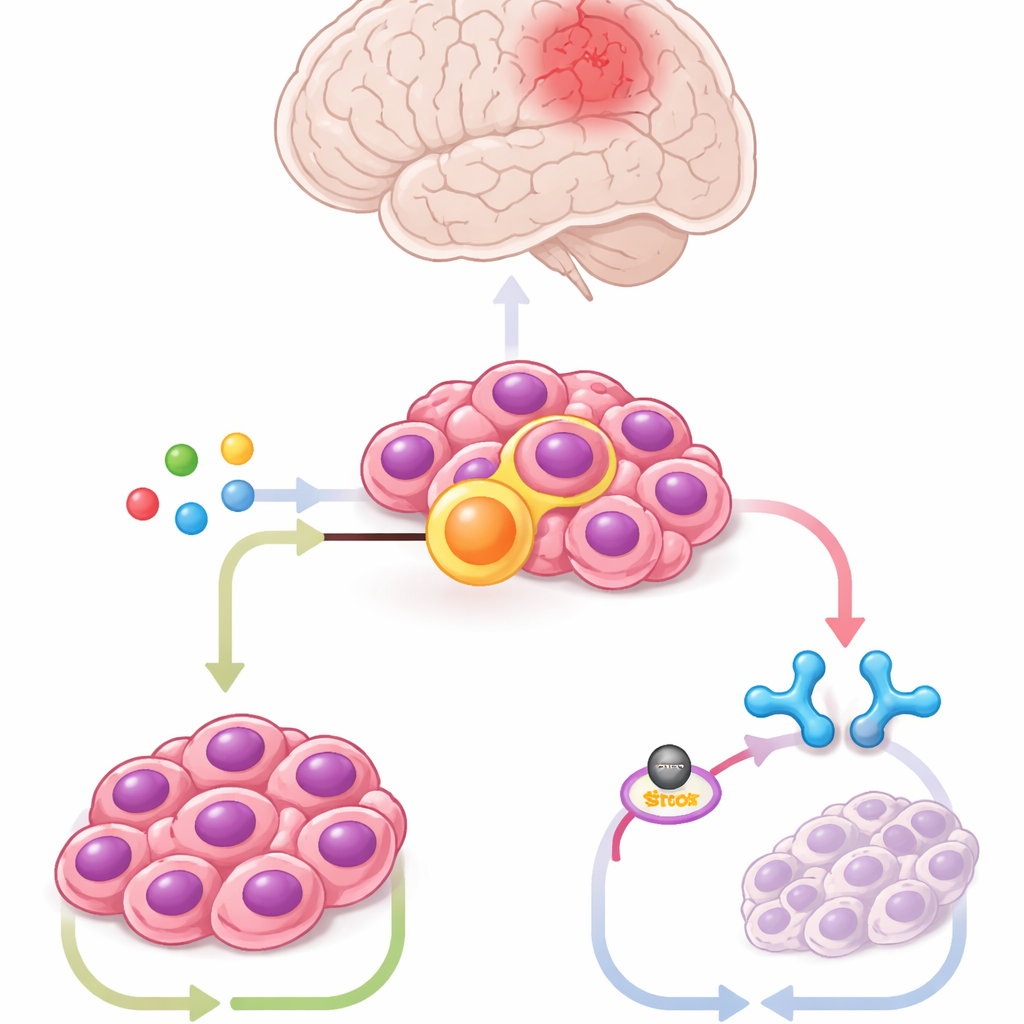
Самоподдерживающаяся петля в системе контроля ДНК опухоли
Почему итаконат оказывается столь важным? Ответ кроется в эпигенетике — химических метках на белках, упаковывающих ДНК, которые определяют, какие гены активны. Авторы обнаружили, что итаконат ингибирует семейство ферментов KDM5, которые обычно удаляют активирующую метку H3K4me3 с гистонов. При блокаде KDM5 H3K4me3 накапливается, особенно в ключевых контрольных областях гена ZFTA, вовлечённых в фузию ZFTA–RELA. Увеличение этой метки усиливает транскрипцию самой фузии, создавая петлю с положительной обратной связью: ZFTA–RELA включает ACOD1, ACOD1 синтезирует итаконат, а итаконат в свою очередь усиливает экспрессию ZFTA–RELA. Нарушение ACOD1 или имитация активности KDM5 разрывали эту петлю, снижали уровень белка фузии и замедляли рост опухоли в нескольких моделях.
Глутамин: топливо за этой «склейкой»
Далее исследование установило, откуда опухоль берёт исходные материалы для синтеза итаконата. Кормя клетки формами глутамина и глюкозы, помеченными тяжёлым углеродом, исследователи показали, что большая часть углеродного скелета итаконата происходит от глутамина. Опухоли с ZFTA–RELA сверхэкспрессируют переносчики глутамина и фермент глутаминазу, а также демонстрируют активированную сигнальную каскаду PI3K–AKT–mTOR, известную тем, что стимулирует использование глутамина. Одновременно фузия эпигенетически заглушает PTEN, критический опухолевый супрессор, который обычно сдерживает эту сигнализацию. В результате метаболизм опухоли перенастроен так, чтобы активно захватывать глутамин, прокачивать его через энергетический цикл клетки и перенаправлять в синтез итаконата — всё с целью поддержания высоких уровней онкогена-фузии. 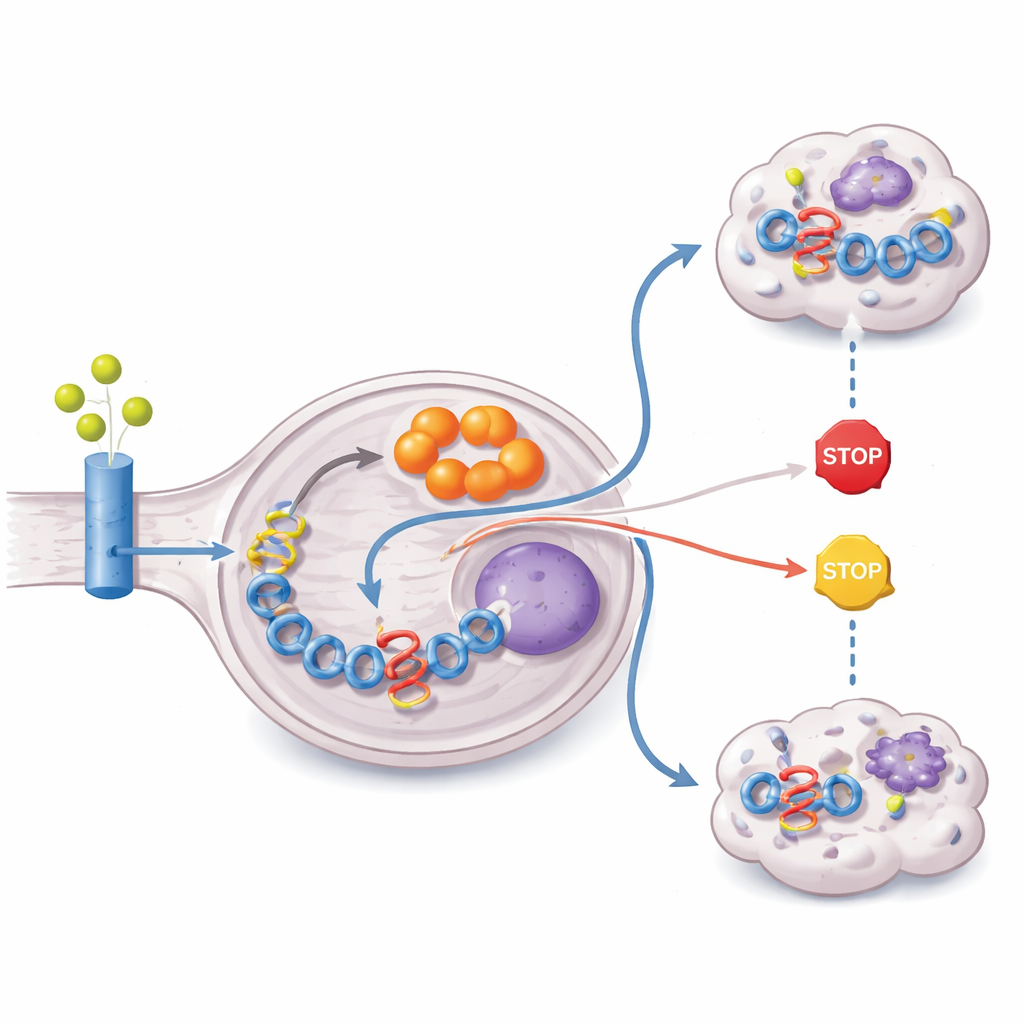
Атака по месту кормления опухоли
Поскольку эта цепочка состоит из нескольких отдельных шагов, она предлагает множество мишеней для лекарств. Авторы протестировали соединения, блокирующие импорт глутамина, глутаминазу, ACOD1 или путь PI3K–mTOR, а также проникающий в мозг антагонист глутамина JHU‑083. Клетки с фузией оказались существенно более чувствительны к этим агентам, чем другие подтипы эпендимом, а у обработанных мышей наблюдалась более долгая выживаемость и меньшие опухоли. Особенно примечательно, что блокада ACOD1 или сочетание антагонизма глутамина с ингибицией PI3K–mTOR не только уменьшали первичные опухоли мозга, но и предотвращали или устраняли метастазы в спинном мозге в мышиных моделях — очаги, которые особенно трудно лечить у пациентов.
Что это значит для пациентов и семей
Для неспециалиста главный вывод таков: эти эпендимомы «зависимы» от специфической метаболической петли собственного производства. Они захватывают метаболит иммунных клеток — итаконат — и обычное питательное вещество, глутамин, чтобы поддерживать включённым свой главный онкоген. Проследив эту петлю полностью, исследование выделяет несколько существующих или разрабатывающихся типов препаратов — направленных на использование глутамина, ACOD1 или сигналинг PI3K–mTOR — которые можно комбинировать, чтобы избирательно ослабить опухоли ZFTA–RELA при минимальном вреде для нормального мозга. Хотя эти результаты пока доклинические и не готовы для рутинного лечения, они прокладывают ясный путь к целевым терапиям для детского рака мозга, для которого в настоящее время мало эффективных вариантов.
Цитирование: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Ключевые слова: эпендимома, метаболизм опухолей мозга, итаконат, зависимость от глутамина, эпигенетическая терапия