Clear Sky Science · de
ZFTA–RELA-Ependymome stellen Itaconat her, um epigenetisch die Fusions‑Expression zu treiben
Warum diese Geschichte über Hirnkrebs wichtig ist
Ependymome sind seltene, aber aggressive Hirntumoren, die häufig Kinder und junge Erwachsene betreffen. Für viele Patientinnen und Patienten können Operation und Bestrahlung den Tumor zwar vorübergehend in Schach halten, heilen ihn jedoch selten. Diese Studie enthüllt eine überraschende Schwäche in einem häufigen Subtyp dieser Tumoren: Sie sind auf ein wenig bekanntes Molekül, Itaconat, angewiesen, um ihr wichtigstes krebserregendes Gen eingeschaltet zu halten. Indem die Forschenden nachverfolgen, wie der Tumor dieses Molekül herstellt und nutzt, zeigen sie mehrere neue Ansatzpunkte auf, mit denen künftige Medikamente diese Tumoren abschalten könnten.
Eine gefährliche Fusion im Gehirn
Mehr als die Hälfte der Ependymome, die im oberen Bereich des Gehirns entstehen, tragen eine genetische Verschmelzung namens ZFTA–RELA. Für sich genommen sind die beiden ursprünglichen Gene harmlos, aber in Fusion erzeugen sie einen starken Krebs‑Treiber, der in den Zellkern gelangt und die Art und Weise, wie DNA abgelesen wird, neu justiert. Bisher konzentrierte sich die Arbeit an ZFTA–RELA vor allem auf seine Rolle in der Gensteuerung. Die neue Studie stellte eine andere Frage: Programmieren diese Fusionen auch den Tumorstoffwechsel um — das Netzwerk chemischer Reaktionen, das Energie und Bausteine liefert — auf eine Weise, die therapeutisch nutzbar wäre?
Ein Makrophagen‑Molekül auf die dunkle Seite gezogen
Anhand von Maus‑Stammzellen aus dem Gehirn, die so verändert wurden, dass sie die Fusion tragen, patientenabgeleiteten Tumorzellen und Mausmodellen analysierte das Team Hunderte von Metaboliten. Ein Molekül hob sich stark hervor: Itaconat, das normalerweise von Immunzellen (Makrophagen) während einer Infektion gebildet wird. Die Tumorzellen produzierten große Mengen Itaconat über ein Enzym namens ACOD1, dessen Menge im Einklang mit ZFTA–RELA anstieg und fiel. Das Herunterregeln von ACOD1 oder dessen Hemmung mit kleinen Molekülen war toxisch für Fusion‑positive Zellen und ließ Tumoren bei Mäusen schrumpfen, während die Zugabe von zusätzlichem Itaconat das Tumorwachstum rettete. Diese Ergebnisse zeigen, dass der Krebs einen Weg der Immunzellen für sein eigenes Überleben kapert. 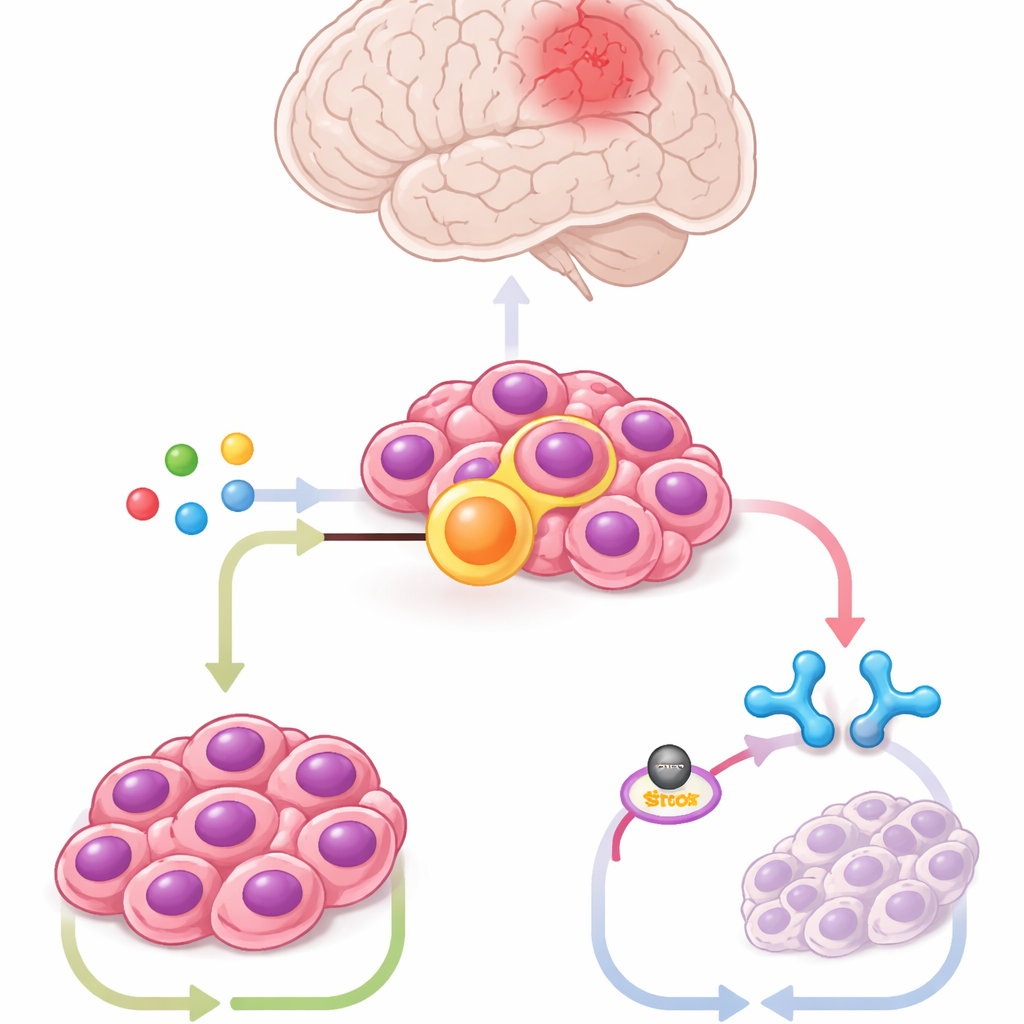
Eine sich selbst verstärkende Schleife in der Tumor‑Genkontrolle
Warum sollte Itaconat so wichtig sein? Die Antwort liegt in der Epigenetik — chemischen Markierungen an DNA‑verpackenden Proteinen, die bestimmen, welche Gene aktiv sind. Die Autorinnen und Autoren entdeckten, dass Itaconat eine Enzymfamilie (KDM5) hemmt, die normalerweise eine aktivierende Markierung namens H3K4me3 von Histonen entfernt. Wenn KDM5 blockiert ist, baut sich H3K4me3 auf, besonders an wichtigen Kontrollregionen des ZFTA‑Gens, die Teil der ZFTA–RELA‑Fusion sind. Diese verstärkte Markierung steigert die Transkription der Fusion selbst und erzeugt eine Vorwärtskopplung: ZFTA–RELA schaltet ACOD1 an, ACOD1 produziert Itaconat, und Itaconat erhöht wiederum die Expression von ZFTA–RELA. Das Unterbrechen von ACOD1 oder das Nachahmen der KDM5‑Aktivität brach diese Schleife, senkte das Fusionsprotein und verlangsamte das Tumorwachstum in mehreren Modellen.
Glutamin: der Treibstoff hinter der Fusion
Die Studie verfolgte danach, woher der Tumor das Rohmaterial zur Itaconat‑Herstellung bezieht. Durch die Fütterung der Zellen mit glutamin‑ und glukoseformen, die mit schwerem Kohlenstoff markiert waren, zeigten die Forschenden, dass der Großteil des Kohlenstoffgerüsts von Itaconat aus Glutamin stammt. ZFTA–RELA‑Tumoren überexprimieren Glutamintransporter und das Enzym Glutaminase und zeigen aktivierte PI3K–AKT–mTOR‑Signalgebung, einen Weg, der bekannt dafür ist, die Glutaminnutzung zu fördern. Gleichzeitig stillt die Fusion epigenetisch PTEN, einen kritischen Tumorsuppressor, der diese Signalgebung normalerweise einschränkt. Das Resultat ist ein umverdrahteter Stoffwechsel, der Glutamin hereinzieht, es durch den zellulären Energiestoffwechsel leitet und es in die Itaconatproduktion umleitet — alles, um hohe Pegel des Fusions‑Treibers aufrechtzuerhalten. 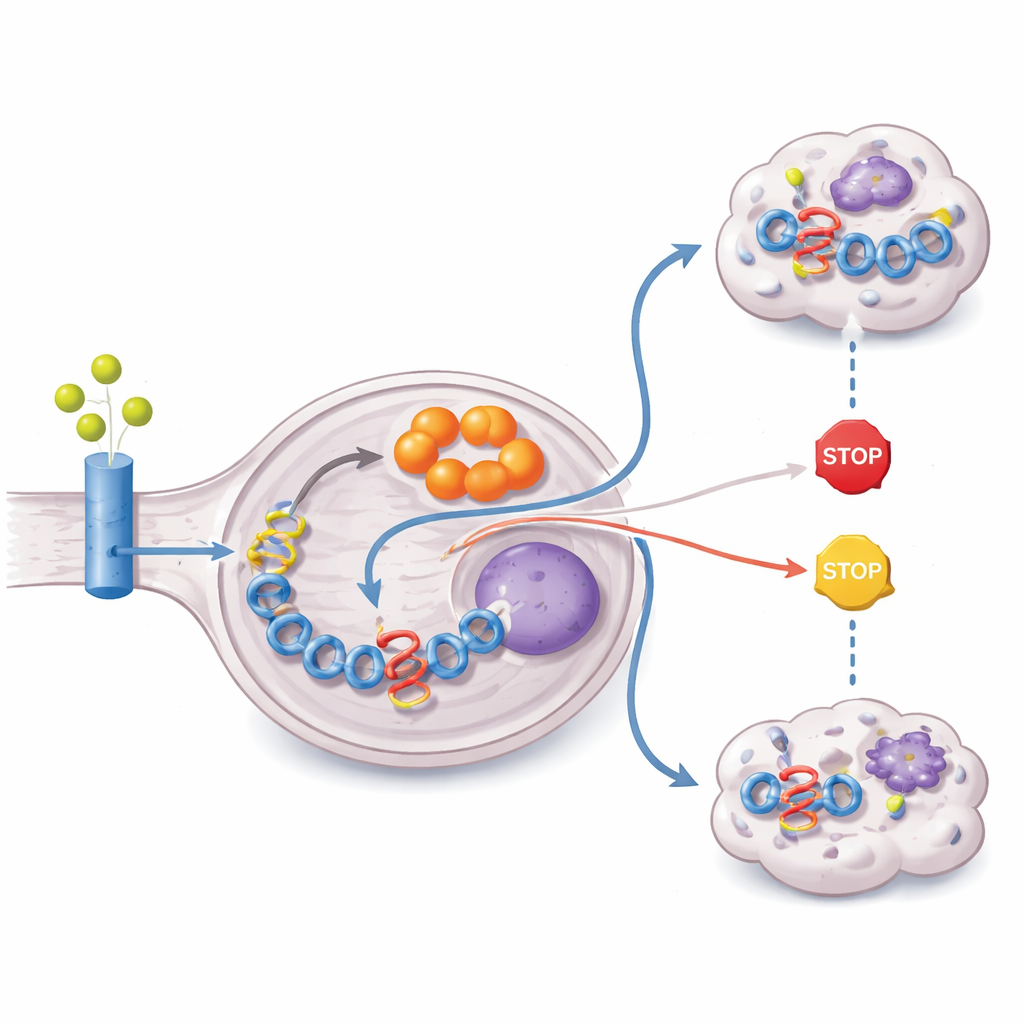
Dem Tumor dort angreifen, wo er sich ernährt
Weil dieser Kreislauf mehrere diskrete Schritte umfasst, bietet er mehrere mögliche Medikamentenziele. Die Autorinnen und Autoren testeten Verbindungen, die den Glutaminimport, die Glutaminase, ACOD1 oder den PI3K–mTOR‑Weg blockieren, sowie einen gehirngängigen Glutaminantagonisten namens JHU‑083. Fusion‑positive Zellen waren gegenüber diesen Wirkstoffen deutlich empfindlicher als andere Ependymom‑Subtypen, und behandelte Mäuse lebten länger und hatten kleinere Tumoren. Besonders auffällig war, dass die Blockade von ACOD1 oder die Kombination von Glutaminantagonismus mit PI3K–mTOR‑Hemmung nicht nur primäre Hirntumoren verringerte, sondern in Mausmodellen auch Rückenmarkmetastasen verhinderte oder beseitigte — Läsionen, die für Patientinnen und Patienten besonders schwer zu behandeln sind.
Was das für Patientinnen, Patienten und Familien bedeutet
Für Nicht‑Spezialisten ist die Hauptaussage, dass diese Ependymome von einer spezifischen, von ihnen selbst geschaffenen metabolischen Schleife abhängig sind. Sie kapern ein Metabolit der Immunzellen, Itaconat, und eine verbreitete Nährstoffquelle, Glutamin, um ihr zentrales Krebsgen eingeschaltet zu halten. Indem die Studie diese Schleife vom Anfang bis zum Ende kartiert, identifiziert sie mehrere bereits existierende oder in Entwicklung befindliche Wirkstofftypen — die auf Glutaminnutzung, ACOD1 oder PI3K–mTOR‑Signalgebung zielen — die kombiniert werden könnten, um ZFTA–RELA‑Tumoren selektiv zu schwächen und dabei normales Gehirngewebe weitgehend zu schonen. Obwohl diese Ergebnisse präklinisch sind und noch nicht für die routinemäßige Behandlung bereitstehen, weisen sie einen klaren Weg zu gezielten Therapien für einen kindlichen Hirntumor, für den es derzeit nur begrenzte wirksame Optionen gibt.
Zitation: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Schlüsselwörter: Ependymom, Gehirntumorstoffwechsel, Itaconat, Glutamin‑Abhängigkeit, epigenetische Therapie