Clear Sky Science · ar
أورام إبينديموما ZFTA–RELA تصنع الإيتاكونات لدفع التعبير عن الاندماج جينياً
لماذا تهم هذه القصة المتعلقة بسرطان الدماغ
الإبينديموما أورام دماغية نادرة لكنها عدوانية تصيب غالباً الأطفال والشباب. بالنسبة لكثير من المرضى، يمكن للجراحة والإشعاع أن تكبح تقدم السرطان مؤقتاً لكنها نادراً ما تشفيه. تكشف هذه الدراسة عن نقطة ضعف مفاجئة في أحد الأنماط الفرعية الشائعة من هذه الأورام: فهي تعتمد على جزيء غير معروف على نطاق واسع، الإيتاكونات، للحفاظ على تشغيل الجين المسبب للسرطان. من خلال تتبع كيفية إنتاج الورم لهذا الجزيء واستخدامه، يكشف الباحثون عن عدة طرق جديدة قد تسمح للأدوية المستقبلية بإيقاف هذه الأورام.
اندماج خطير في الدماغ
أكثر من نصف الإبينديموما التي تنشأ في الجزء العلوي من الدماغ تحمل خلطاً جينياً يسمى ZFTA–RELA. بمفردهما، الجينان الأصليان غير ضارين، لكن عندما يندمجان يخلقان مُشغّلاً قوياً للسرطان ينتقل إلى نواة الخلية ويُعيد برمجة كيفية قراءة الحمض النووي. إلى الآن، ركزت معظم الأبحاث على دور ZFTA–RELA في التحكم في الجينات. طرحت الدراسة الجديدة سؤالاً مختلفاً: هل يعيد هذا الاندماج أيضاً برمجة تمثيل الورم الغذائي — شبكة التفاعلات الكيميائية التي توفّر الطاقة والمواد البنائية — بطرق يمكن استغلالها للعلاج؟
جزيء من البلاعة المحببة تحول إلى الجانب المظلم
باستخدام خلايا جذعية من جذع الدماغ للفأر مُهندسة لحمل الاندماج، وخلايا ورمية مستمدة من مرضى، ونماذج فأرية، قام الفريق بتحليل مئات المستقلبات. برز واحد بوضوح: الإيتاكونات، جزيء يُنتَج عادةً بواسطة خلايا مناعية تسمى البلاعات أثناء العدوى. صنعت خلايا الورم كميات كبيرة من الإيتاكونات عبر إنزيم يسمى ACOD1، وارتفعت وانخفضت مستويات هذا الإنزيم بالتزامن مع ZFTA–RELA. كان تثبيط ACOD1 أو منعه بجزيئات صغيرة ساماً للخلايا الإيجابية للاندماج ومُصغِّراً للأورام في الفئران، بينما أعاد إضافة الإيتاكونات نمو الورم. تُظهر هذه النتائج أن السرطان قد استولى على مسار خلايا مناعية لصالح بقائه. 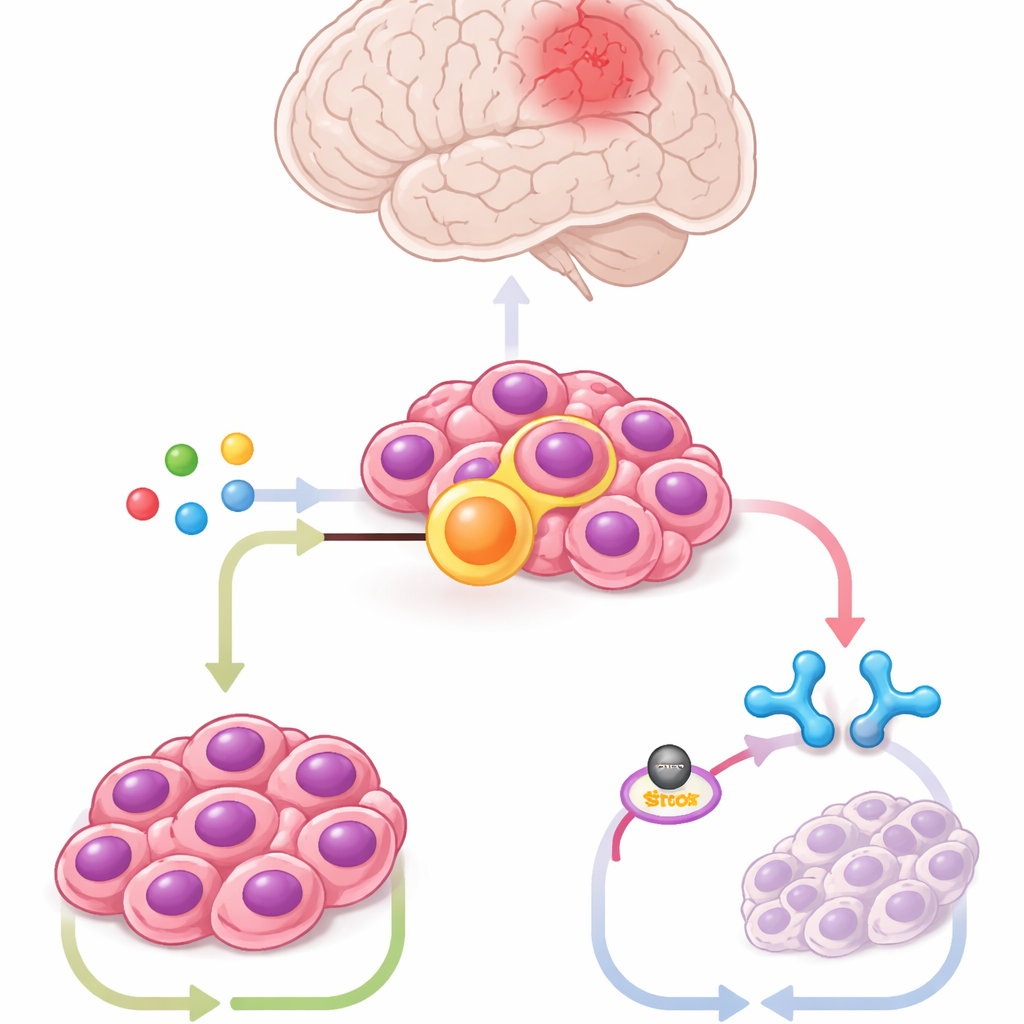
حلقة معززة ذاتياً في ضبط الحمض النووي للورم
لماذا يكون الإيتاكونات مهماً بهذا القدر؟ يكمن الجواب في علم فوق الجينات — علامات كيميائية على بروتينات تغليف الحمض النووي تحدد أي الجينات نشطة. اكتشف المؤلفون أن الإيتاكونات يثبط عائلة من الإنزيمات (KDM5) التي تزيل عادةً علامة تفعيل تسمى H3K4me3 من الهستونات. عندما تُمنع KDM5، تتراكم H3K4me3، خصوصاً في مناطق تحكم رئيسية من جين ZFTA التي تشارك في اندماج ZFTA–RELA. يعمل هذا التمييز المتزايد على تعزيز نسخ الاندماج نفسه، مكوناً حلقة تغذية أمامية: ZFTA–RELA يشغّل ACOD1، وACOD1 يصنع الإيتاكونات، والإيتاكونات بدورها يعزّز تعبير ZFTA–RELA. كسر الحلقة بتعطيل ACOD1 أو بمحاكاة نشاط KDM5 خفض هذا الاندماج، وأقلل من نمو الأورام في نماذج متعددة.
الغلوتامين: الوقود وراء الاندماج
تتبعت الدراسة بعد ذلك من أين يحصل الورم على المواد الخام لصنع الإيتاكونات. عن طريق تغذية الخلايا أشكالاً من الغلوكامين والجلوكوز الموسومة بالكربون الثقيل، أظهر الباحثون أن معظم هيكل الكربون في الإيتاكونات يأتي من الغلوتامين. تعبر أورام ZFTA–RELA عن ناقلات غلوتامين وإنزيم الغلوتاميناز بمستويات مرتفعة، وتظهر تنشيط مسار PI3K–AKT–mTOR، وهو مسار معروف بدفع استخدام الغلوتامين. في الوقت نفسه، يقوم الاندماج بكبت فوق جيني لـ PTEN، وهو مساعد سرطاني حاسم يقيّد هذا المسار عادةً. والنتيجة هي إعادة توصيل استقلابية تسحب الغلوتامين، توجهه عبر دورة طاقة الخلية، وتحوّله إلى إنتاج الإيتاكونات، وكل ذلك للحفاظ على مستويات عالية من مُشغّل الاندماج. 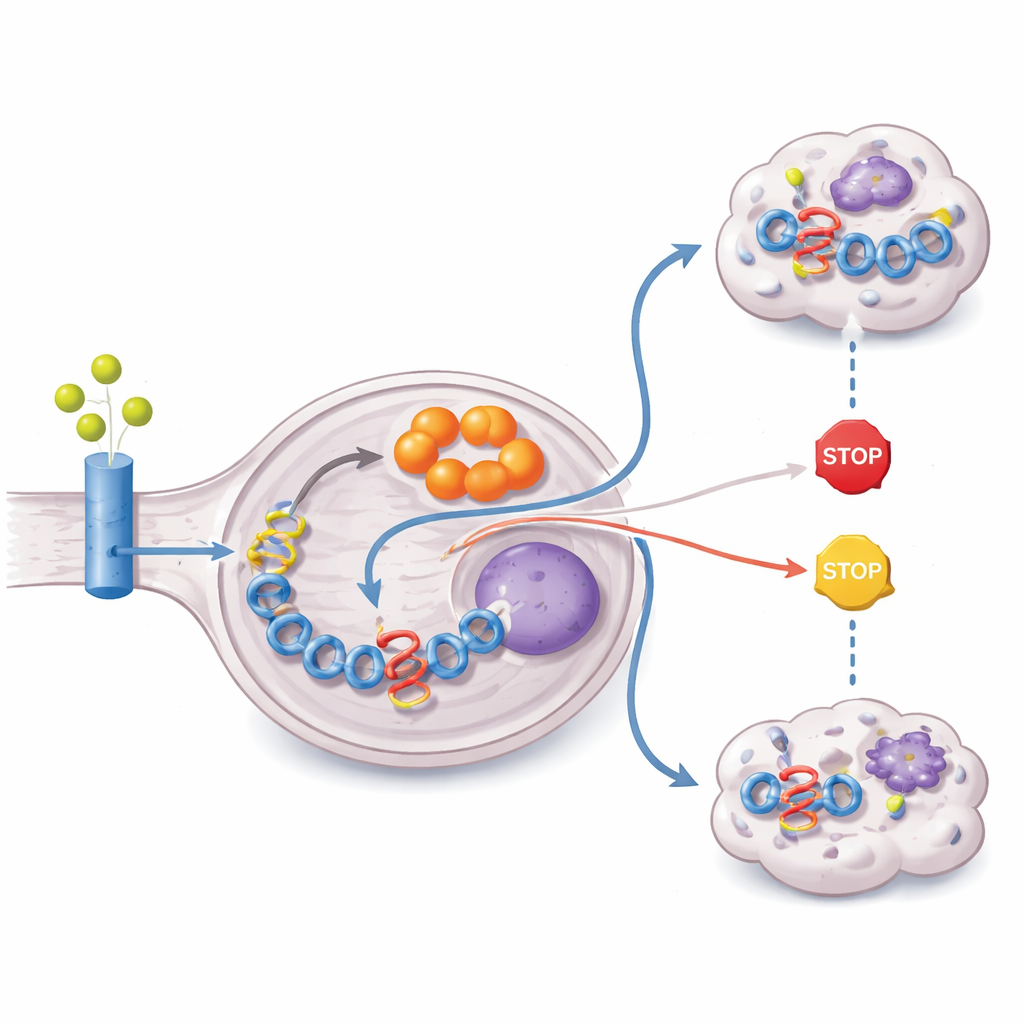
مهاجمة الورم حيث يتغذى
لأن هذه الدائرة تحتوي على عدة خطوات متميزة، فهي تقدم أهدافاً دوائية متعددة. اختبر المؤلفون مركبات تعيق دخول الغلوتامين، الغلوتاميناز، ACOD1، أو مسار PI3K–mTOR، بالإضافة إلى مضاد للغلوتامين قادر على اختراق الدماغ يُدعى JHU‑083. كانت الخلايا الإيجابية للاندماج أكثر حساسية بكثير لهذه العوامل من الأنماط الفرعية الأخرى من الإبينديموما، وعاشت الفئران المعالجة لفترات أطول مع أورام أصغر. وبشكل لافت، فإن منع ACOD1 أو الجمع بين مكافح الغلوتامين وكبح PI3K–mTOR لم يقلص فقط الأورام الدماغية الأولية بل منع أو قضى أيضاً على نَقْلات الحبل الشوكي في نماذج الفأر — آفات يصعب علاجها بشكل خاص لدى المرضى.
ماذا يعني هذا للمرضى والعائلات
لغير المتخصص، الرسالة الأساسية هي أن هذه الإبينديموما مدمِّنة على حلقة استقلابية محددة صنعتها بنفسها. تخطف مَستقلباً خلوياً مناعياً، الإيتاكونات، ومغذٍ شائعاً، الغلوتامين، للحفاظ على تشغيل جين السرطان الرئيسي لديها. من خلال رسم هذه الحلقة من البداية إلى النهاية، تحدد الدراسة عدة أنواع من الأدوية الموجودة أو الناشئة — تستهدف استخدام الغلوتامين، ACOD1، أو إشارة PI3K–mTOR — التي يمكن جمعها لإضعاف أورام ZFTA–RELA بشكل انتقائي مع حماية الدماغ الطبيعي. رغم أن هذه النتائج قبل سريرية وليست جاهزة للعلاج الروتيني بعد، فإنها تمهد طريقاً واضحاً نحو علاجات موجهة لسرطان دماغي طفولي يفتقر حالياً إلى خيارات فعالة.
الاستشهاد: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
الكلمات المفتاحية: إبينديموما, تمثيل غذائي لأورام الدماغ, الإيتاكونات, اعتماد على الغلوتامين, العلاج فوق الجيني