Clear Sky Science · ja
ZFTA–RELA 融合髄芽腫はイタコネートを作り出し、融合遺伝子の発現をエピジェネティックに駆動する
なぜこの脳腫瘍の話が重要か
髄芽腫はまれながら攻撃的な脳腫瘍で、しばしば小児や若年成人に発症します。多くの患者では手術や放射線で一時的に病勢を抑えられても根治には至らないことが多い。本研究は、この腫瘍の一般的な亜型の一つに意外な弱点があることを明らかにしました:主要な発癌遺伝子の発現を維持するために、あまり知られていない分子イタコネートに依存しているのです。腫瘍がこの分子をどのように作り利用しているかをたどることで、将来の薬剤がこのがんを止めるためのいくつかの新たな手段が示されます。
脳内に現れる危険な融合遺伝子
上位脳で発生する髄芽腫の半数以上は ZFTA–RELA と呼ばれる遺伝子融合を持ちます。元の二つの遺伝子は単独では無害ですが、融合すると核内に入り込み、DNAの読み取り方を再配線する強力な発癌因子になります。これまで ZFTA–RELA に関する研究の多くは遺伝子制御に注目してきました。本研究は別の問いを立てました:この融合は腫瘍の代謝、すなわちエネルギーや構成要素を供給する化学反応のネットワークをも再プログラムし、治療に利用できる脆弱性を生むのだろうか?
マクロファージ由来分子の“闇への転用”
融合を導入したマウス脳幹細胞、患者由来腫瘍細胞、マウスモデルを用いて数百の代謝物をプロファイリングしたところ、ひときわ目立ったのがイタコネートでした。イタコネートは通常、感染時にマクロファージと呼ばれる免疫細胞が産生する分子です。腫瘍細胞は ACOD1 という酵素を介して大量のイタコネートを産生しており、その発現は ZFTA–RELA と歩調を合わせて増減しました。ACOD1 をノックダウンするか小分子で阻害すると融合陽性細胞に対して毒性を示し、マウスの腫瘍は縮小しました。一方でイタコネートを外から補うと腫瘍成長が回復しました。これらの結果は、腫瘍が生存のために本来免疫細胞で働く経路を自分のものにしていることを示しています。 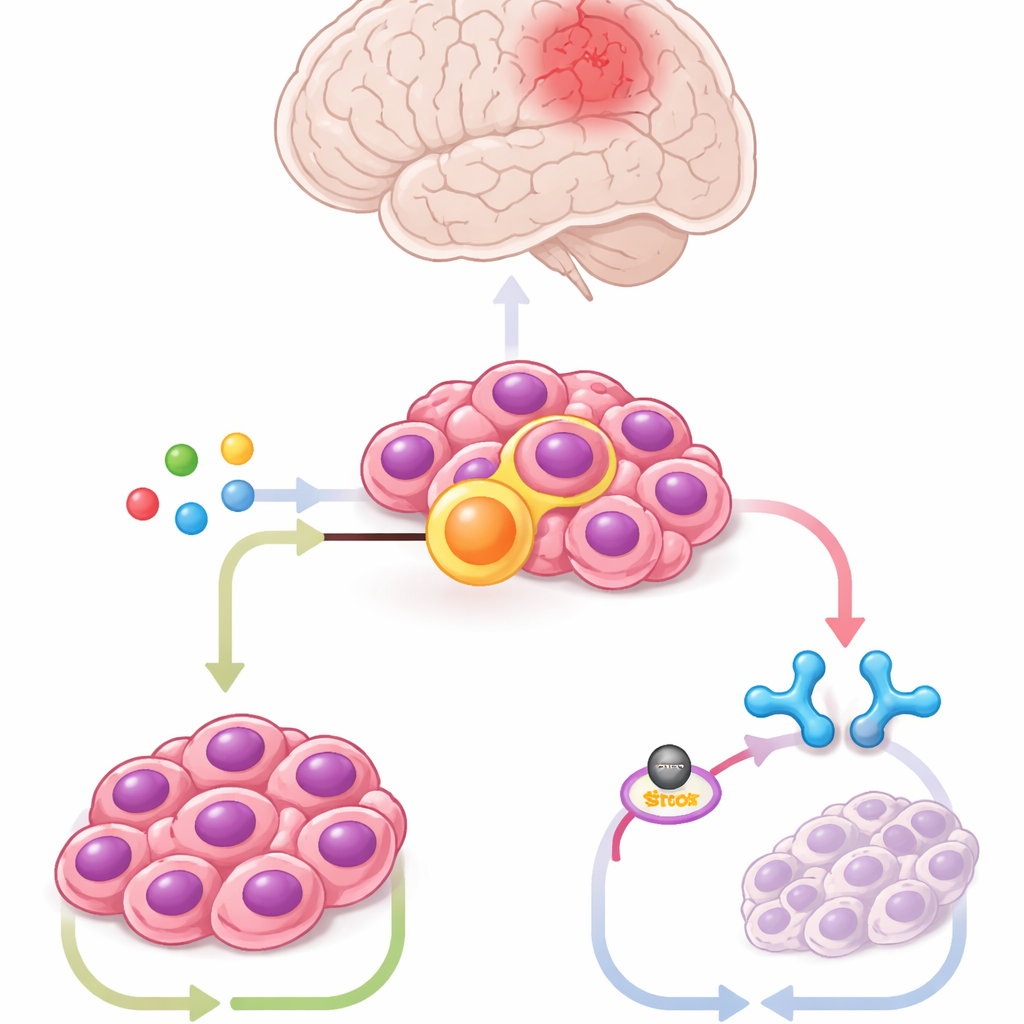
腫瘍の遺伝子制御における自己増幅ループ
なぜイタコネートがこれほど重要なのか。答えはエピジェネティクスにあります—DNAを包むタンパク質(ヒストン)に付く化学的標識がどの遺伝子が活性化されるかを決めます。著者らはイタコネートが、通常ヒストンから活性化マークである H3K4me3 を除去する酵素群(KDM5)を阻害することを発見しました。KDM5 が阻害されると H3K4me3 は蓄積し、特に ZFTA–RELA 融合の一部である ZFTA 遺伝子の重要な制御領域で顕著に増えました。この増加した標識は融合遺伝子の転写を高め、フィードフォワードループを作ります:ZFTA–RELA が ACOD1 をオンにし、ACOD1 がイタコネートを作り、イタコネートがさらに ZFTA–RELA の発現を促進するのです。ACOD1 を破壊するか KDM5 の働きを模倣するとこのループは壊れ、融合タンパク質が低下し、複数のモデルで腫瘍成長が遅延しました。
融合を支える燃料:グルタミン
研究は次に、腫瘍がイタコネートを作るための原料をどこから得ているかを追跡しました。重炭素で標識したグルタミンやグルコースを細胞に与えることで、イタコネートの炭素骨格の大部分がグルタミン由来であることが示されました。ZFTA–RELA 腫瘍はグルタミン輸送体と酵素グルタミナーゼを過剰発現し、グルタミン利用を促進することで知られる PI3K–AKT–mTOR シグナルが活性化していました。同時に融合はこのシグナルを抑える重要な腫瘍抑制因子 PTEN をエピジェネティックにサイレンシングしていました。その結果、グルタミンを大量に取り込み、エネルギー代謝サイクルを経てそれをイタコネート産生へと振り向け、融合ドライバーの高発現を維持するよう代謝が書き換えられているのです。 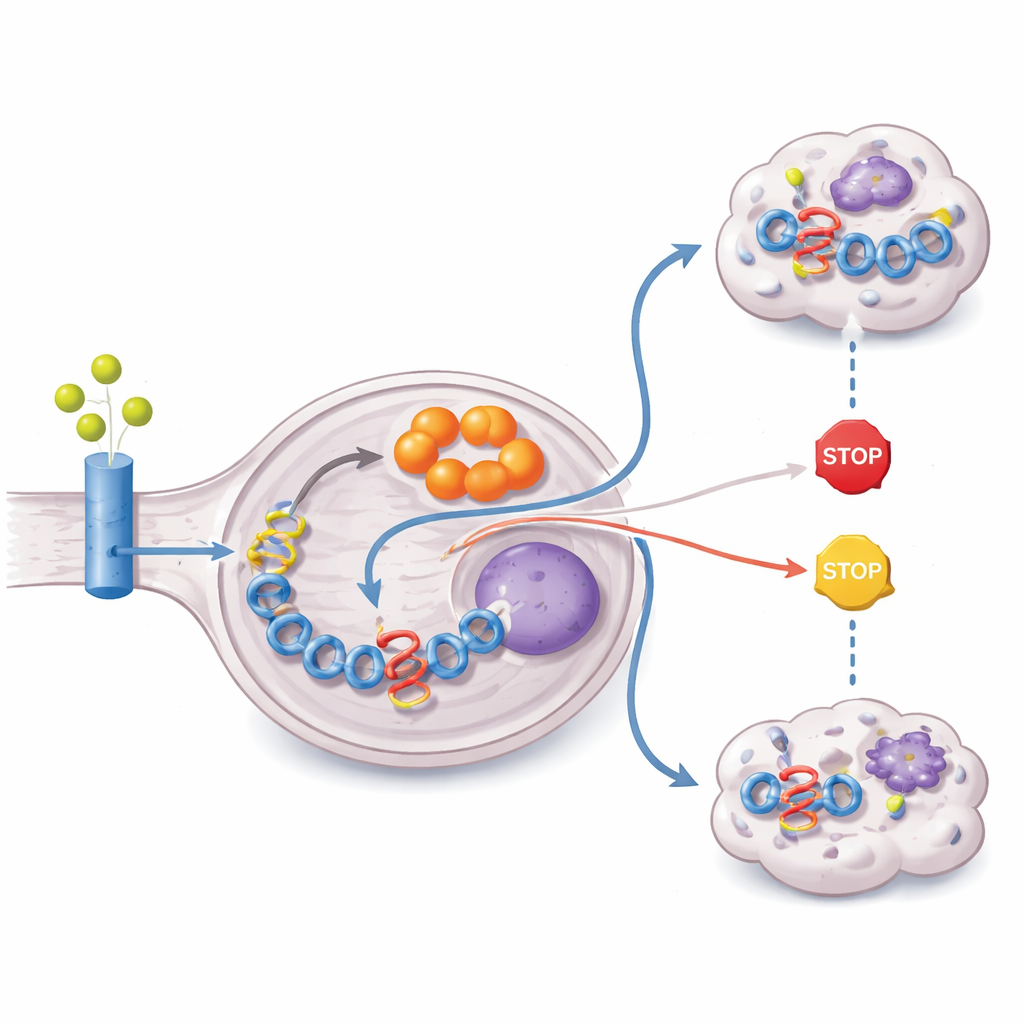
腫瘍の“給餌”を断つ
この回路は複数の分岐点があるため、いくつもの薬剤標的を提供します。著者らはグルタミン取り込み阻害、グルタミナーゼ阻害、ACOD1 阻害、PI3K–mTOR 経路阻害、さらに脳浸透性のグルタミン拮抗薬 JHU‑083 といった化合物を試しました。融合陽性細胞は他の髄芽腫亜型よりこれらの薬剤に遥かに感受性が高く、処置を受けたマウスは腫瘍が小さくなり生存期間が延びました。特に印象的だったのは、ACOD1 を阻害するかグルタミン拮抗と PI3K–mTOR 阻害を組み合わせることで、原発性脳腫瘍を縮小させるだけでなく、マウスモデルで脊髄転移を予防または消失させたことで、患者で治療が難しい病変にも効きうる可能性を示しています。
患者と家族にとっての意味
専門外の人向けに言えば、この髄芽腫は自ら作り出した特定の代謝ループに依存しているということが主要なメッセージです。腫瘍は免疫細胞由来の代謝物イタコネートと、一般的な栄養素グルタミンを乗っ取り、主要な発癌遺伝子のスイッチを入れ続けます。このループを端から端まで明らかにすることで、グルタミン利用、ACOD1、あるいは PI3K–mTOR シグナルを標的とする既存または新興の薬剤群を組み合わせて ZFTA–RELA 腫瘍を選択的に弱め、正常な脳をなるべく温存する戦略が示されました。これらの結果は前臨床段階でありまだ日常診療に直ちに適用できるものではありませんが、小児期に発症し有効な治療法が限られる脳腫瘍に対する標的治療への明確な道筋を描いています。
引用: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
キーワード: 脈絡叢腫(※訳注:原語は ependymoma), 脳腫瘍の代謝, イタコネート, グルタミン依存, エピジェネティック療法