Clear Sky Science · it
ZFTA–RELA ependimomi producono itaconato per guidare epigeneticamente l’espressione della fusione
Perché questa storia sul cancro al cervello è importante
Gli ependimomi sono tumori cerebrali rari ma aggressivi che colpiscono spesso bambini e giovani adulti. Per molti pazienti, chirurgia e radioterapia possono contenere temporaneamente la malattia ma raramente la curano. Questo studio scopre una vulnerabilità sorprendente in un sottotipo comune di questi tumori: dipendono da una molecola poco conosciuta, l’itaconato, per mantenere attivo il loro principale gene oncogenico. Tracciando come il tumore produce e utilizza questa molecola, i ricercatori rivelano diversi nuovi punti di intervento che futuri farmaci potrebbero sfruttare per bloccare questi tumori.
Una fusione pericolosa nel cervello
Più della metà degli ependimomi che insorgono nella parte superiore del cervello presenta un ibrido genetico chiamato ZFTA–RELA. I due geni originali sono innocui da soli, ma quando si fondono creano un potente driver tumorale che si sposta nel nucleo cellulare e riscrive il modo in cui il DNA viene letto. Finora, la maggior parte degli studi su ZFTA–RELA si è concentrata sul suo ruolo nel controllo genico. Il nuovo lavoro pone una domanda diversa: questa fusione riprogramma anche il metabolismo del tumore — la rete di reazioni chimiche che fornisce energia e mattoncini — in modi che possano essere sfruttati terapeuticamente?
Una molecola dei macrofagi voltata al lato oscuro
Usando cellule staminali del tronco encefalico di topo ingegnerizzate per portare la fusione, cellule tumorali derivate da pazienti e modelli murini, il team ha profilato centinaia di metaboliti. Uno è emerso in modo netto: l’itaconato, una molecola normalmente prodotta dalle cellule immunitarie chiamate macrofagi durante l’infezione. Le cellule tumorali producevano grandi quantità di itaconato tramite un enzima chiamato ACOD1, i cui livelli salivano e scendevano in sincronia con ZFTA–RELA. L’abbattimento di ACOD1 o il suo blocco con piccole molecole era tossico per le cellule positive alla fusione e riduceva i tumori nei topi, mentre l’aggiunta di itaconato esogeno ripristinava la crescita tumorale. Questi risultati mostrano che il cancro ha cooptato una via delle cellule immunitarie per la propria sopravvivenza. 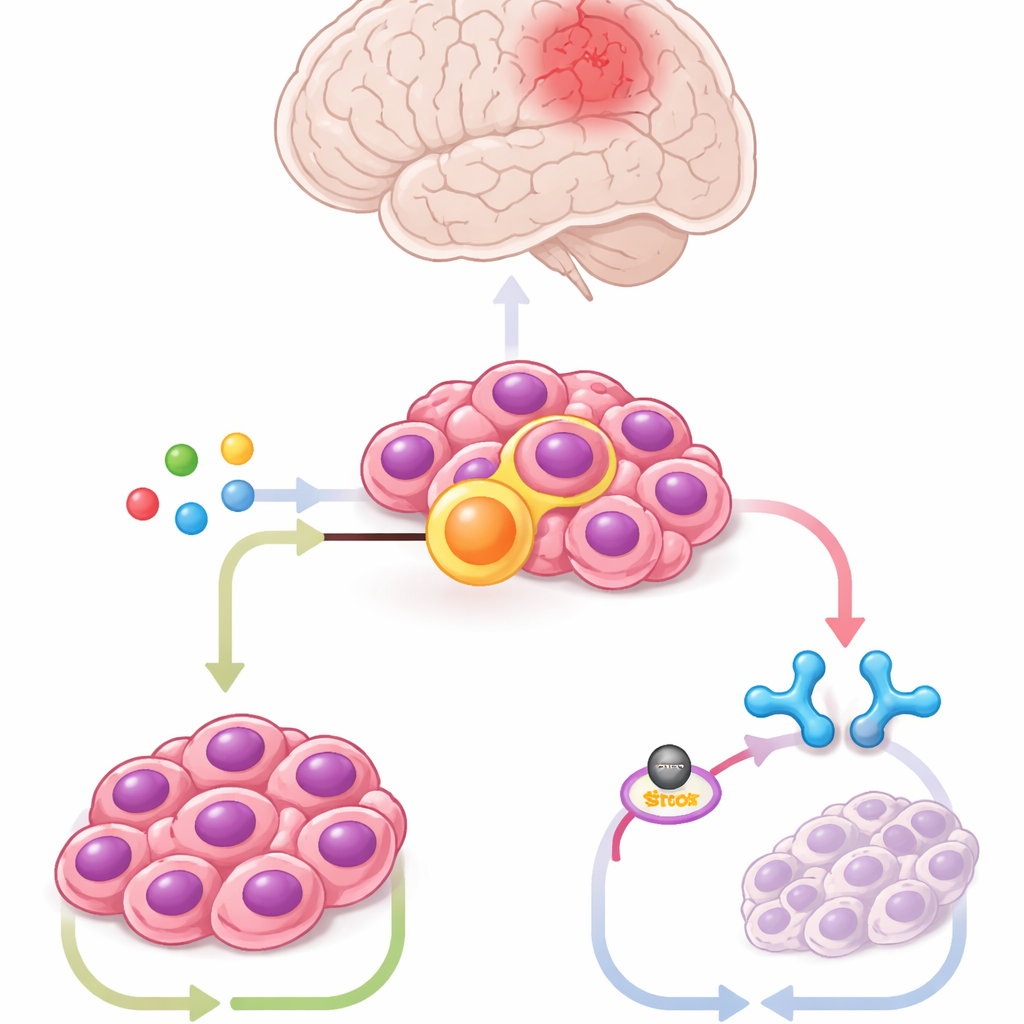
Un circuito auto‑rinforzante nel controllo del DNA del tumore
Perché l’itaconato sarebbe così importante? La risposta si trova nell’epigenetica — marcatori chimici sulle proteine che impacchettano il DNA che determinano quali geni sono attivi. Gli autori hanno scoperto che l’itaconato inibisce una famiglia di enzimi (KDM5) che normalmente rimuovono un marcatore attivante chiamato H3K4me3 dalle istoni. Quando KDM5 è bloccato, H3K4me3 si accumula, soprattutto in regioni di controllo chiave del gene ZFTA che fanno parte della fusione ZFTA–RELA. Questo aumento dei marcatori potenzia la trascrizione della fusione stessa, creando un circuito a retroazione positiva: ZFTA–RELA attiva ACOD1, ACOD1 produce itaconato, e l’itaconato a sua volta aumenta l’espressione di ZFTA–RELA. Interrompere ACOD1 o mimare l’attività di KDM5 rompe questo circuito, riduce la proteina di fusione e rallenta la crescita tumorale in diversi modelli.
Glutamina: il carburante dietro la fusione
Lo studio ha poi ricostruito da dove il tumore ottiene la materia prima per produrre itaconato. Alimentando le cellule con forme di glutamina e glucosio marcate con carbonio pesante, i ricercatori hanno mostrato che la maggior parte dello scheletro carbonioso dell’itaconato proviene dalla glutamina. I tumori ZFTA–RELA sovraesprimono trasportatori della glutamina e l’enzima glutaminasi, e mostrano l’attivazione della via PI3K–AKT–mTOR, un percorso noto per guidare l’uso della glutamina. Allo stesso tempo, la fusione silenzia epigeneticamente PTEN, un soppressore tumorale critico che normalmente frena questa segnalazione. Il risultato è un metabolismo riscritto che attrae glutamina, la convoglia attraverso il ciclo energetico cellulare e la devia verso la produzione di itaconato, il tutto per sostenere alti livelli del driver di fusione. 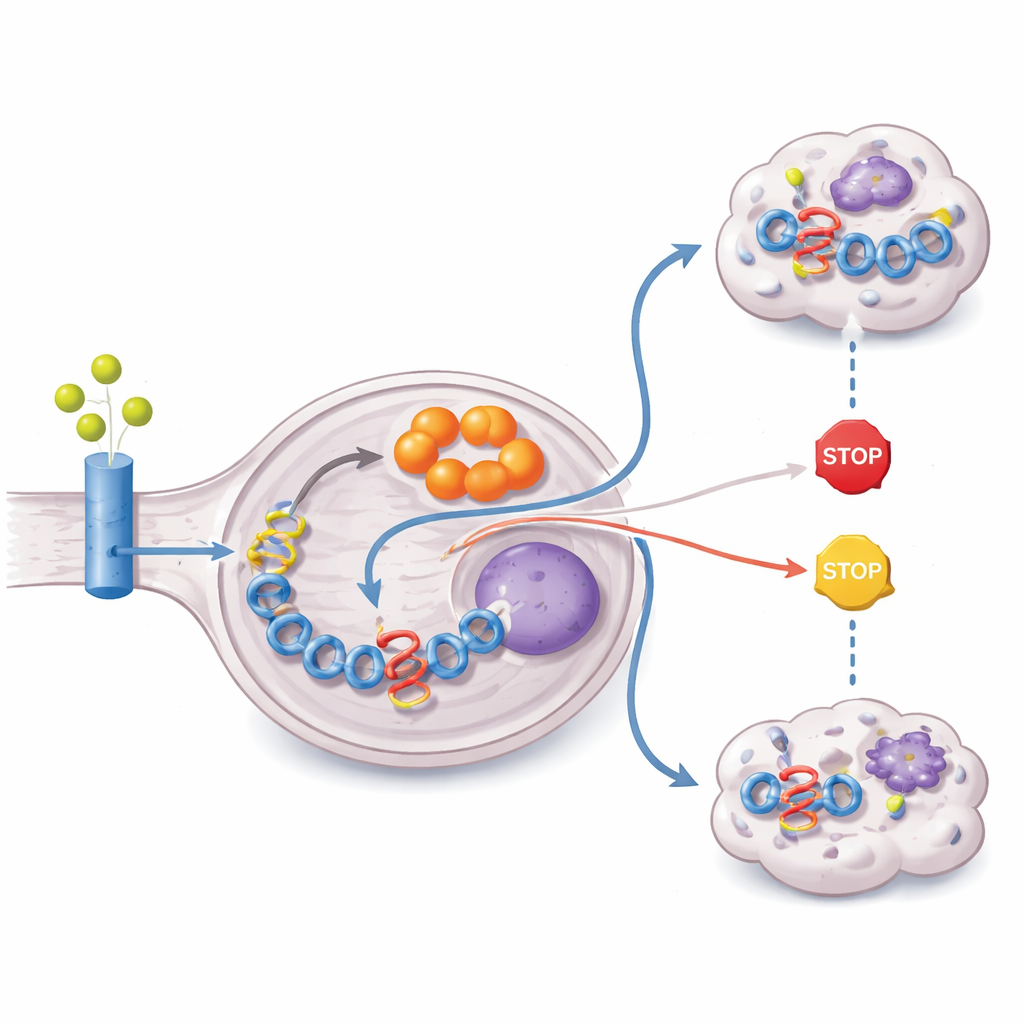
Colpire il tumore dove si nutre
Poiché questo circuito ha diversi passaggi distinti, offre molteplici bersagli farmacologici. Gli autori hanno testato composti che bloccano l’importazione della glutamina, la glutaminasi, ACOD1 o la via PI3K–mTOR, oltre a un antagonista della glutamina capace di attraversare la barriera emato‑encefalica chiamato JHU‑083. Le cellule positive per la fusione erano molto più sensibili a questi agenti rispetto ad altri sottotipi di ependimoma, e i topi trattati vivevano più a lungo con tumori più piccoli. Particolarmente rilevante, il blocco di ACOD1 o la combinazione di antagonismo della glutamina con l’inibizione di PI3K–mTOR non solo riduceva i tumori cerebrali primari ma preveniva o eliminava anche metastasi del midollo spinale nei modelli murini — lesioni particolarmente difficili da trattare nei pazienti.
Cosa significa per pazienti e famiglie
Per un non specialista, il messaggio chiave è che questi ependimomi sono dipendenti da un circuito metabolico specifico di cui sono artefici. Dirottano un metabolita delle cellule immunitarie, l’itaconato, e un nutriente comune, la glutamina, per mantenere acceso il loro principale gene cancerogeno. Mappando questo circuito dall’inizio alla fine, lo studio identifica diversi tipi di farmaci esistenti o in sviluppo — che mirano all’uso della glutamina, ad ACOD1 o alla segnalazione PI3K–mTOR — che potrebbero essere combinati per indebolire selettivamente i tumori ZFTA–RELA risparmiando il tessuto cerebrale normale. Sebbene questi risultati siano preclinici e non ancora pronti per l’uso clinico routinario, tracciano un percorso chiaro verso terapie mirate per un tumore cerebrale infantile che attualmente manca di opzioni efficaci.
Citazione: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Parole chiave: ependimoma, metabolismo dei tumori cerebrali, itaconato, dipendenza dal glutamine, terapia epigenetica