Clear Sky Science · fr
Les épendymomes ZFTA–RELA produisent de l’itaconate pour activer épigénétiquement l’expression de la fusion
Pourquoi cette découverte sur le cancer du cerveau compte
Les épendymomes sont des tumeurs cérébrales rares mais agressives qui touchent souvent les enfants et les jeunes adultes. Pour de nombreux patients, la chirurgie et la radiothérapie peuvent contenir la maladie temporairement, mais guérissent rarement. Cette étude met au jour une vulnérabilité surprenante d’un sous‑type fréquent de ces tumeurs : elles dépendent d’une molécule peu connue, l’itaconate, pour maintenir l’expression de leur principal gène cancérigène. En retraçant la façon dont la tumeur fabrique et utilise cette molécule, les chercheurs révèlent plusieurs nouvelles stratégies que de futurs médicaments pourraient exploiter pour arrêter ces cancers.
Une fusion dangereuse dans le cerveau
Plus de la moitié des épendymomes situés dans la partie supérieure du cerveau portent une recombinaison génétique appelée ZFTA–RELA. Pris séparément, les deux gènes originels sont inoffensifs, mais fusionnés ils forment un puissant moteur oncogénique qui se rend dans le noyau cellulaire et réorganise la lecture de l’ADN. Jusqu’ici, la plupart des travaux sur ZFTA–RELA se concentraient sur son rôle dans le contrôle des gènes. La nouvelle étude pose une question différente : cette fusion reprogramme‑t‑elle aussi le métabolisme tumoral — le réseau de réactions chimiques fournissant énergie et éléments de construction — d’une manière exploitable en thérapie ?
Une molécule des macrophages détournée du bon côté
En utilisant des cellules souches du tronc cérébral de souris modifiées pour porter la fusion, des cellules tumorales dérivées de patients et des modèles murins, l’équipe a profilé des centaines de métabolites. Un composé s’est particulièrement distingué : l’itaconate, une molécule normalement produite par des cellules immunitaires appelées macrophages lors d’une infection. Les cellules tumorales produisaient de grandes quantités d’itaconate via une enzyme nommée ACOD1, dont l’expression variait en parallèle de celle de ZFTA–RELA. Inhiber ACOD1 par ARN ou avec de petites molécules était toxique pour les cellules porteuses de la fusion et réduisait les tumeurs chez la souris, tandis que l’apport d’itaconate supplémentaire restaurait la croissance tumorale. Ces résultats montrent que le cancer a détourné une voie propre aux cellules immunitaires pour sa survie. 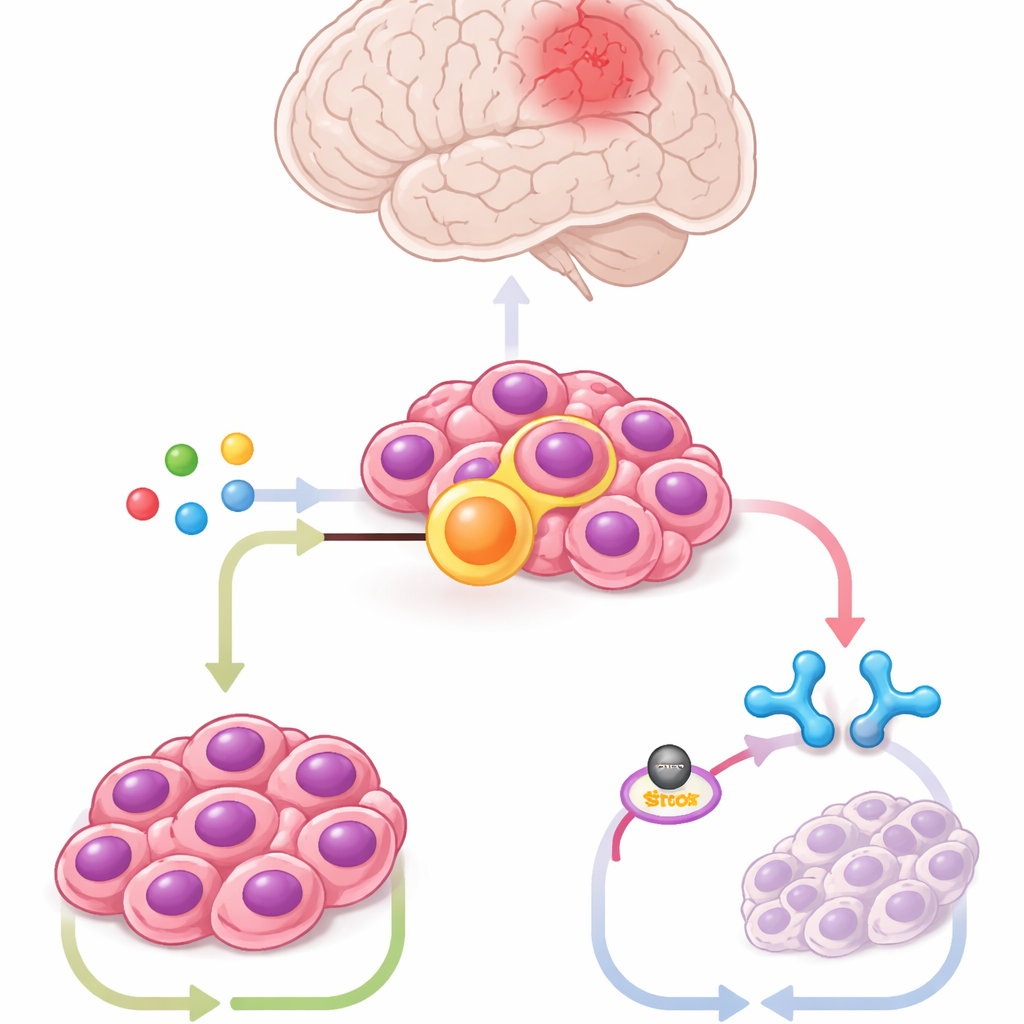
Une boucle auto‑renforçante dans le contrôle épigénétique
Pourquoi l’itaconate est‑il si important ? La réponse tient à l’épigénétique — des marques chimiques sur les protéines qui empaquettent l’ADN et déterminent quels gènes sont actifs. Les auteurs ont découvert que l’itaconate inhibe une famille d’enzymes (KDM5) qui retirent normalement une marque activatrice appelée H3K4me3 des histones. Quand KDM5 est bloquée, H3K4me3 s’accumule, en particulier sur des régions régulatrices clés du gène ZFTA impliquées dans la fusion ZFTA–RELA. Cet accroissement des marques stimule la transcription de la fusion elle‑même, créant une boucle en feed‑forward : ZFTA–RELA active ACOD1, ACOD1 produit de l’itaconate, et l’itaconate renforce à son tour l’expression de ZFTA–RELA. Rompre ACOD1 ou restaurer l’activité de KDM5 brisait cette boucle, réduisait la protéine de fusion et ralentissait la croissance tumorale dans plusieurs modèles.
Glutamine : le carburant derrière la fusion
L’étude a ensuite retracé d’où provient la matière première pour fabriquer l’itaconate. En nourrissant les cellules avec des formes de glutamine et de glucose marquées par du carbone lourd, les chercheurs ont montré que la majeure partie du squelette carboné de l’itaconate provient de la glutamine. Les tumeurs ZFTA–RELA surexpriment des transporteurs de glutamine et l’enzyme glutaminase, et présentent une activation de la voie PI3K–AKT–mTOR, connue pour stimuler l’utilisation de la glutamine. Parallèlement, la fusion réprime épigénétiquement PTEN, un suppresseur tumoral critique qui limite normalement cette signalisation. Le résultat est un métabolisme réorienté qui attire la glutamine, la canalise via le cycle énergétique de la cellule et la détourne vers la production d’itaconate, afin de maintenir des niveaux élevés du moteur de la fusion. 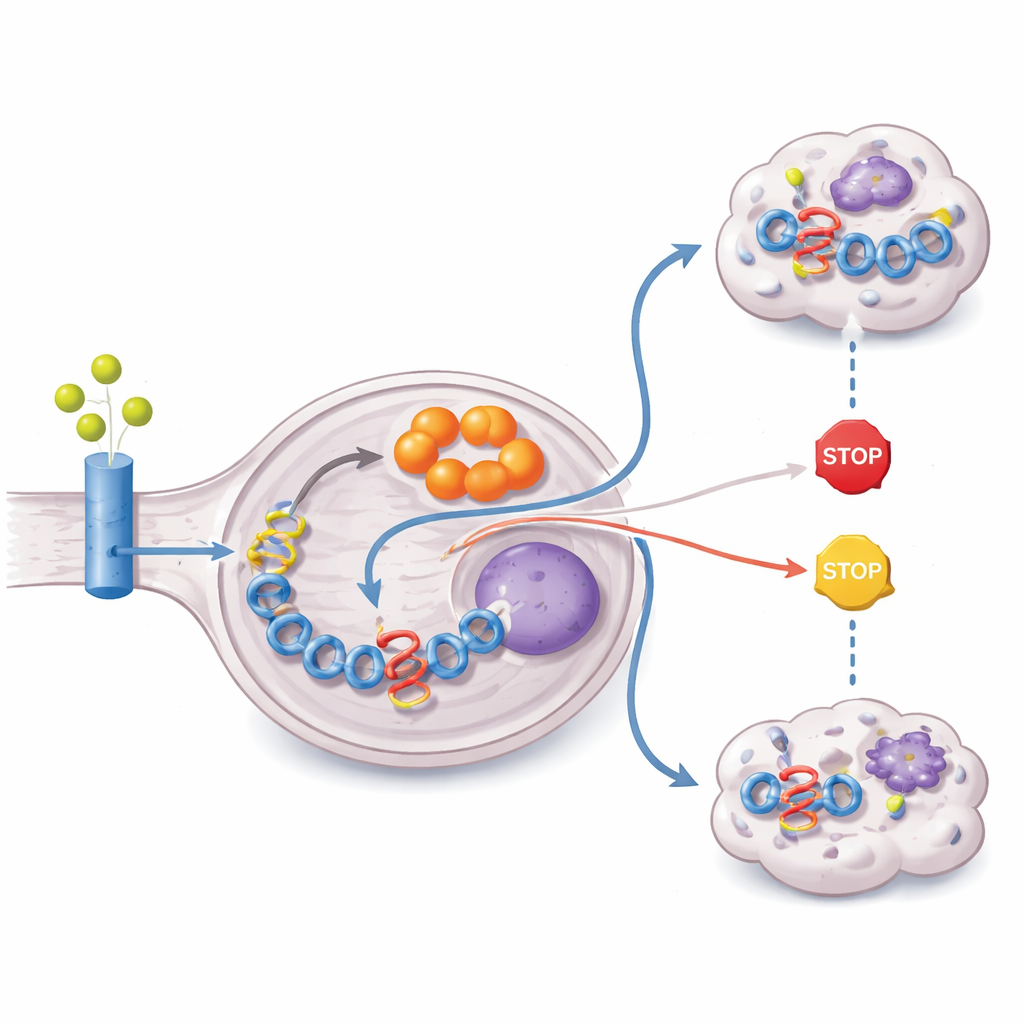
Frapper la tumeur là où elle se nourrit
Parce que ce circuit comporte plusieurs étapes distinctes, il offre de multiples cibles médicamenteuses. Les auteurs ont testé des composés bloquant l’import de glutamine, la glutaminase, ACOD1 ou la voie PI3K–mTOR, ainsi qu’un antagoniste de la glutamine capable de traverser la barrière hémato‑encéphalique nommé JHU‑083. Les cellules porteuses de la fusion étaient bien plus sensibles à ces agents que d’autres sous‑types d’épendymome, et les souris traitées vivaient plus longtemps avec des tumeurs plus petites. Fait particulièrement marquant : bloquer ACOD1 ou combiner l’antagonisme de la glutamine avec l’inhibition PI3K–mTOR réduisait non seulement les tumeurs cérébrales primaires mais prévenait ou éliminait aussi les métastases de la moelle épinière chez la souris — des lésions particulièrement difficiles à traiter chez les patients.
Ce que cela signifie pour les patients et les familles
Pour un non‑spécialiste, le message clé est que ces épendymomes sont dépendants d’une boucle métabolique spécifique qu’ils ont eux‑mêmes instaurée. Ils détournent un métabolite des cellules immunitaires, l’itaconate, et un nutriment courant, la glutamine, pour maintenir leur gène oncogénique principal activé. En cartographiant cette boucle de bout en bout, l’étude identifie plusieurs classes de médicaments existantes ou en développement — ciblant l’utilisation de la glutamine, ACOD1 ou la signalisation PI3K–mTOR — qui pourraient être combinées pour affaiblir sélectivement les tumeurs ZFTA–RELA tout en épargnant le tissu cérébral normal. Bien que ces résultats soient précliniques et pas encore applicables en routine clinique, ils tracent une voie claire vers des thérapies ciblées pour un cancer cérébral pédiatrique qui manque aujourd’hui d’options efficaces.
Citation: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Mots-clés: épendymome, métabolisme des tumeurs cérébrales, itaconate, addiction au glutamine, thérapie épigénétique