Clear Sky Science · sv
ZFTA–RELA‑ependymom producerar itakonat för att epigenetiskt driva fusionsuttryck
Varför den här berättelsen om hjärncancer är viktig
Ependymom är sällsynta men aggressiva hjärntumörer som ofta drabbar barn och unga vuxna. För många patienter kan kirurgi och strålning hålla cancern i schack en tid men sällan bota den. Denna studie avslöjar en överraskande svaghet i en vanlig undergrupp av dessa tumörer: de är beroende av en relativt okänd molekyl, itakonat, för att hålla sitt huvudorsakande genfusionsuttryck påslaget. Genom att följa hur tumören tillverkar och använder denna molekyl visar forskarna flera nya sätt som framtida läkemedel skulle kunna stänga ner dessa cancerformer.
En farlig fusion i hjärnan
Mer än hälften av ependymom som uppstår i övre delen av hjärnan bär på en genetisk sammanslagning kallad ZFTA–RELA. Var för sig är de två ursprungliga generna ofarliga, men när de slås ihop skapas en potent cancerdrivare som går in i cellkärnan och omprogrammerar hur DNA läses. Hittills har de flesta studier av ZFTA–RELA fokuserat på dess roll i genreglering. Den nya studien ställde en annan fråga: omprogrammerar denna fusion också tumörens metabolism — nätverket av kemiska reaktioner som ger energi och byggstenar — på sätt som kan utnyttjas terapeutiskt?
En makrofagmolekyl använd åt fel håll
Med musstamceller från hjärnan som konstruerats att bära fusionen, tumörceller från patienter och musmodeller profilerade teamet hundratals metaboliter. En stack ut markant: itakonat, en molekyl som normalt produceras av immunceller kallade makrofager vid infektion. Tumörcellerna producerade stora mängder itakonat via enzymet ACOD1, vars nivåer steg och föll i takt med ZFTA–RELA. Nedsättning av ACOD1 eller blockering med småmolekyler var giftigt för fusion‑positiva celler och krympte tumörer hos möss, medan tillsatt itakonat räddade tumörtillväxten. Dessa resultat visar att cancern har kapat en immuncells‑väg för sin egen överlevnad. 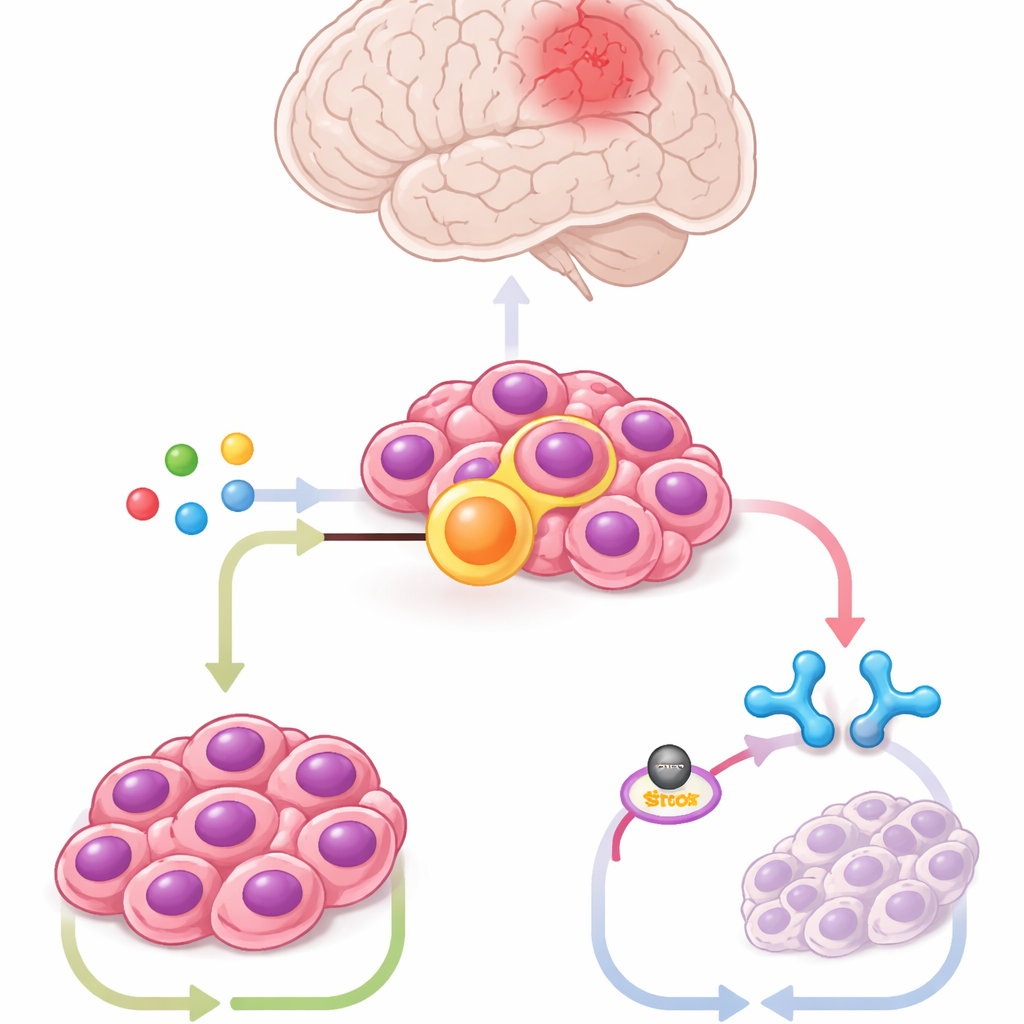
Ett självförstärkande kretslopp i tumörens DNA‑reglering
Varför skulle itakonat vara så viktigt? Svaret ligger i epigenetik — kemiska markörer på DNA‑paketerande proteiner som bestämmer vilka gener som är aktiva. Författarna upptäckte att itakonat hämmar en enzymfamilj (KDM5) som normalt tar bort en aktiverande markör kallad H3K4me3 från histoner. När KDM5 blockeras byggs H3K4me3 upp, särskilt vid nyckelreglerande regioner i ZFTA‑genen som ingår i ZFTA–RELA‑fusionen. Denna ökade märkning förstärker transkriptionen av fusionen själv och skapar ett framåtdrivande kretslopp: ZFTA–RELA slår på ACOD1, ACOD1 tillverkar itakonat, och itakonat stärker i sin tur uttrycket av ZFTA–RELA. Att störa ACOD1 eller efterlikna KDM5‑aktivitet bröt detta kretslopp, sänkte nivåerna av fusionsproteinet och bromsade tumörtillväxt i flera modeller.
Glutamin: bränslet bakom fusionen
Studien spårade sedan varifrån tumören får råmaterialet för att göra itakonat. Genom att mata celler med former av glutamin och glukos märkta med tungt kol visade forskarna att större delen av itakonatets kolskelett kommer från glutamin. ZFTA–RELA‑tumörer överuttrycker glutamintransportörer och enzymet glutaminas, och uppvisar aktiverad PI3K–AKT–mTOR‑signalering, en bana känd för att driva glutaminanvändning. Samtidigt tystar fusionen epigenetiskt PTEN, en kritisk tumörsuppressor som normalt begränsar denna signalering. Resultatet är en omskriven metabolism som drar in glutamin, kanaliserar det genom cellens energicykel och leder det in i itakonatproduktion — allt för att upprätthålla höga nivåer av fusionsdrivaren. 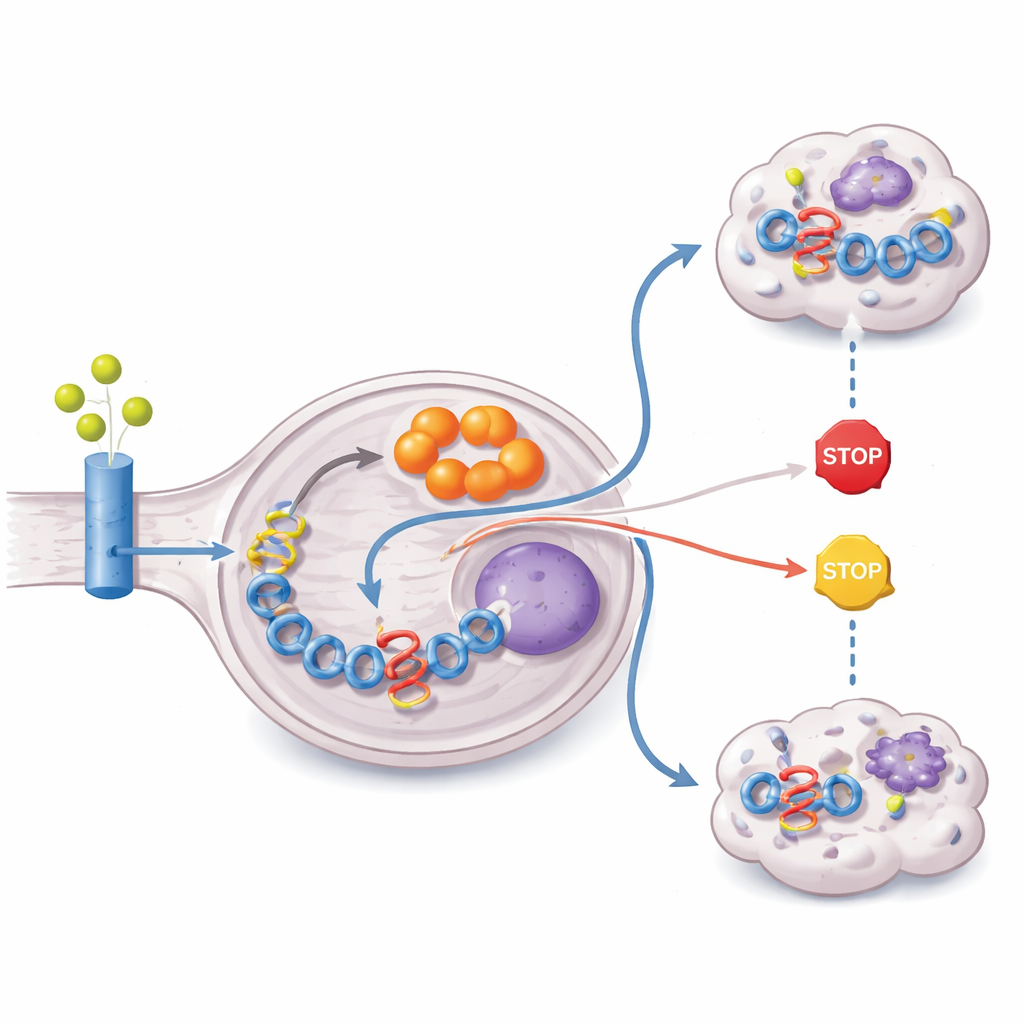
Att träffa tumören där den äter
Eftersom kretsen har flera distinkta steg erbjuder den flera läkemedelsmål. Författarna testade föreningar som blockerar glutaminimport, glutaminas, ACOD1 eller PI3K–mTOR‑vägen, samt en hjärngångbar glutaminantagonist kallad JHU‑083. Fusion‑positiva celler var mycket känsligare för dessa medel än andra ependymomsubtyper, och behandlade möss levde längre med mindre tumörer. Särskilt anmärkningsvärt var att blockad av ACOD1 eller kombinationen av glutaminantagonism med PI3K–mTOR‑inhibering inte bara minskade primära hjärntumörer utan också förhindrade eller eliminerade metastaser i ryggmärgen i musmodeller — lesioner som är särskilt svåra att behandla hos patienter.
Vad detta betyder för patienter och familjer
För en icke‑specialist är huvudbudskapet att dessa ependymom är beroende av ett specifikt metabolt kretslopp som de själva skapat. De kapar en immuncellmetabolit, itakonat, och en vanlig näringskälla, glutamin, för att hålla sin huvudcancergen påslagen. Genom att kartlägga kretsen från början till slut identifierar studien flera befintliga eller framväxande läkemedelstyper — som riktar sig mot glutaminanvändning, ACOD1 eller PI3K–mTOR‑signalering — som kan kombineras för att selektivt försvaga ZFTA–RELA‑tumörer samtidigt som normal hjärnvävnad i möjligaste mån skonas. Även om dessa resultat är prekliniska och ännu inte redo för rutinbehandling, pekar de ut en tydlig väg mot målinriktade terapier för en barndomshjärncancer som i dag saknar effektiva alternativ.
Citering: Natarajan, S.K., Lum, J., Skeans, J.H. et al. ZFTA–RELA ependymomas make itaconate to epigenetically drive fusion expression. Nature 652, 1004–1015 (2026). https://doi.org/10.1038/s41586-025-10005-1
Nyckelord: ependymom, hjärntumörmetabolism, itakonat, glutaminberoende, epigenetisk terapi